Clear Sky Science · nl
Fetale terugkeer uit verschillende lijnen onderhoudt de darmstamcelvoorraad en geeft stressresistentie
Hoe de darm zichzelf herstelt onder druk
Het slijmvlies van je darm is een van de drukst bewerkte weefsels in je lichaam. Het verteert voedsel, neemt voedingsstoffen op en beschermt tegen ziekteverwekkers, terwijl het zichzelf elke paar dagen vernieuwt. Dit artikel onderzoekt hoe dat kwetsbare oppervlak zware aanvallen — van ontsteking tot chemotherapie — overleeft door cellen tijdelijk terug te spoelen naar een meer fetale, flexibele toestand die helpt bij herstel en weerstand tegen schade.
De dagelijkse assemblagelijn in de darm
In gezonde darmen bevindt zich een gespecialiseerde groep cellen, crypt base columnar-cellen (CBC's), onderaan kleine kuiltjes die crypten worden genoemd. Deze stamcellen delen voortdurend en sturen hun nakomelingen omhoog richting de vingervormige villi die in de darmpijp uitsteken. Tijdens die reis rijpen de cellen uit tot verschillende functies, zoals absorberende enterocyten die voedingsstoffen opnemen, of secretorische cellen die slijm en antimicrobiële stoffen produceren. Onder normale omstandigheden zorgt deze boven-naar-benedenstroom voor een ordelijke en continue vernieuwing van het darmslijmvlies.
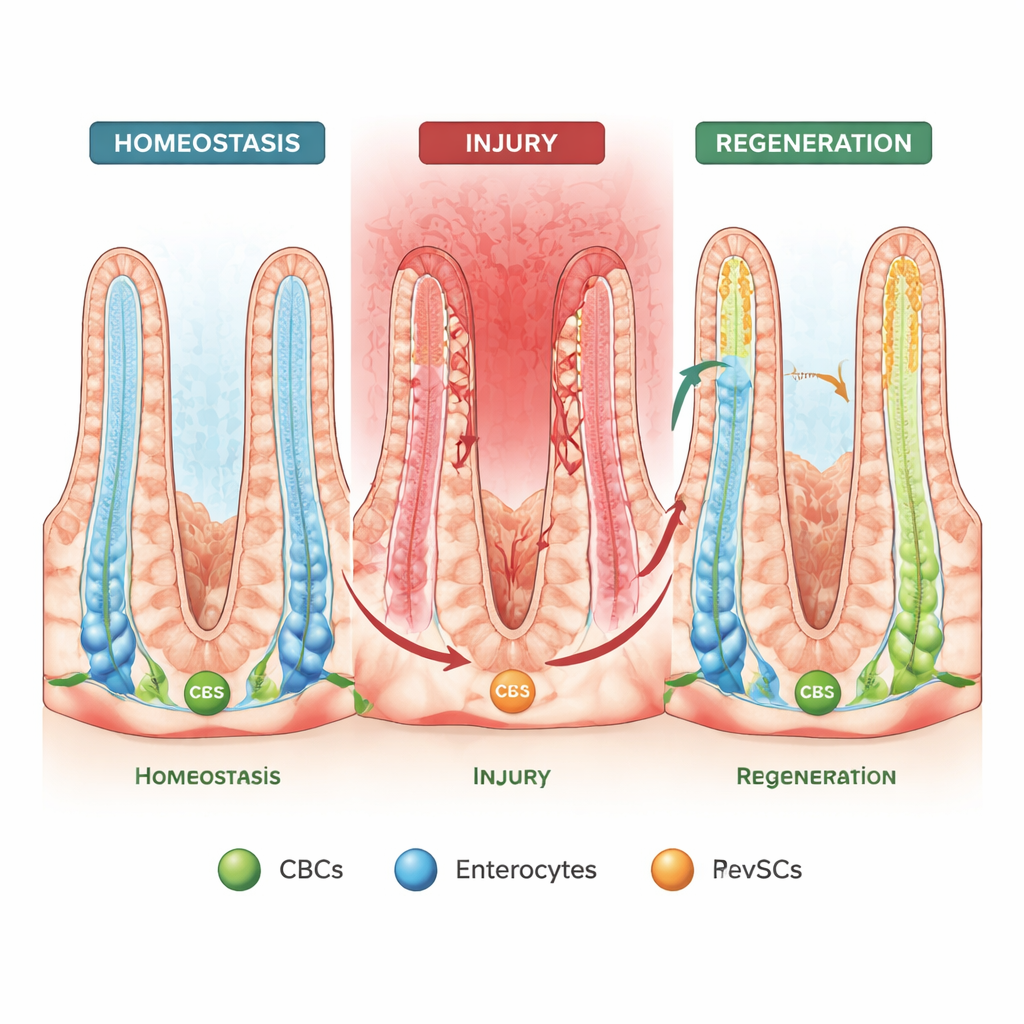
Cellen die de assemblagelijn achteruit kunnen laten lopen
Wanneer het darmslijmvlies beschadigd raakt en CBC's verloren gaan, toonden eerdere studies aan dat sommige volwassen cellen naar beneden de crypt kunnen "terugwandelen" en stamcelachtige eigenschappen kunnen herwinnen — een gedrag dat ruimtelijke plasticiteit wordt genoemd. Een tweede, nieuwere verschijnsel is "fetale terugkeer", waarbij cellen een genactiviteitspatroon aannemen dat lijkt op de ontwikkelende darm. In deze studie verbinden de auteurs deze twee ideeën met behulp van verfijnde organoïde (mini-darm) kweek, single-cell RNA-sequencing en linietracering in muizen. Ze identificeren een speciale fetale-achtige populatie, revival-stamcellen (revSC's), die zowel uit CBC's als uit gewone absorberende enterocyten kan ontstaan en vervolgens een volledige reeks darmceltypen kan regenereren.
Mini-darmen onthullen verborgen flexibiliteit
Om deze veranderingen in actie te bekijken kweekte het team muis- en humane darmorganoïden in twee verschillende gels. In Matrigel gedroegen organoïden zich als normaal volwassen weefsel, rijk aan CBC's en rijpe celtypen. In een collagengel werden organoïden echter gedomineerd door revSC-achtige cellen met een fetale genselectie. Single-cell analyses toonden aan dat revSC's langs twee hoofdroutes herleid konden worden: vanuit klassieke CBC's en vanuit absorberende enterocyten. Sorteerexperimenten bevestigden dat CBC's de grootste capaciteit hebben om in revSC's om te zetten, maar zelfs meer rijpe cellen konden dit doen wanneer ze in de juiste omgeving werden geplaatst. Cruciaal was dat gezuiverde revSC's terug naar Matrigel konden worden verplaatst en daar CBC's en alle belangrijke darmlijnen regenereren, wat bewijst dat de fetale-achtige staat zowel omkeerbaar als volledig functioneel is.
Villuscellen en schade in de echte wereld
De studie gaat een stap verder door te onderzoeken of deze flexibiliteit buiten het laboratorium optreedt. De onderzoekers labelden enterocyten in de villi van muizen en kweekten vervolgens ofwel villusfragmenten of stelden de dieren bloot aan het darmbeschadigende chemotherapiemedicijn 5-fluorouracil (5-FU). In collageen vormden villusfragmenten — normaal gesproken als arm aan stamcellen beschouwd — nieuwe organoïden die revSC-eigenschappen aannamen en later CBC-markers herwonnen wanneer ze naar standaardcondities werden teruggebracht. Toen deze "villus-afgeleide" organoïden werden getransplanteerd in colitismodellen, herbouwden ze gezond darmepitheel. In levende muizen behandeld met 5-FU begonnen gelabelde enterocyten revSC-markers te expressen en verschenen later als lange klonale strepen die nieuwe CBC's aan de basis van de crypt bevatten, wat bevestigt dat volwassen cellen waren ingesprongen om de stamcelvoorraad aan te vullen.
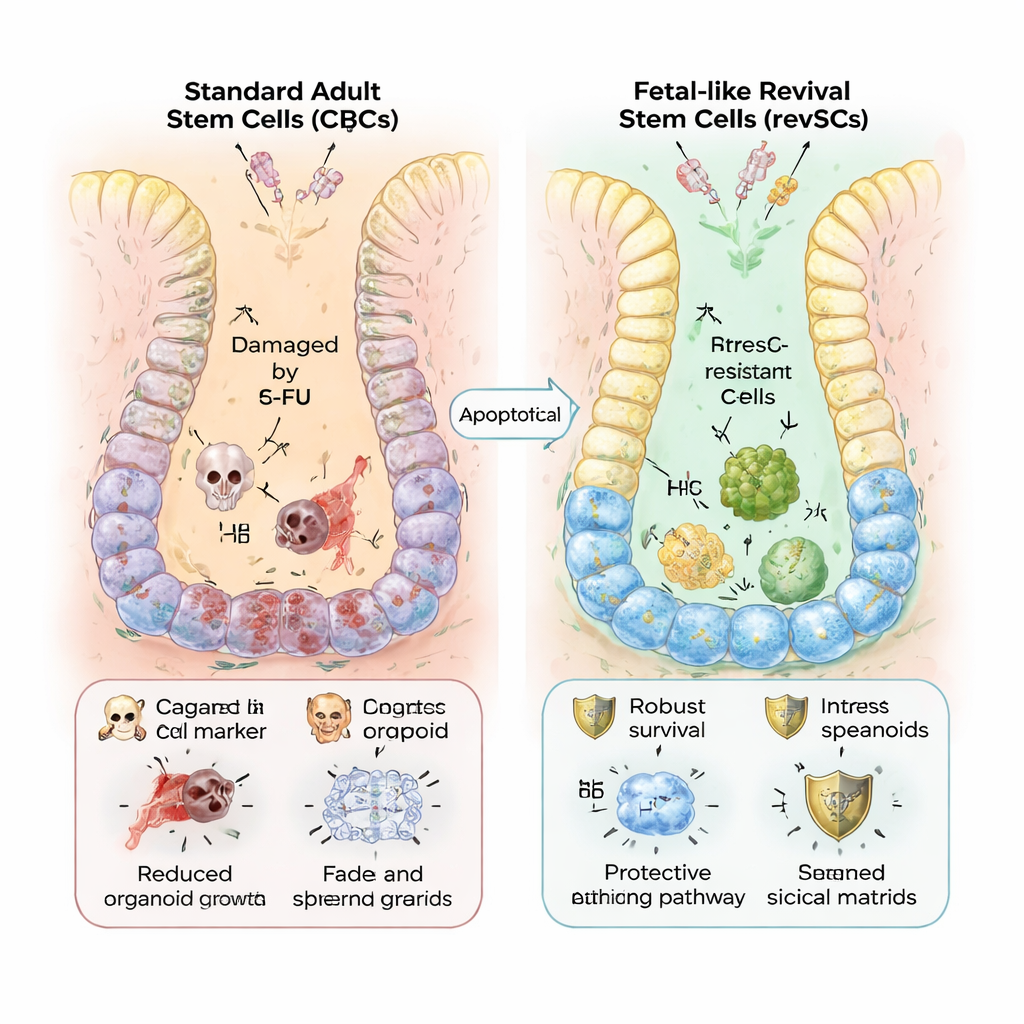
Stressbestendige herstelploegen
Waarom zou het lichaam deze fetale omweg gebruiken? De auteurs tonen aan dat revSC's veel beter bestand zijn tegen stress. Wanneer organoïden werden blootgesteld aan 5-FU, krimpten die in standaard Matrigel en toonden ze brede genprogramma's die gekoppeld zijn aan DNA-schade en paniekerige proliferatie. Collageengekweekte, revSC-rijke organoïden bleven daarentegen doorgroeien en vertoonden een rustiger, meer gerichte respons. Genanalyses toonden hogere activiteit van antioxidanten, anti-apoptotische eiwitten en hitteschokchaperonnes — moleculaire schilden die cellen helpen ontsteking en toxische aanvallen te overleven. Vergelijkbare patronen werden gezien in zowel muis- als humane cellen, en dezelfde revSC-genen zijn verhoogd in ontstoken menselijke darmen.
Wat dit betekent voor darmziekten en therapie
Voor niet-specialisten is de conclusie dat het darmslijmvlies een ingebouwd noodplan heeft. Wanneer ontsteking of medicijnen de gebruikelijke stamcellen bedreigen, kunnen zowel stamcellen als gewone absorberende cellen tijdelijk terugkeren naar een fetale, stressbestendige revSC-toestand. Van daaruit kunnen ze de normale stamcelcompartimenten herstellen en het weefsel herbouwen. Dit werk verenigt twee regeneratieconcepten — ruimtelijke plasticiteit en fetale terugkeer — tot een hiërarchie van herstel en suggereert dat het gecontroleerd benutten van dit flexibele, fetale programma behandelingen voor aandoeningen zoals inflammatoire darmziekte en colorectale kanker kan verbeteren, terwijl het ook waarschuwt dat ongecontroleerde terugkeer tumorvorming kan aanwakkeren.
Bronvermelding: Kirino, S., Uefune, F., Miyake, K. et al. Fetal reversion from diverse lineages sustains the intestinal stem cell pool and confers stress resilience. Commun Biol 9, 255 (2026). https://doi.org/10.1038/s42003-026-09533-x
Trefwoorden: darmstamcellen, weefselregeneratie, celplasticiteit, inflammatoire darmziekte, organoïden