Clear Sky Science · nl
Fluvastatine onderdrukt het ontstaan en de progressie van borstkanker door CYP4Z1 te richten
Waarom een cholesterolverlager van belang is bij borstkanker
Veel vrouwen die behandeld worden voor borstkanker ontwikkelen afwijkende bloedvetwaarden en lopen het voortdurende risico dat de ziekte terugkeert of zich verspreidt. Deze studie onderzoekt een intrigerend idee: kan een veelgebruikt cholesterolverlagend middel, fluvastatine, een nieuwe toepassing krijgen om borstkanker te vertragen of te voorkomen door een eiwit uit te schakelen dat met name gevaarlijke, stamcelachtige tumorcellen aandrijft?
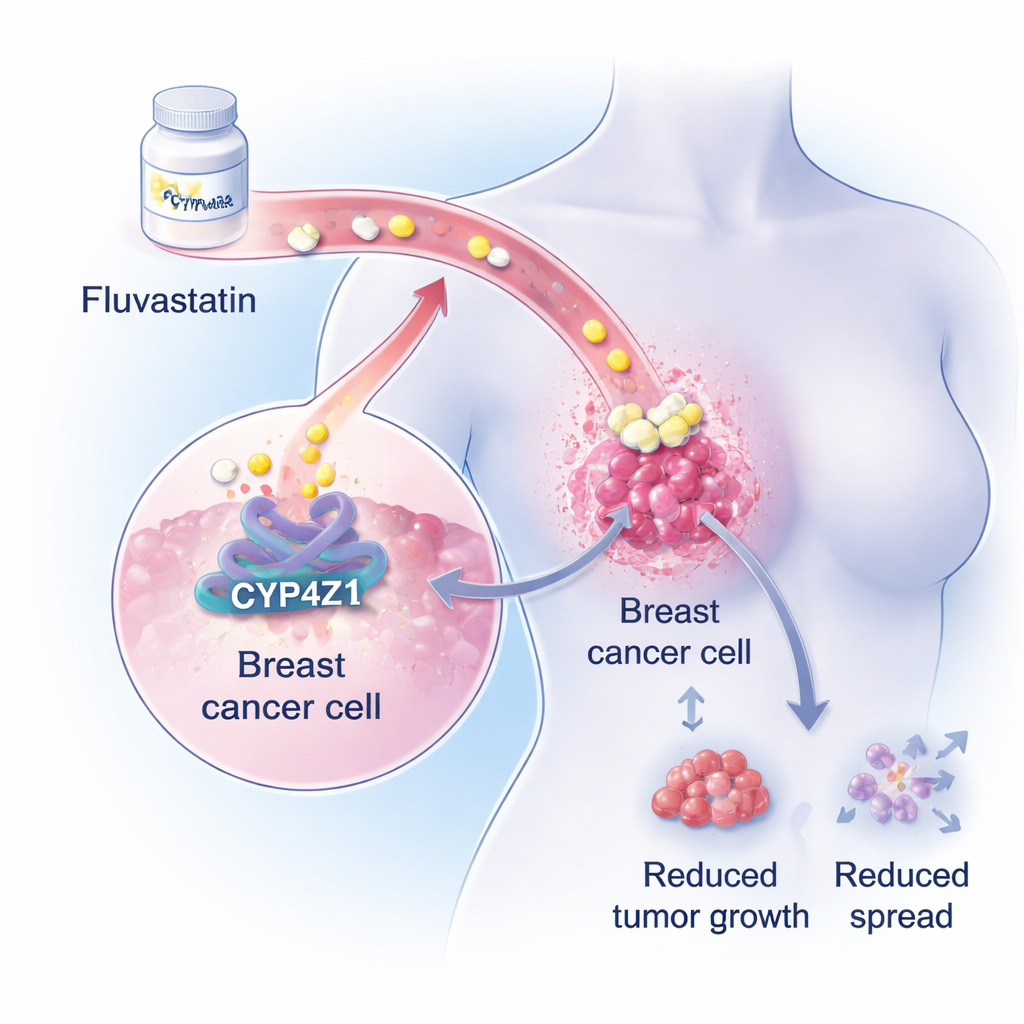
Een verborgen drijfveer in borsttumoren
De onderzoekers richten zich op een weinig bekend eiwit genaamd CYP4Z1, dat in hoge concentraties voorkomt in borstkankercellen maar niet in gezond borstweefsel. Eerder werk toonde aan dat CYP4Z1 kankercellen meer stamcelachtige eigenschappen geeft — cellen die zich onbeperkt zelf kunnen vernieuwen, weerstand bieden tegen chemotherapie en tumoren opnieuw kunnen opstarten na behandeling. In uitgebreide genetische en biochemische analyses laat het team nu zien dat overactief CYP4Z1 sterk de vetopbouwroutes in borstkankercellen stimuleert, met name de productie van triglyceriden, een belangrijk opslagvet. Omdat veel borstkankerpatiënten tijdens chemotherapie al verstoorde bloedvetten ontwikkelen, suggereert deze vetbevorderende rol van CYP4Z1 een aanknopingspunt voor bestaande lipidenverlagende middelen.
Fluvastatine herbestemmen van hart- naar kankerzorg
Om dit idee te testen onderzochten de wetenschappers een kleine bibliotheek van 23 door de FDA goedgekeurde middelen die gebruikt worden om bloedlipiden te verlagen. Fluvastatine, een veel voorgeschreven statinepil voor een hoog cholesterol, kwam naar voren als opvallende kandidaat: het blokkeerde de enzymactiviteit van CYP4Z1 rechtstreeks op een dosisafhankelijke manier. Bij doseringen die veel minder schadelijk waren voor normale borstcellen dan voor kankercellen, verminderde fluvastatine scherp belangrijke stamcelmarkers, het vermogen van borstkankercellen om vrij zwevende "tumorsferen" te vormen, en hun capaciteit om te migreren en weefselachtige barrières binnen te dringen in laboratoriumtests. Het maakte tumoren ook gevoeliger voor het chemotherapeuticum adriamycine, wat suggereert dat het bestaande behandelingen kan versterken.
Het middel testen in levende dieren
Het team evalueerde daarna fluvastatine in muismodellen. Bij muizen die waren geïmplanteerd met humane borstkankercellen, remde periodieke behandeling met fluvastatine de tumorgroei, verlaagde het de niveaus van een stamcelmarker (ALDH1A1) en de delingsmarker Ki67 in tumoren, en verminderde het aantal metastatische knobbeltjes in de longen. Belangrijk is dat muizen die fluvastatine kregen hun lichaamsgewicht behielden en geen grote bloed- of beenmergafwijkingen toonden, wat een gunstig veiligheidsprofiel bij de geteste dosis ondersteunt. In een realistischer genetisch model — muizen die zo zijn geconstrueerd dat ze borstkanker ontwikkelen door een kankerverwekkend gen — brachten de onderzoekers bovendien menselijke CYP4Z1 in het borstweefsel in. Deze muizen ontwikkelden meer precancereuze en cancereuze laesies, en meer lever- en longmetastasen dan controledieren. Behandeling met fluvastatine verminderde zowel het aantal mammaire laesies als verre metastasen aanzienlijk, vooral bij muizen die het extra CYP4Z1-gen droegen.
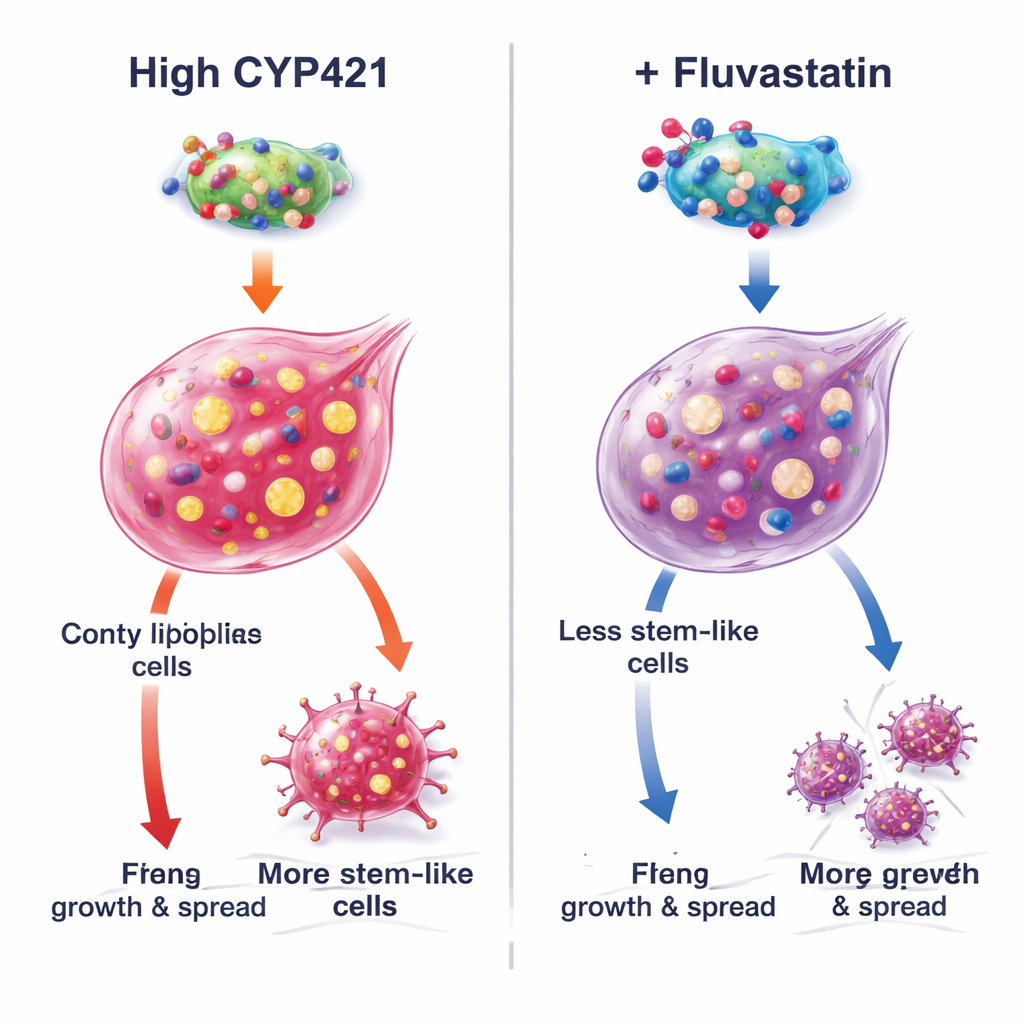
Hoe fluvastatine een kankervermijdend eiwit uitschakelt
Om het mechanisme te begrijpen combineerden de auteurs computermodellering met nauwkeurige eiwitmanipulatie. Ze voorspelden dat fluvastatine zich in de actieve plaats van CYP4Z1 klampt aan drie kritieke aminozuren (Lys109, Pro444 en Arg450). Toen die plaatsen werden gemuteerd, daalde de activiteit van CYP4Z1 en kon fluvastatine het enzym niet verder remmen, wat deze posities als bindingspunten bevestigt. In cellen die van nature geen CYP4Z1 bevatten, verhoogde het toevoegen van het normale eiwit de stamceligheid en activeerde het groeibevorderende PI3K/AKT-signaal, terwijl fluvastatine deze effecten omkeerde. Mutante versies van CYP4Z1 waren minder potent en minder reageerbaar op het middel. Aanvullende experimenten toonden dat de impact van fluvastatine verzwakte wanneer de triglycerideproductie kunstmatig werd verhoogd, of wanneer CYP4Z1 werd gereduceerd, wat benadrukt dat de sterkste effecten van het middel voortkomen uit het blokkeren van dit specifieke eiwit en diens vetopbouwende gevolgen in plaats van het opwekken van celdood via ijzergeïnduceerde "ferroptose."
Wat dit betekent voor patiënten
Over het geheel genomen suggereert de studie dat fluvastatine, naast het verlagen van cholesterol, in experimentele modellen zowel de vroegste stadia als de latere verspreiding van borstkanker kan remmen door CYP4Z1 te richten, een eiwit dat vetmetabolisme en stamcelachtig gedrag in tumoren stuurt. Omdat fluvastatine al is goedgekeurd en het veiligheidsprofiel goed bekend is, bieden deze bevindingen een veelbelovende route naar snellere klinische tests als aanvullende therapie, met name bij patiënten van wie de tumoren hoge CYP4Z1-expressie vertonen. Hoewel meer werk nodig is om deze benadering bij mensen te testen en om eventuele aanvullende doelen van het middel te identificeren, opent het onderzoek de deur naar het gebruik van een bekend hartmiddel als onderdeel van een nieuwe strategie tegen agressieve, terugvalgevoelige borstkankers.
Bronvermelding: Li, H., Chen, Y., Shi, W. et al. Fluvastatin suppresses breast cancer initiation and progression via targeting CYP4Z1. Commun Biol 9, 254 (2026). https://doi.org/10.1038/s42003-026-09532-y
Trefwoorden: borstkanker, fluvastatine, kankerstamcellen, lipidenmetabolisme, hergebruik van geneesmiddelen