Clear Sky Science · nl
Gerichte blokkering van gen-splicing kan primaire microRNA's in introns ontregelen
Verborgen boodschappen in onze genen
Veel nieuwe gentherapieën werken door de RNA‑boodschappen van onze cellen bij te sturen, maar die RNA's verbergen vaak extra “aantekeningen in de marge” die wetenschappers nog maar net beginnen te doorgronden. Dit artikel laat zien dat medicijnen die zijn ontworpen om foutieve splicing van genen te corrigeren per ongeluk kleine regulerende RNA's begraven in introns — de niet‑coderende stukken tussen gensegmenten — kunnen opkrikken, met verrassende effecten op de aanleg van hersenbanen en ontwikkeling.
Gentherapieën die RNA herschrijven
Antisense-oligonucleotiden, of ASO's, zijn korte synthetische stukjes genetisch materiaal die aan RNA kleven en veranderen hoe het wordt afgelezen of verwerkt. Meerdere ASO's worden al getest of gebruikt voor zeldzame genetische aandoeningen, vooral die veroorzaakt door fouten in RNA‑splicing — de stap die coderende segmenten van een gen aan elkaar naait. De meeste veiligheidstests richten zich op de vraag of een ASO het juiste eiwit herstelt en duidelijke bijwerkingen vermijdt. Maar veel genen dragen ook niet‑coderende RNA's, waaronder microRNA's, in hun introns. Deze kleine moleculen kunnen de genactiviteit sterk bijstellen, en tot de helft van de bekende microRNA's bij gewervelden komt uit introns. De nieuwe studie stelt de vraag: wat gebeurt er met deze ingebedde microRNA's wanneer we met ASO's veranderingen in splicing afdwingen?
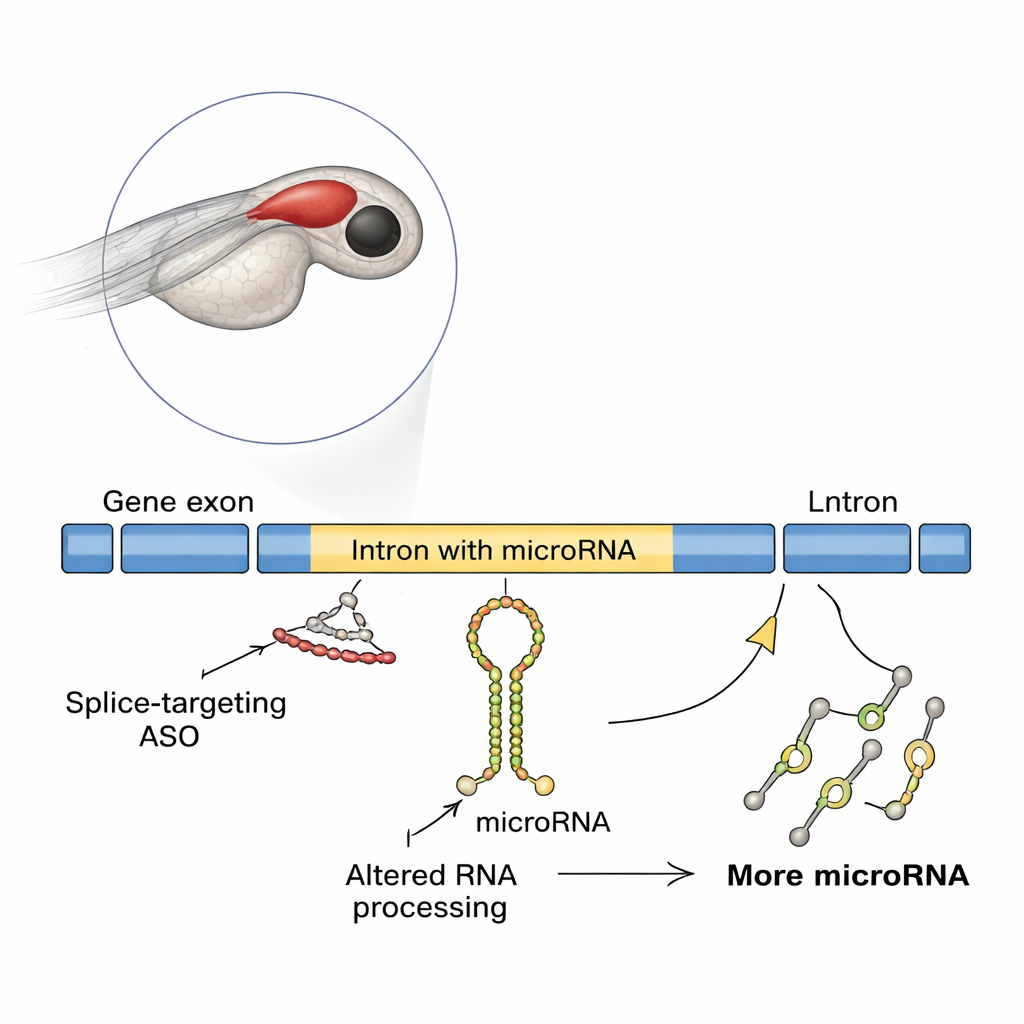
Een verrassend effect in zich ontwikkelende vissenhersenen
De onderzoekers gebruikten zebravissen, een populair gewerveld model waarvan de transparante embryo's de ontwikkeling van de hersenen makkelijk te volgen maken. Ze concentreerden zich op een gen dat slit3 heet, dat helpt zenuwvezels te begeleiden en een microRNA bevat genaamd mir-218a-1 in een van zijn introns. Toen het team het begin van de slit3-translatie blokkeerde, leek de ontwikkeling van hormoon‑afgevende hypofyseaxonen normaal. Maar wanneer ze een andere ASO gebruikten die splicing op een specifiek slit3-splice‑site blokkeerde, waren de axonen die naar de achterste hypofyse moesten projecteren sterk verminderd, hoewel het aantal oxytocine‑producerende neuronen hetzelfde bleef. Moleculaire testen toonden aan dat deze splice‑blokkerende ASO intronretentie in het gen‑RNA veroorzaakte, en onverwacht de niveaus van het slit3-transcript, zijn lange intron en het in het intron ingebedde primaire mir-218a-1-transcript verhoogde.
MicroRNA, niet eiwitverlies, veroorzaakt de afwijkingen
Om te ontrafelen wat het axonale probleem veroorzaakte, vergeleken de auteurs verschillende scenario's. Het alleen blokkeren van rijp mir-218a-1 veranderde de slit3-niveaus niet, en een aparte ASO gericht op een andere splice‑site nabij het microRNA veroorzaakte geen axonale defecten of toename van mir-218a-1. Cruciaal was dat wanneer de splice‑blokkerende slit3-ASO werd gecombineerd met een ASO die mir-218a-1 neutraliseerde, de axonale bedrading grotendeels herstelde. Eveneens veroorzaakte diezelfde splice‑blokkerende ASO geen axonale defecten meer in zebravissen die genetisch het mir-218a-1 misten, terwijl injectie van een synthetische mir-218a-mimic het fenotype in normale vissen kon nabootsen. Deze experimenten wijzen op verhoogde intronale microRNA's — in plaats van een verkort Slit3‑eiwit — als de belangrijkste oorzaak van de ontwikkelingsstoornis.
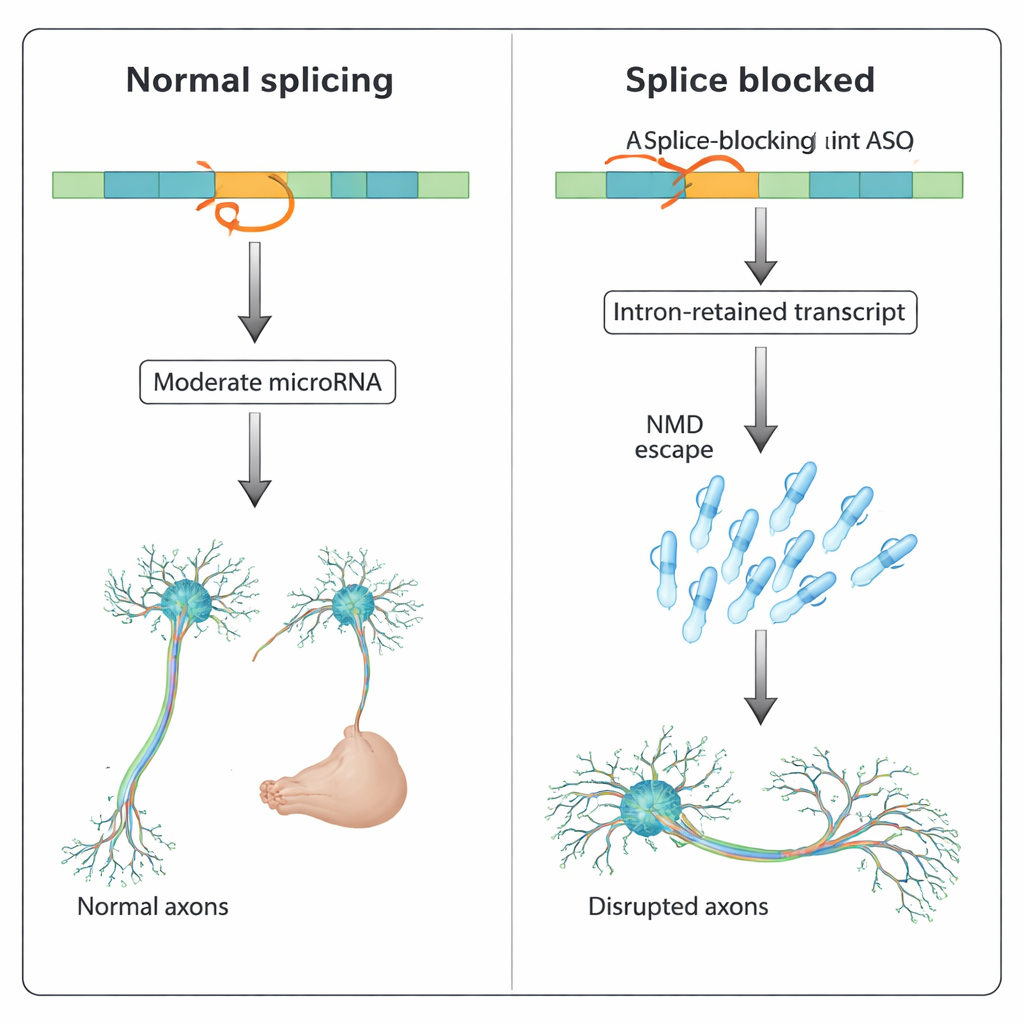
Een breder patroon bij meerdere genen
Het team vroeg zich vervolgens af of dit effect uniek is voor slit3. Ze doorzochten het zebravisgenoom en vonden tientallen eiwitcoderende genen die intronale microRNA's herbergen, veel betrokken bij ontwikkeling en signaaloverdracht. Twee van die genen, pank2 en dnm2a, lieten eerder ernstige ontwikkelingsproblemen zien wanneer hun splicing door ASO's werd geblokkeerd, waaronder hersenvochtophoping, hartzwelling en lichaamsmisvormingen — problemen die genetische knockouts van dezelfde genen niet reproduceerden. In deze studie redde co‑injectie van ASO's die specifiek de intronale microRNA's mir-103 (in pank2) of mir-199-5p (in dnm2a) blokkeerden deze door ASO's geïnduceerde fenotypes deels. In sommige gevallen herstelde de microRNA‑blokkade ook de expressie van het gastgen, terwijl dat in andere gevallen niet gebeurde, wat suggereert dat verhoogde microRNA‑activiteit schadelijk kan zijn, zelfs wanneer de totale niveaus slechts modest veranderen.
Wat dit betekent voor toekomstige behandelingen
De bevindingen tonen aan dat op splicing gerichte ASO's meer kunnen doen dan exons laten overslaan of introns laten retineren: ze kunnen intron‑behouden transcripties stabiliseren die het kwaliteitscontrolesysteem van de cel ontlopen en intronale primaire microRNA's versterken, die vervolgens netwerken van doelsgenen verkeerd reguleren. In zich ontwikkelende neuronen kan zulke ongecontroleerde microRNA‑activiteit de axongroei en connectiviteit vervormen. Voor geneesmiddelenontwikkelaars betekent dit dat ongewone of “off‑target” fenotypes bij dierproeven niet altijd voortkomen uit generieke toxiciteitsroutes zoals p53‑activatie, maar uit onbedoelde effecten op verborgen intronale RNA's. Zorgvuldig vergelijken van translatie‑blokkerende en splice‑blokkerende ASO's en het monitoren van intronale microRNA‑expressie kan helpen deze risico's vroegtijdig te signaleren en ASO‑ontwerpen te verfijnen voordat ze patiënten bereiken.
Bronvermelding: Ali, M.H., Ramesh, A.R., Nedunchezhian, N. et al. Targeted blocking of gene splicing can dysregulate intron-embedded primary microRNAs. Commun Biol 9, 252 (2026). https://doi.org/10.1038/s42003-026-09529-7
Trefwoorden: antisense-oligonucleotiden, microRNA, RNA-splicing, zebravisontwikkeling, veiligheid van gentherapie