Clear Sky Science · nl
Epigenoom-brede associatiestudie van circulerende interleukine-6 legt verband tussen DNA-methylering en immunometabole en ontstekingsgerelateerde gezondheid
Waarom dit belangrijk is voor alledaagse gezondheid
Chronische, laaggradige ontsteking beïnvloedt stilletjes ons risico op ziekten zoals type 2-diabetes, hartziekten en inflammatoire darmziekten. Een belangrijke speler in dit proces is een signaalproteïne in het bloed dat interleukine‑6 (IL‑6) wordt genoemd. Deze studie stelt een fundamentele vraag: hoe interacteert IL‑6 met ons epigenoom — de chemische tags op DNA die helpen genactiviteit te regelen — en wat betekent dat voor onze gezondheid op lange termijn?
Kijken naar chemische markers op DNA
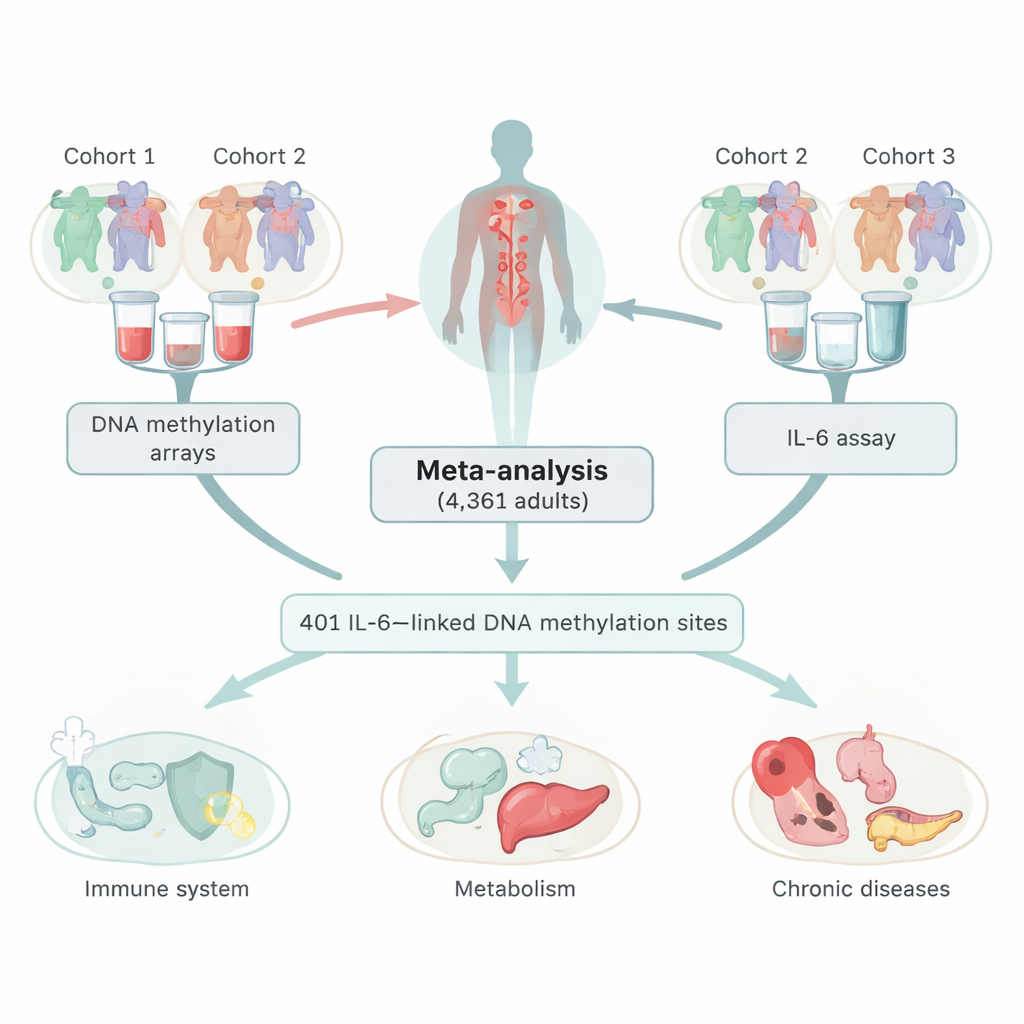
De onderzoekers combineerden gegevens uit drie grote Europese cohorts, in totaal 4.361 volwassenen die bloedmonsters afgaven. In deze monsters bepaalden ze zowel IL‑6-niveaus als DNA-methylering, een veelvoorkomend chemisch merkteken op DNA dat genen omhoog of omlaag kan schakelen zonder de genetische code zelf te veranderen. Door meer dan 400.000 locaties in het genoom te scannen, identificeerden ze 401 plekken waar methyleringsniveaus samenhingen met de hoeveelheid circulerend IL‑6. De meeste van deze locaties lieten een inverse relatie zien: hogere IL‑6 ging gepaard met lagere methylering op die plekken. Het team controleerde zorgvuldig dat deze verbanden niet eenvoudigweg bijproducten waren van roken, verschillen in bloedceltypen of een andere ontstekingsmarker, C‑reactief proteïne (CRP).
Ontsteking koppelen aan metabolisme en ziekte
Vervolgens onderzochten de auteurs of deze IL‑6‑gekoppelde DNA-locaties overlapten met signalen die in andere grote epigenetische studies waren gevonden. Ze zagen sterke verrijking voor kenmerken met een ontstekings- of metabole component, waaronder body‑mass index, bloedlipiden, bloeddruk, bloedsuiker, type 2‑diabetes, chronische nierziekte en psychiatrische en stressgerelateerde aandoeningen. Veel van dezelfde methyleringsplaatsen waren eerder al aan CRP gekoppeld, maar de patronen suggereerden dat IL‑6 en CRP elk deels verschillende epigenetische handtekeningen dragen. Met andere woorden: de chemische markeringen geassocieerd met IL‑6 zijn niet simpelweg een kopie van die bij CRP en kunnen aanvullende informatie geven over iemands ontstekings- en metabolische toestand.
Waar in het genoom de activiteit plaatsvindt
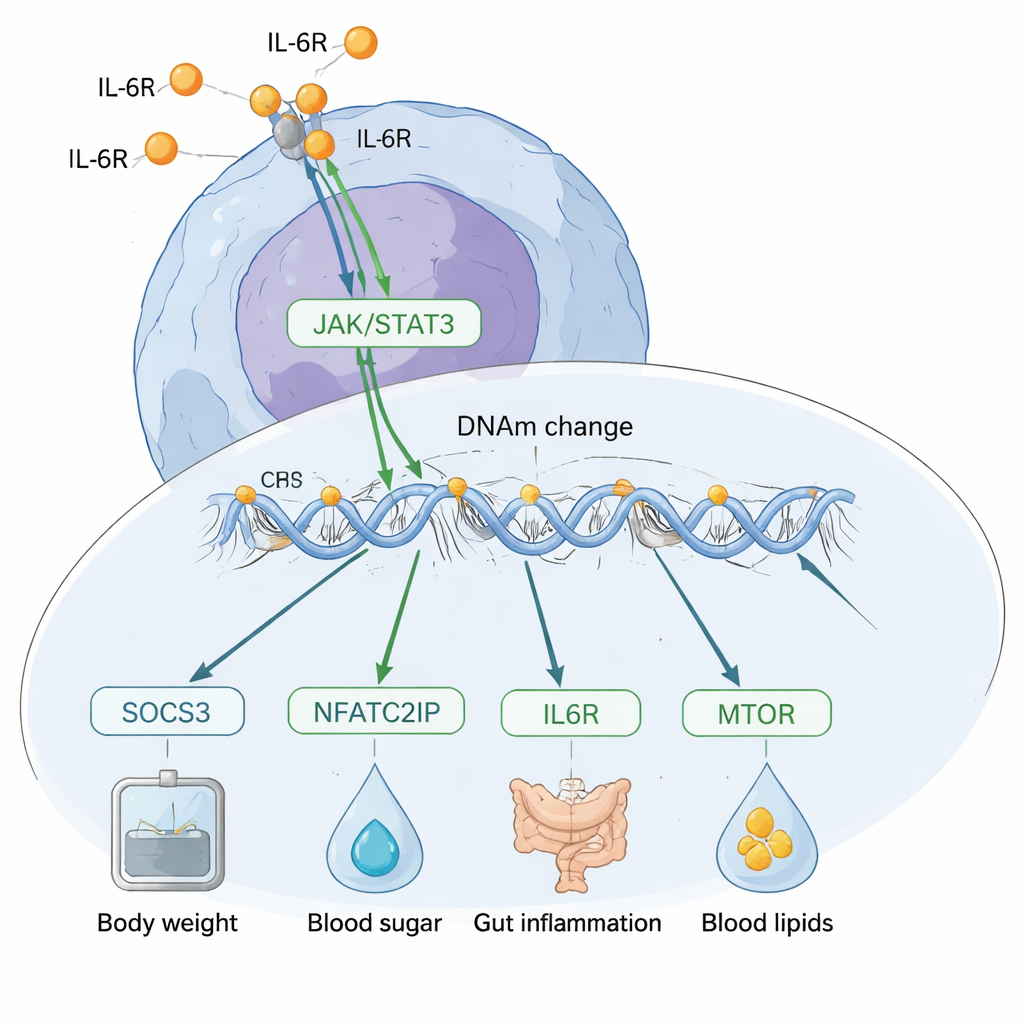
Om te begrijpen wat deze methyleringsplaatsen mogelijk doen, plaatste het team ze op bekende regulatorische gebieden van het genoom. Ze vonden dat IL‑6‑geassocieerde locaties geconcentreerd waren in actieve controle-elementen zoals enhancers — DNA‑stukken die helpen genen aan te zetten — in plaats van in inactieve regio’s. Deze plekken lagen ook dicht bij bindingssequenties voor transcriptiefactoren die IL‑6 en stressreacties direct reguleren, waaronder NF‑κB, Atf4, CHOP en Nrf2. Door methyleringsgegevens te combineren met grote genexpressiedatasets, koppelden de onderzoekers meer dan 400 genen aan de IL‑6‑gerelateerde locaties. Veel van deze genen staan centraal in immuun- en metabole regulatie, waaronder SOCS3, IL6R, AIM2, IFI16, MTOR en RORC, en zijn betrokken bij pathways die activatie en energiegebruik aansturen in een gespecialiseerde T‑celtype (Th17‑cellen) dat wordt geïmpliceerd in chronische ontstekingsziekten.
In welke richting loopt oorzaak en gevolg?
Een grote uitdaging is uit te vinden of DNA‑methylering veranderingen in IL‑6 veroorzaakt, of dat IL‑6 de methylering hervormt. Het team gebruikte verschillende genetische benaderingen om deze richting te onderzoeken. Over het genoom steunden hun “triangulatie”-analyses een model waarin IL‑6 meestal veranderingen in DNA‑methylering aanstuurt, in plaats van andersom. Daarna zoomden ze in op specifieke locaties en vonden dat methyleringsveranderingen nabij het SOCS3‑gen lijken te bemiddelen in de invloed van IL‑6 op risicofactoren zoals lichaamsgewicht, cholesterol, CRP‑niveaus en inflammatoire darmziekte. Daarentegen toonde één opvallende plek nabij een genregulator genaamd NFATC2IP tekenen dat deze de IL‑6‑productie zelf beïnvloedt en ook verschillende aandoeningen kan beïnvloeden, waaronder body‑mass index, type 2‑diabetes en darmontsteking.
Wat dit betekent voor toekomstige preventie en behandeling
Voor een niet‑specialistische lezer is de kernboodschap dat IL‑6 en epigenetische DNA‑merken nauw met elkaar verweven zijn op manieren die veel voorkomende ziekten raken. Meestal lijkt IL‑6 een chemische "voetafdruk" op het genoom achter te laten, met name in immuuncellen, die pro‑ontstekingsstatussen markeert en mogelijk stabiliseert. Op enkele sleutelplaatsen kan methylering echter mede bepalen hoeveel IL‑6 wordt geproduceerd en hoe sterk immuunpaden reageren. Deze bevindingen wijzen op DNA‑methyleringspatronen als veelbelovende bloedgebaseerde indicatoren van ontstekings- en metabole gezondheid, en suggereren dat zorgvuldig gerichte epigenetische aanpassingen — vooral rond genen als SOCS3 en NFATC2IP — op termijn IL‑6‑blokkerende geneesmiddelen zouden kunnen aanvullen bij het voorkomen of behandelen van chronische aandoeningen.
Bronvermelding: Sinke, L., van Dongen, J., Delerue, T. et al. Epigenome-wide association study of circulating interleukin-6 connects DNA methylation to immunometabolic and inflammatory health. Commun Biol 9, 242 (2026). https://doi.org/10.1038/s42003-026-09520-2
Trefwoorden: interleukine-6, DNA-methylering, ontsteking, metabole ziekte, epigenetica