Clear Sky Science · nl
MAT2A versterkt PARN-transcriptie via SRF om glycolyse te versnellen en maligne progressie in osteosarcoom aan te drijven
Waarom deze studie over botkanker ertoe doet
Osteosarcoom is de meest voorkomende botkanker bij kinderen en tieners, en de behandelingen zijn al decennialang nauwelijks veranderd. Veel jonge patiënten hebben nog steeds slechte vooruitzichten, vooral wanneer de kanker uitzaait of resistent is tegen chemotherapie. Deze studie onthult een verborgen "hoofdschakelaar"-eiwit genaamd MAT2A dat osteosarcoomcellen helpt groeien, hun energiehuishouding herprogrammeren en agressieve tumoren vormen — en toont aan dat een medicijn gericht op MAT2A deze tumoren in laboratoriummodellen kan vertragen of verkleinen.
Een verborgen motor in tumorcellen
De onderzoekers begonnen met het vergelijken van botkankermonsters met normaal botweefsel op enkelcelniveau. Ze vonden dat osteosarcoomweefsel meer tumoropbouwende cellen en minder immuuncellen bevat, en dat één gen in het bijzonder — MAT2A — abnormaal actief was in kankercellen. Analyse van openbare kanker-databases en in het laboratorium gekweekte cellijnen bevestigde dat MAT2A-niveaus veel hoger waren in osteosarcoom dan in gezonde botcellen, en dat patiënten met hogere MAT2A-waarden vaker een gevorderd ziektebeeld en lymfeklieruitzaaiingen hadden. Dit plaatste MAT2A centraal als een potentiële aandrijver van de ziekte in plaats van een passieve toeschouwer.
MAT2A verminderen remt kankergroei
Om te testen hoe belangrijk MAT2A echt is voor het tumorgedrag, gebruikte het team genetische hulpmiddelen om MAT2A-niveaus in osteosarcoomcelijnen te verlagen. Wanneer MAT2A werd uitgeschakeld, deelden kankercellen zich langzamer en waren ze vatbaarder voor geprogrammeerde celdood. In muizen waarin deze gemodificeerde cellen waren geïmplanteerd, groeiden tumoren veel langzamer en bleken ze uiteindelijk significant kleiner, terwijl het lichaamsgewicht van de dieren stabiel bleef. Deze experimenten lieten zien dat osteosarcoomcellen sterk afhankelijk zijn van MAT2A voor zowel overleving als hun vermogen tumorvorming te ondersteunen.
Een signaalrelay die het brandstofgebruik verhoogt
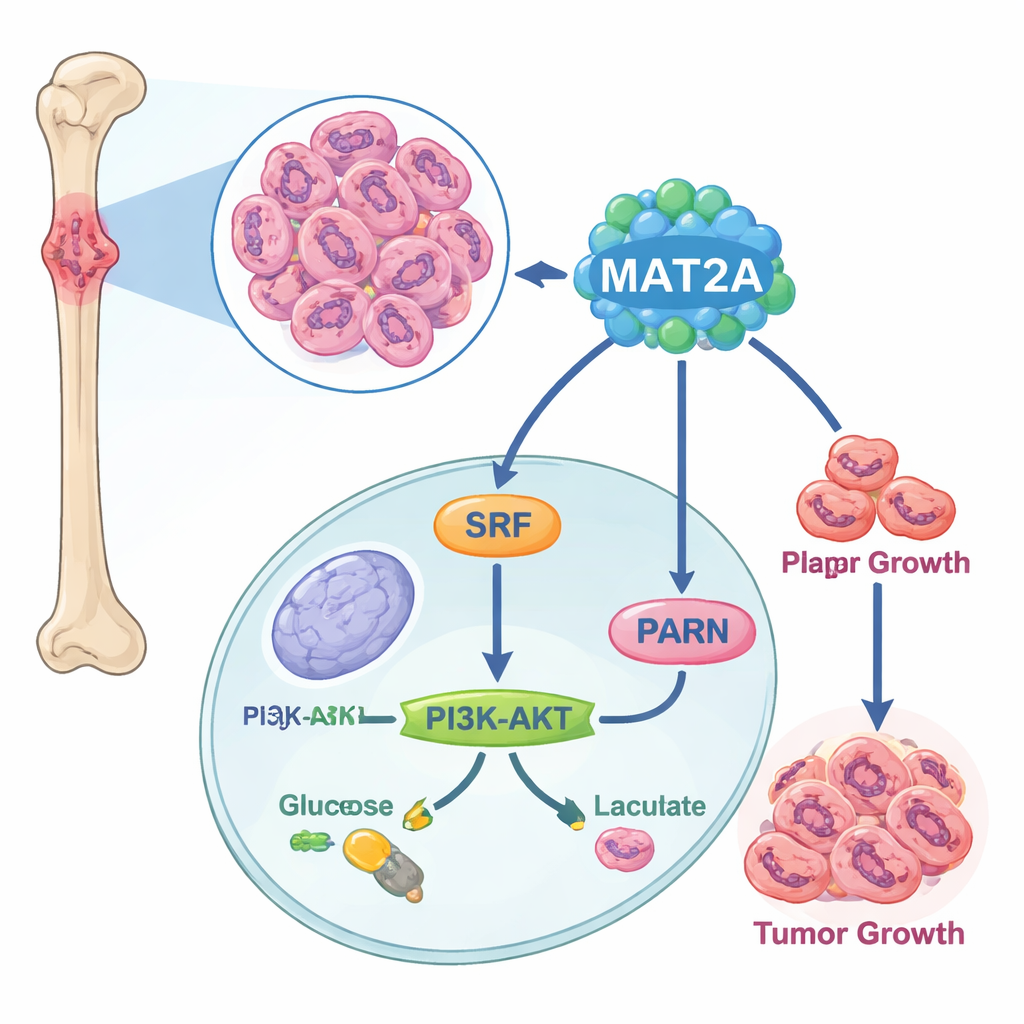
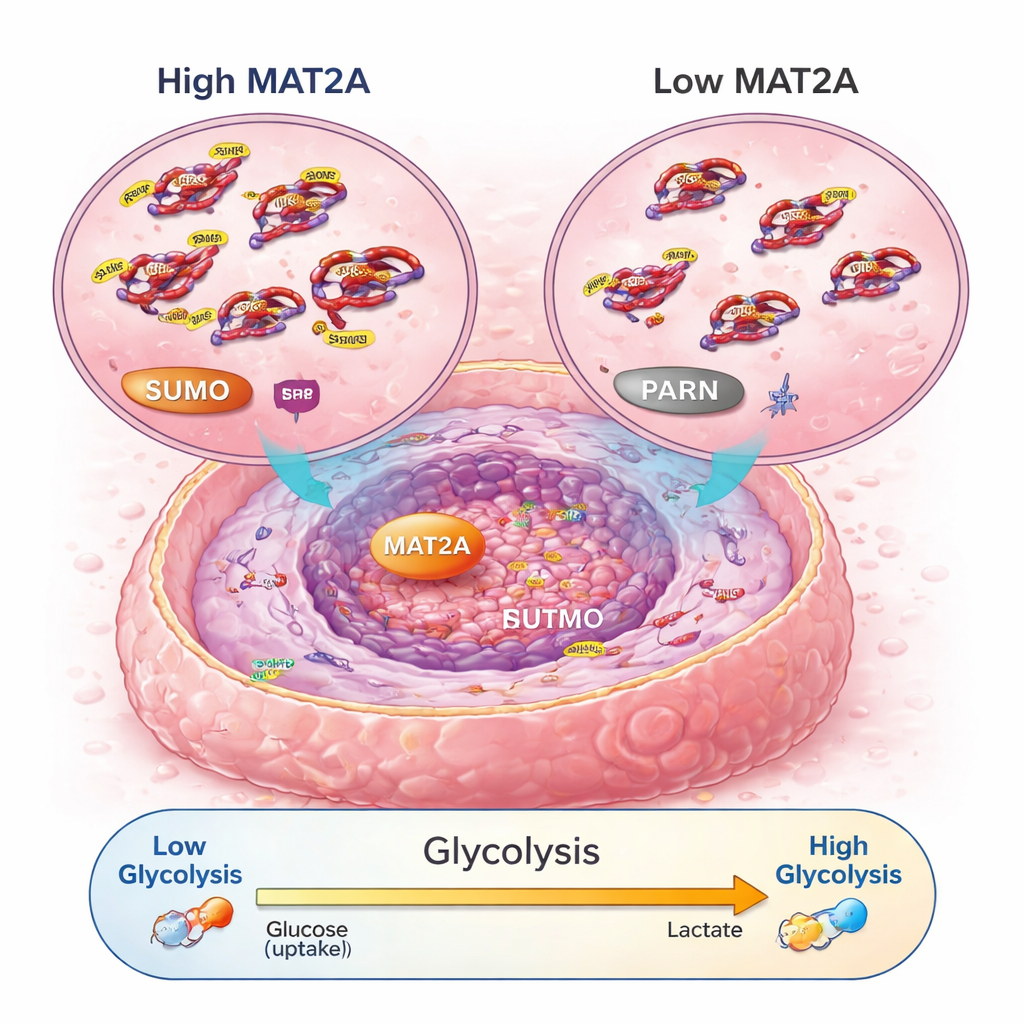
Dieper gravend ontdekten de wetenschappers dat MAT2A meer doet dan zijn gebruikelijke metabole taak. In de kern bindt het aan een transcriptiefactor genaamd SRF, en helpt het SRF stabiel en actief te houden door de bevordering van een chemische markering bekend als SUMO. Op zijn beurt schakelt SRF een gen aan genaamd PARN, dat vervolgens de bekende PI3K–AKT-route activeert en het mechanisme van aerobe glycolyse opendraait — een snelle maar inefficiënte manier waarop cellen energie produceren die kankercellen prefereren. Wanneer MAT2A werd gereduceerd, produceerden kankercellen minder ATP (hun energievaluta), namen ze minder glucose op, maakten ze minder melkzuur en schakelden ze terug naar rustiger, zuurstofafhankelijk ademhalen. Het verstoren van PARN of AKT kon de pro-groeien pro-glycolyse effecten van MAT2A terugdraaien, wat bevestigt dat deze relay — MAT2A naar SRF naar PARN naar PI3K–AKT — fungeert als een sleutelcircuit voor energie en groei in osteosarcoom.
Een niet-traditionele rol en een geneesmiddelbaar doelwit
Opvallend is dat een variant van MAT2A die zijn normale enzymatische activiteit miste nog steeds SRF-stabiliteit en PARN-activatie ondersteunde, wat betekent dat deze kankepromoterende rol niet afhankelijk is van zijn gebruikelijke chemische reactie. In plaats daarvan werkt MAT2A meer als een scaffold die andere eiwitten organiseert. Dit heeft praktische implicaties: geneesmiddelen hoeven niet per se het katalytische centrum te blokkeren om tumoren te verzwakken. De onderzoekers testten een klein-moleculair remmer genaamd FIDAS-5, ontworpen om MAT2A te raken, zowel in celkweek als in muismodellen. Behandeling verminderde nucleair SRF, verlaagde PARN- en PI3K–AKT-signaalgeving, dempte glycolyse, vertraagde celdeling en induceerde kankerceldood. In muizen krompen of vertraagden tumoren onder FIDAS-5 zonder merkbaar gewichtsverlies, wat wijst op aanvaardbare bijwerkingen in deze setting.
Wat dit betekent voor patiënten en toekomstige therapieën
Voor niet-specialisten is de kernboodschap dat osteosarcoomcellen afhankelijk zijn van MAT2A om hun groeiprogramma's en suikerverbrandingsmotoren op volle toeren te laten draaien. Door sleutelcontrole-eiwitten te stabiliseren en een keten van signalen te versterken, helpt MAT2A tumoren sneller te groeien en agressiever te worden. Het blokkeren van dit eiwit — hetzij via genetische methoden of met een medicijn zoals FIDAS-5 — snijdt die ondersteuning af, waardoor kankercellen vertragen, minder frenetiek energie verbruiken en uiteindelijk afsterven. Hoewel nog veel werk nodig is voordat zulke behandelingen de kliniek bereiken, positioneert deze studie MAT2A als een veelbelovend nieuw doelwit in de strijd tegen botkanker en opent het een potentiële route naar preciezere en minder toxische therapieën voor jonge patiënten.
Bronvermelding: Ren, Z., Chen, H., Qiao, Q. et al. MAT2A enhances PARN transcription via SRF to accelerate glycolysis and drive malignant progression in osteosarcoma. Commun Biol 9, 241 (2026). https://doi.org/10.1038/s42003-026-09518-w
Trefwoorden: osteosarcoom, MAT2A, kankermetabolisme, PI3K AKT-route, gerichte therapie