Clear Sky Science · nl
Strategische vorderingen voor cryo-EM-structuurstudies van kleine (<100 kDa) GPCR's
Waarom kleine schakelaars in cellen belangrijk zijn voor de geneeskunde
Veel moderne geneeskunde werkt door het subtiel beïnvloeden van kleine schakelaars in onze celmembranen, die G-eiwit‑gekoppelde receptoren (GPCR's) worden genoemd. Deze schakelaars registreren hormonen, geuren en geneesmiddelen, en ongeveer een derde van alle goedgekeurde medicijnen werkt via deze receptoren. Om veiligere, slimmere medicijnen te ontwerpen, hebben wetenschappers gedetailleerde 3D-beelden van deze receptoren nodig, vooral in hun "uit"- of inactieve vormen, waarop veel geneesmiddelen specifiek gericht zijn. Dit artikel legt uit hoe onderzoekers sommige van de kleinste GPCR's zichtbaar proberen te maken met cryo‑elektronenmicroscopie (cryo‑EM), een krachtige beeldvormingstechniek die moleculen in een bijna natuurlijke, ingevroren toestand kan bekijken.
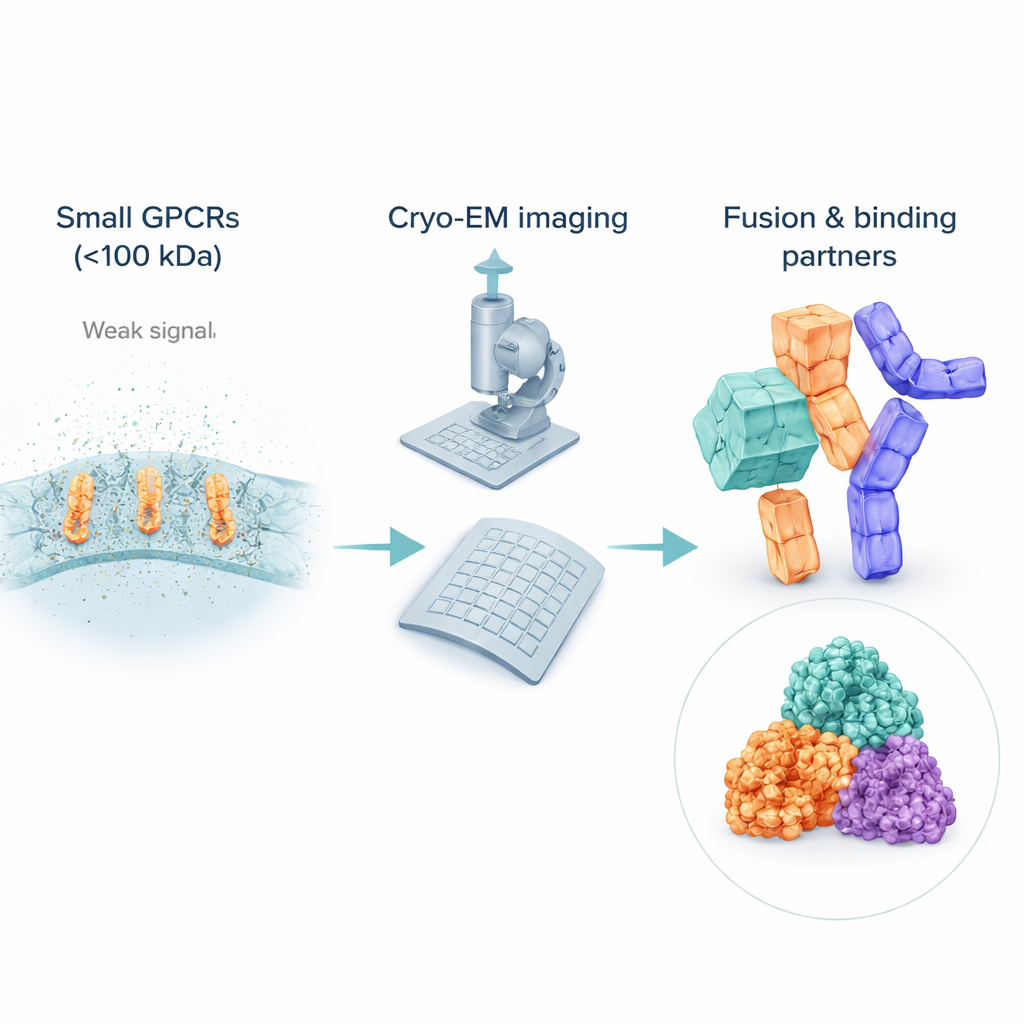
De uitdaging om zeer kleine receptoren te zien
Hoewel cryo‑EM de structurele biologie heeft getransformeerd, heeft deze techniek nog steeds moeite met kleine, flexibele moleculen. Veel inactieve GPCR's wegen ver onder 100 kilodalton, waardoor ze moeilijk te detecteren en uit te lijnen zijn in ruisachtige beelden. Om ze oplosbaar te houden, wikkelen wetenschappers deze receptoren in detergentbellen of lipide-imitaties, die voor de elektronenbundel zelfs "groter" kunnen lijken dan het receptor-eiwit zelf en daarmee het signaal van het doelwit kunnen overstemmen. In tegenstelling tot actieve receptoren die gebonden zijn aan omvangrijke partners zoals G-eiwitten, missen inactieve GPCR's vaak opvallende externe kenmerken, waardoor computers het lastig vinden om veel beelden te middelen tot een scherp 3D‑beeld. Daardoor komen de meeste structuren van inactieve GPCR's nog steeds uit oudere röntgenmethoden, en blijft er een leemte in cryo‑EM-dekking precies daar waar veel medicijnen werken.
Receptoren opvouwen met ingebouwde helpers
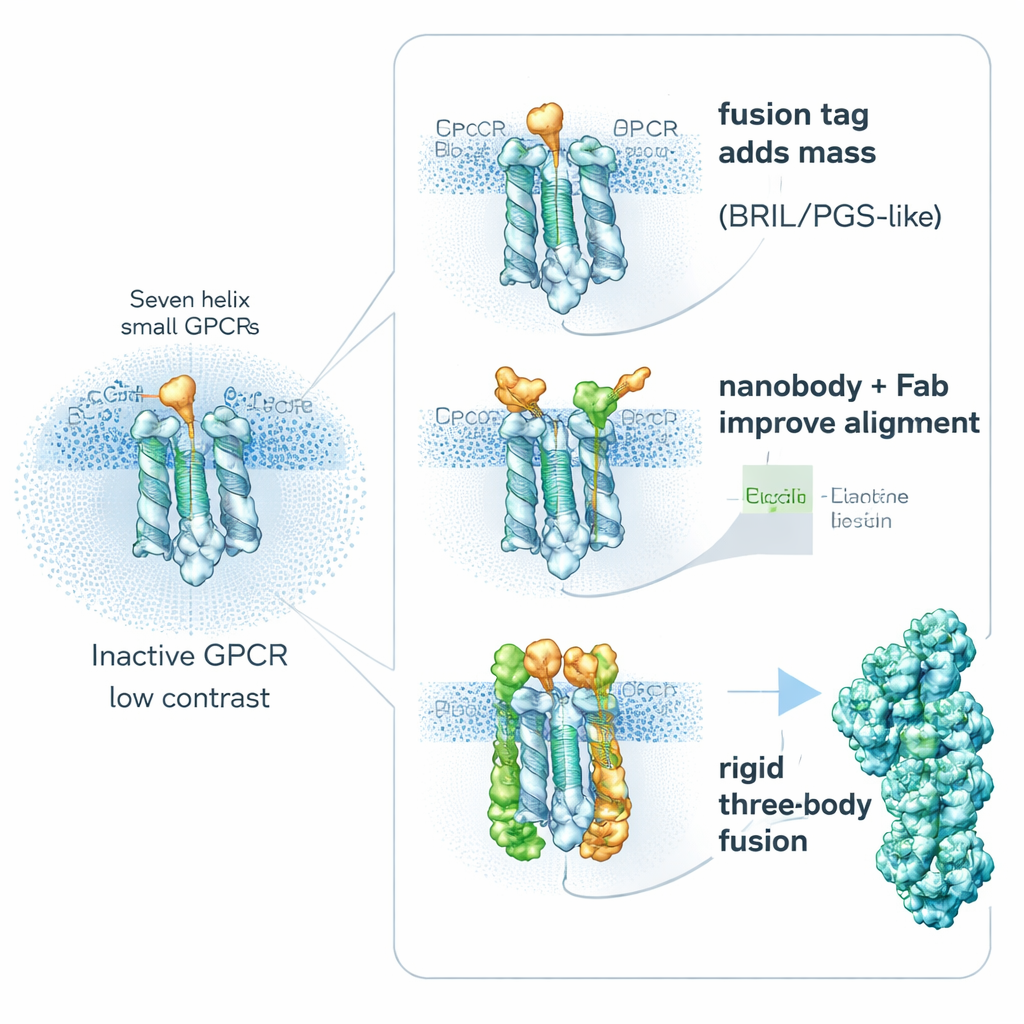
Een belangrijke strategie is verrassend eenvoudig: maak de receptor opzettelijk "zwaarder". Onderzoekers fuseren genetisch kleine, stabiele helper-eiwitten aan flexibele delen van GPCR's om hun grootte en stijfheid te vergroten, zonder de belangrijke geneesmiddelbindingsplaatsen te blokkeren. Populaire helpers zijn BRIL (een vierhelixbundel), PGS (een thermostabiel enzymfragment) en een grotere klemachtige eiwitpartner zoals calcineurine. Deze fusiepartners worden vaak ingevoegd in een beweeglijke binnenlus die twee helices verbindt. Door dit gebied te verstevigen verminderen ze de vervaging door moleculaire beweging en leveren ze herkenbare vormen die computers helpen de deeltjes uit te lijnen. Studies tonen aan dat de exacte positie en oriëntatie van het fusiedeel een project kan maken of breken: bij één receptor verbeterde een anders gepositioneerde PGS-tag de resolutie van een vage 6 angstrom naar een veel duidelijkere 3,7 angstrom.
Antilichamen en ontworpen binders lenen als handvatten
Een tweede route vermijdt het inbouwen van grote fusies in de receptor en bevestigt in plaats daarvan hoge-affiniteits "handvatten" van buitenaf. Kleine antilichaamfragmenten, nanobodies en verwante binders kunnen worden opgewekt om inactieve GPCR's te herkennen en zich vast te klampen aan flexibele binnenlussen. Een opvallend voorbeeld is Nanobody‑6, dat aanvankelijk werd gemaakt als sensor voor één opioïdreceptor en daarna, met bescheiden aanpassingen, opnieuw werd gebruikt om meerdere andere GPCR's in hun inactieve vormen te stabiliseren. Omdat het off-center bindt, geeft het elk deeltje een duidelijke oriënteringscue, wat het middelen van beelden betrouwbaarder maakt. Onderzoekers breiden dit idee vaak uit door een tweede laag toe te voegen—een gewoon antilichaamfragment dat het nanobody zelf herkent—waardoor een grotere, stijvere complex ontstaat dat scherp zichtbaar is in cryo‑EM. Andere ontworpen binders, zoals DARPins, kunnen worden gebruikt als modulaire afstandhouders of als verbindingsstukken naar grotere proteïnekooien, wat het signaal van zeer kleine doelen verder versterkt.
Slimmere monsterontwerpen en AI-ondersteunde beeldverwerking
Het samenvoegen van helpers of het toevoegen van binders is maar een deel van het verhaal. De review benadrukt dat goede structuren beginnen met zorgvuldig ontworpen receptorconstructen: het wegknippen van slappe staarten, het introduceren van stabiliserende mutaties en het gebruik van moderne structuurvoorspellingsgereedschappen om delen te identificeren die problemen kunnen veroorzaken. Aan de beeldvormingszijde worden oudere trucs zoals faseplaten, die contrast verhogen voor zwakke deeltjes, aangevuld of zelfs vervangen door kunstmatige-intelligentiehulpmiddelen. Deep-learningprogramma's kunnen piepkleine deeltjes in ruisachtige micrografen opvangen, en nieuwe algoritmen kunnen beelden in verschillende vormen sorteren wanneer receptoren meerdere conformaties aannemen. Samen met fiduciaire helpers duwen deze ontwikkelingen cryo‑EM naar het betrouwbaar oplossen van membraaneiwitten die ooit te klein of te dynamisch werden geacht om te bestuderen.
Wat dit betekent voor toekomstige geneesmiddelen
Het artikel besluit dat er geen enkel "magisch" hulpmiddel is dat voor alle receptoren werkt, maar dat een steeds grotere gereedschapskist van fusiepartners, antilichaamachtige binders en AI-gestuurde methoden gestaag het inactieve landschap van GPCR's voor cryo‑EM opent. Voor niet-experts is de belangrijkste conclusie dat door kleine receptoren groter en ordelijker te laten lijken voor het microscoopbeeld, wetenschappers eindelijk gedetailleerde momentopnamen kunnen verkrijgen van de exacte vormen waaraan veel geneesmiddelen de voorkeur geven om te binden. Deze structurele blauwdrukken zouden het ontwerp van medicijnen moeten versnellen die deze cellulaire schakelaars nauwkeuriger uit kunnen schakelen—of hun activiteit fijn kunnen afstemmen—met minder bijwerkingen.
Bronvermelding: Singh, S.K., Agrawal, M., Pattanayak, A. et al. Strategic advances for cryo-EM structural studies of small (<100 kDa) GPCRs. Commun Biol 9, 237 (2026). https://doi.org/10.1038/s42003-026-09516-y
Trefwoorden: G-eiwit-gekoppelde receptoren, kryo-elektronenmicroscopie, geneesmiddelenontwikkeling, structurele biologie, nanobody-steigers