Clear Sky Science · nl
Het koppelen van moleculaire spanning en cellulaire trekkrachten: een multiscale benadering van de mechanica van focale adhesies
Hoe cellen hun omgeving voelen en eraan trekken
Elke keer dat een cel beweegt, deelt of een weefsel van vorm verandert, trekt zij stilletjes aan haar omgeving. Deze kleine mechanische trekkrachten zijn cruciaal bij wondheling, de verspreiding van kanker en de ontwikkeling van organen, maar ze zijn moeilijk zichtbaar en nog moeilijker te meten. Deze studie presenteert een nieuwe manier om die krachten vanuit twee invalshoeken tegelijk te bekijken: hoe hard een hele cel aan een zacht materiaal trekt, en hoeveel kracht individuele “moleculaire veren” binnen de verankeringsplaatsen van de cel dragen. Door deze perspectieven te koppelen, helpt het werk te verklaren hoe cellen stijfheid waarnemen en hun grip op de omgeving reguleren.
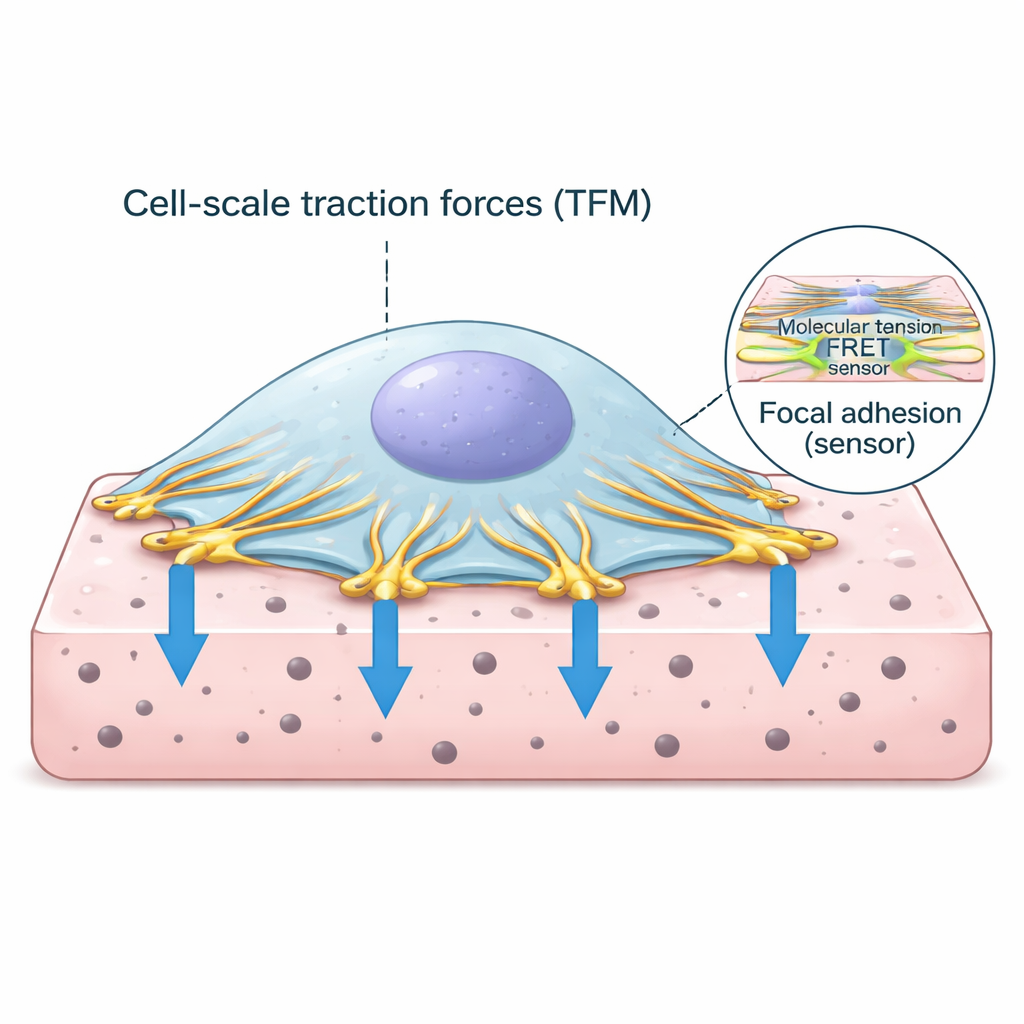
De grijppunten van de cel op de buitenwereld
Cellen zweven niet zomaar in weefsels; ze verankeren zich via gespecialiseerde contactpunten die focale adhesies worden genoemd. Op deze plekken verbindt het interne skelet van actinevezels zich met eiwitten die het celmembraan overspannen en zich vastklampen aan de omliggende matrix. Een van de sleutelproteïnen in dit verankeringscomplex is vinculine, dat zich gedraagt als een krachtsensitieve schakel. Wanneer het contractiele apparaat van de cel aan actine trekt, voelt vinculine de belasting en helpt het de verbinding te versterken. Begrijpen hoeveel kracht door deze schakels gaat, en hoe dat zich verhoudt tot het algehele trekken van de cel, is essentieel om te ontrafelen hoe weefsels gezond blijven of ziek worden.
Twee vensters op cellulaire kracht
De onderzoekers combineerden twee krachtige technieken in één workflow. Ten eerste meet tractiekrachtmicroscopie hoeveel een cel een zacht, gelachtig substraat vervormt door de beweging van kleine fluorescerende deeltjes in de gel te volgen. Vanuit deze deeltjesbewegingen kan men de verdeling van duw- en trekkrachten onder de cel berekenen. Ten tweede draagt een speciaal ontworpen vinculine-eiwit een fluorescent spanningssensor die zijn lichtsignaal verandert als hij wordt uitgerekt. Met geavanceerde life‑time imaging zette het team dit lichtsignaal om in een uitlezing van moleculaire spanning op vinculine. Ze ontwierpen dunne, platte hydrogelsubstraten die op hoge resolutie te beeldvormen waren en schreven aangepaste software om beide datasets tot op individuele adhesieplaatsen uit te lijnen, te segmenteren en te analyseren.
Hoe stijfheid de inzet van de cel verandert
Wanneer cellen werden gekweekt op zachte versus stijvere gels, veranderde hun gedrag op een duidelijke manier. Op stijvere substraten verspreidden cellen zich meer en oefenden ze sterkere trekkrachten uit op het gelaagde oppervlak. Tegelijkertijd toonde de fluorescerende uitlezing van de vinculine-sensor een hogere moleculaire spanning binnen focale adhesies. Interessant genoeg veranderden de basale structurele kenmerken van deze adhesies — zoals hun aantal of gemiddelde grootte — niet veel tussen zachte en stijve gels. In plaats daarvan veranderde de manier waarop krachten waren georganiseerd. Grote, radiaal georiënteerde adhesies met meer vinculine droegen vaker hogere trekkrachten, wat suggereert dat zowel de geometrie als de moleculaire samenstelling van deze plekken bepalen hoe hard de cel trekt.
Een complexe relatie tussen lokale en moleculaire krachten
Nadere blik op individuele adhesies toonde dat de relatie tussen lokale trekkracht en vinculine-spanning niet universeel is. In sommige cellen vertoonden adhesies die hogere trekkrachten genereerden ook hogere vinculine-spanning, wat impliceert dat ingeschakelde, lastdragende contacten krachten directer via hun moleculaire schakels delen. In andere cellen verscheen het tegenovergestelde patroon: regio's met sterke trekkracht waren geassocieerd met lagere vinculine-spanning, terwijl andere adhesies meer moleculaire last droegen zonder grote uitwendige trekken te veroorzaken. Veel cellen vertoonden helemaal geen duidelijk patroon. Deze verschillende gedragingen weerspiegelen waarschijnlijk verschillende celtoestanden — zoals actief verspreiden, stabiele adhesie of retractie — en suggereren dat cellen krachten op meerdere manieren over hun adhesienetwerk kunnen herverdelen.
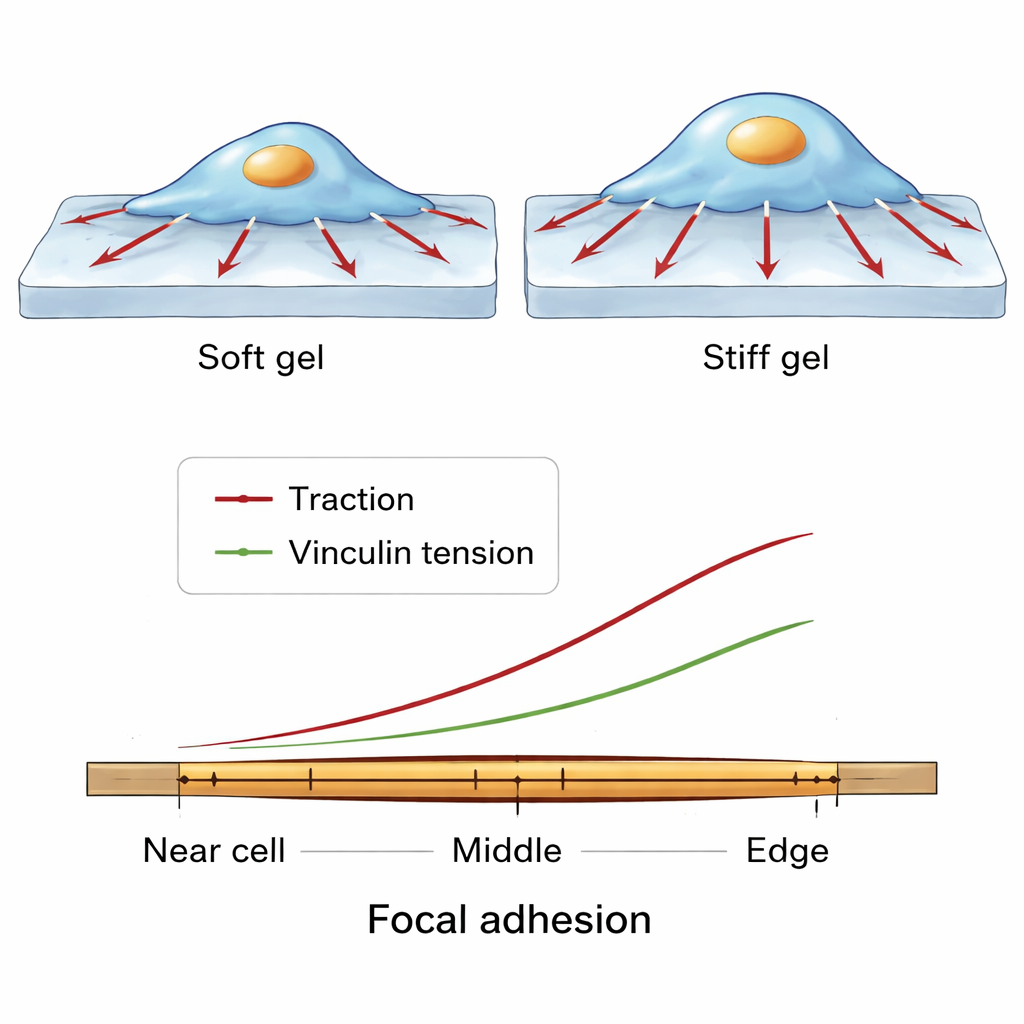
Fijnmazige krachtpatronen langs een enkele grijppunt
Het team zoomde vervolgens nog dichter in en onderzocht hoe krachten veranderen langs de lengte van een enkele focale adhesie, van de zijde dichter bij het celcentrum tot de rand nabij de celperiferie. Over veel cellen en condities kwam een consistent patroon naar voren. Vinculinemoleculen waren het dichtst opeengepakt richting het midden van de adhesie. Toch namen zowel de op het substraat uitgeoefende trekkracht als de moleculaire spanning op vinculine toe richting het buitenste, meer perifere uiteinde. Dit suggereert een evenwichtsoefening: in centrale regio's kunnen veel vinculinemoleculen de last delen, zodat elk molecuul minder spanning voelt, terwijl aan de buitenrand minder moleculen relatief meer kracht dragen en zo sterke lokale trekken ondersteunen terwijl de adhesie intact blijft.
Wat dit betekent voor gezondheid en ziekte
Door hele-cel trekkrachtkaarten te combineren met eiwitniveau-spanningsmetingen biedt deze studie een multiscale beeld van hoe cellen hun mechanische grip beheren. Het werk laat zien dat naarmate de omgeving stijver wordt, cellen zowel harder trekken als hun vinculine‑schakels meer belasten, maar dat de gedetailleerde relatie tussen uitwendige krachten en moleculaire spanning per adhesie en per cel varieert. Tegelijkertijd lijkt een robuust ruimtelijk patroon van krachtsverdeling binnen individuele adhesies behouden te blijven. Voor een niet‑specialist is de kernboodschap dat cellen zowel nauwkeurig afstemmen waar als hoe ze trekken, en krachten over vele kleine moleculaire “veren” herverdelen om zich aan verschillende mechanische omgevingen aan te passen — een principe dat ten grondslag kan liggen aan processen variërend van weefselontwikkeling tot fibrose en kankerinvasie.
Bronvermelding: Aytekin, S., Kimps, L., Coucke, Q. et al. Linking molecular tension and cellular tractions: a multiscale approach to focal adhesion mechanics. Commun Biol 9, 236 (2026). https://doi.org/10.1038/s42003-026-09514-0
Trefwoorden: celmechanica, focale adhesies, vinculine, tractiekrachtmicroscopie, mechanotransductie