Clear Sky Science · nl
Temporale dynamiek van collaterale RNA-splitsing door LbuCas13a in menselijke cellen
Een bacteriële verdediging omgevormd tot een precieze celdoder
Onderzoekers hebben een manier ontdekt om een bacterieel immuuneiwit te veranderen in een zeer selectieve "zelfvernietigings"-schakelaar voor menselijke cellen. Door een CRISPR-enzym genaamd LbuCas13a te benutten, kunnen ze een gekozen RNA-bericht in een cel herkennen en vervolgens vrijwel al het andere RNA van die cel versnipperen. Voor niet-specialisten is dit intrigerend omdat RNA-berichten bepalen welke eiwitten een cel aanmaakt; leren om ze op commando uit te wissen opent deuren naar nieuwe kankerbehandelingen, antivirale strategieën en krachtige onderzoeksgereedschappen.
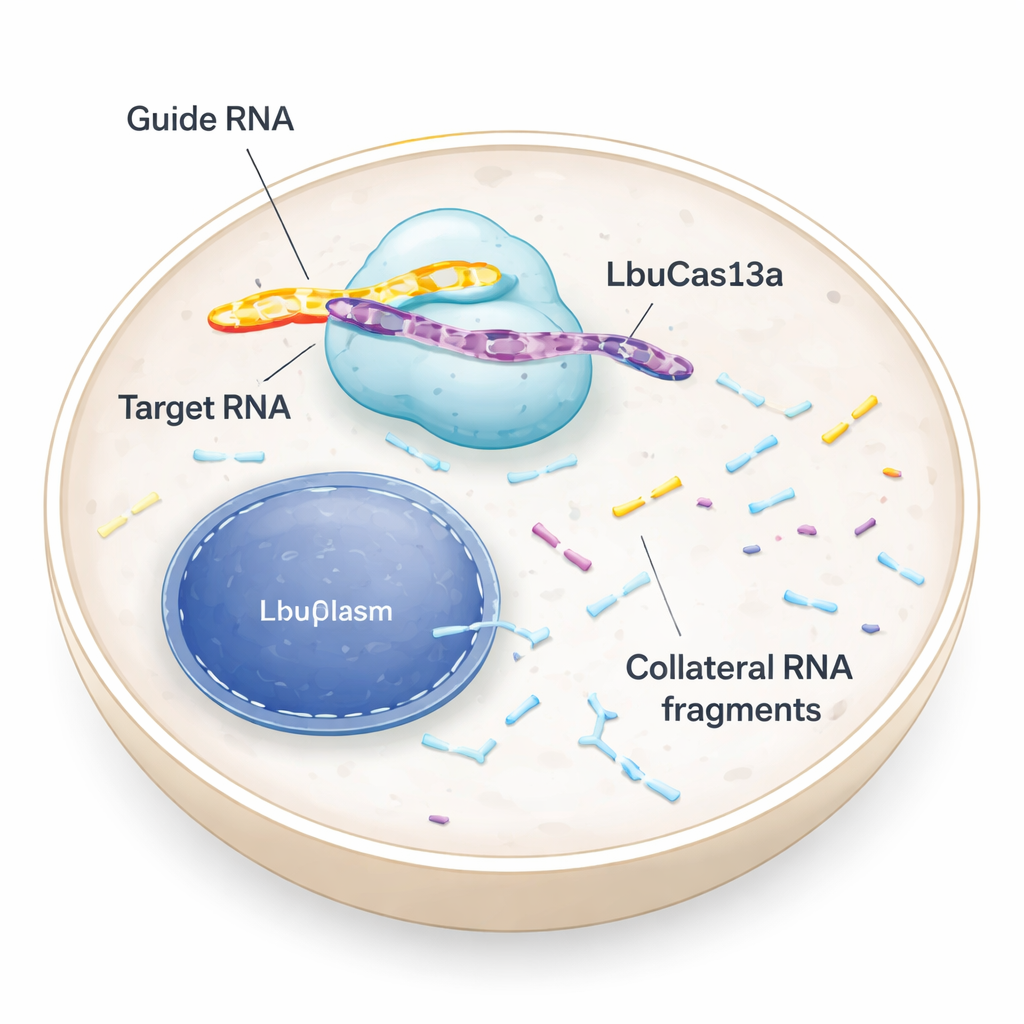
Een moleculaire schaar die RNA, niet DNA, richt
De meeste mensen hebben gehoord van CRISPR-tools die DNA knippen en de genetische code herschrijven. LbuCas13a is anders: het herkent en knipt RNA, de tijdelijke boodschappen die instructies van het DNA naar de eiwitfabrieken van de cel brengen. In bacteriën maken Cas13-enzymen deel uit van de antivirale verdediging. Zodra ze een viraal RNA detecteren, versnipperen ze niet alleen die indringer maar beginnen ze ook veel andere nabijgelegen RNA's te knippen. Deze zogenaamde "collaterale" activiteit kan geïnfecteerde cellen in een rusttoestand of naar celdood duwen, wat helpt de bacteriële gemeenschap te beschermen. Vroege tests in dier- en menselijke cellen suggereerden dat Cas13’s collaterale knipactiviteit zwak of afwezig was, waardoor het enzym vooral werd gebruikt als een nauwkeurige RNA-"uit"-schakelaar. De nieuwe studie heroverweegt die aanname en toont aan dat, onder de juiste omstandigheden, collaterale activiteit in menselijke cellen zowel sterk als nuttig kan zijn.
Het ontketenen van collateraal knippen in menselijke cellen
Het team vergeleek verschillende Cas13-varianten en ontdekte dat LbuCas13a bijzonder krachtig was. Ze brachten gezuiverd LbuCas13a-eiwit, vooraf geladen met een kort gids-RNA, rechtstreeks in menselijke cellen aan — een vorm van moleculaire "eiwitinjectie" genaamd ribonucleoproteïne (RNP)-levering. Wanneer de gids overeenkwam met een doel-RNA—zoals een fluorescerend merkgene of overvloedige natuurlijke boodschappen zoals GAPDH en 18S ribosomaal RNA—sneed het enzym eerst dat doel en begon daarna veel andere RNA's te verscheuren. Binnen ongeveer 50 minuten veranderde het algehele RNA-profiel van de cel drastisch, met karakteristieke knipfragmenten die verschenen. Dit collaterale effect werd waargenomen bij verschillende afleveringsmethoden en in een reeks celtypen, wat aantoont dat het geen toevalligheid was van één cellijn of één kunstmatig doel.
Van RNA-versnippering naar celdood en selectie
Wat gebeurt er met een cel waarvan de RNA-berichten plotseling verdwijnen? Met live-cel beeldvorming observeerden de onderzoekers dat cellen die het doel-RNA tot expressie brachten geleidelijk in apoptose gingen, een ordelijke vorm van geprogrammeerde celdood die wordt gekenmerkt door karakteristieke "vroege waarschuwings"-signalen voordat de cel uiteenvallen. Belangrijk was dat naburige cellen die het doel-RNA niet tot expressie brachten grotendeels onaangetast bleven, wat aantoont dat de zelfvernietiging specifiek is. De groep gebruikte deze eigenschap vervolgens als een selectietool. Toen ze cellen met het doel-RNA mengden met normale cellen en LbuCas13a activeerden, werden de doel-cellen selectief uitgeput over meerdere dagen. Het herhalen van de behandeling meerdere keren duwde hun aandeel nog verder omlaag. Ze toonden aan dat dit gebruikt kon worden om succesvol gen-bewerkte cellen te verrijken en dat het ook kon worden afgesteld om kankercellen aan te pakken die een oncogen overproduceren, hier CDK4, terwijl verwante cellen die veel minder van dat RNA maken gespaard blijven.
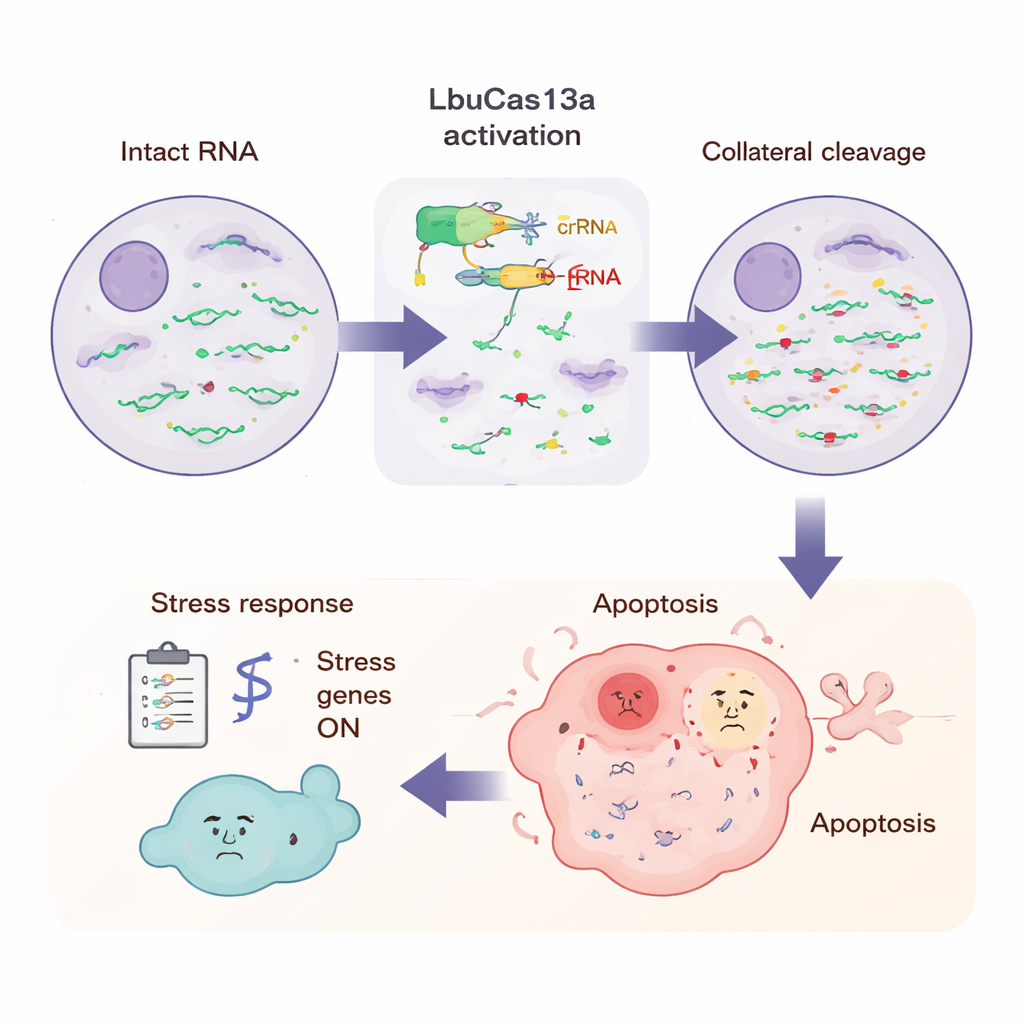
Wat de cel ervaart tijdens de aanval
Om het grotere beeld te zien, maten de wetenschappers alle RNA's in de cel op meerdere tijdstippen na activatie van LbuCas13a. Door bekende RNA-standaarden toe te voegen konden ze vaststellen dat de meeste eiwitcoderende RNA's in het cytoplasma binnen enkele uren met meer dan de helft daalden, terwijl bepaalde RNA's — zoals mitochondriale boodschappen en sommige nucleaire niet-coderende RNA's — grotendeels gespaard bleven. Lang-lees sequencing toonde aan dat er werd geknipt op herhaalde, specifieke nucleotideposities, vaak in flexibele lusregio's van RNA rijk aan de base uracil, overeenkomend met patronen gezien in proefbuisexperimenten. Op latere tijdstippen gingen veel stress- en aangeboren-immuungerelateerde genen aan, inclusief die gekoppeld aan ontstekingssignalen en antivirale verdedigingen. Dit patroon suggereert dat de cel de plotselinge vloed van gebroken RNA-einden waarneemt op een wijze die lijkt op het detecteren van een virusinfectie, en een alarmprogramma in gang zet dat culmineert in apoptose.
Waarom dit ertoe doet en waar het toe kan leiden
In eenvoudige termen toont de studie aan dat LbuCas13a kan worden omgevormd tot een RNA-geleide "doodschakelaar" voor cellen: als een cel te veel van een bepaald RNA maakt, veroorzaakt het activeren van LbuCas13a tegen dat RNA bijna-globaal RNA-verlies, een immuunachtig alarm en vervolgens gecontroleerde celdood. Omdat het proces sterk afhankelijk is van de abundanties van het doel-RNA, zou het gebruikt kunnen worden om cellen te elimineren die schadelijke genen overproduceren — zoals bepaalde kankercellen — of om ongewenste cellen in gemengde culturen tijdens onderzoek of bij de productie van celtherapieën op te ruimen. Tegelijkertijd is het werk een waarschuwing: CRISPR-tools gericht op RNA kunnen sterke bijwerkingen hebben die zorgvuldig beheerd moeten worden. Begrijpen wanneer en hoe collaterale RNA-splitsing optreedt is essentieel voor het veilig toepassen van Cas13-technologieën in de geneeskunde en biotechnologie.
Bronvermelding: Bot, J.F., Zhao, Z., Li, M. et al. Temporal dynamics of collateral RNA cleavage by LbuCas13a in human cells. Commun Biol 9, 233 (2026). https://doi.org/10.1038/s42003-026-09511-3
Trefwoorden: CRISPR-Cas13, RNA-splitsing, celdood, kankerrichting, genbewerkingstools