Clear Sky Science · nl
Structurele inzichten in metaalcluster‑trafiek binnen het nitrogenase‑assemblageskelet NifEN
Hoe de natuur een krachtig chemisch werktuig bouwt
Stikstof zit overal om ons heen in de lucht, maar de meeste levende wezens kunnen het niet in die vorm gebruiken. Een speciaal enzym, nitrogenase, lost dit probleem op door atmosferische stikstof om te zetten in ammoniak, een cruciaal bestanddeel voor leven en voor kunstmest. In het hart van nitrogenase bevindt zich een compacte metalen "cluster" die de zware chemie doet, maar hoe cellen dit ingewikkelde onderdeel assembleren was lange tijd onduidelijk. Dit artikel geeft een kijkje in dat bouwproces en onthult hoe een proteïne‑skelet genaamd NifEN functioneert als een flexibel laadplatform en transportsysteem voor het metalen vrachtstuk van de cluster.
Een moleculaire fabriek achter kunstmest en brandstoffen
Nitrogenase is de natuurlijke tegenhanger van industriële processen die ammoniak en vloeibare brandstoffen maken. In plaats van enorme reactoren gebruiken microben een compacte eiwitmachine die wordt aangedreven door cellulaire energie. De werking ervan hangt af van een uitzonderlijk complex metaalcentrum, opgebouwd uit ijzer, zwavel, molybdeen, koolstof en een organische zijgroep. Het samenstellen van deze kern is te delicaat om aan het toeval over te laten, dus cellen gebruiken een relais van helperproteïnen. Een van de belangrijkste is NifEN, dat een bijna voltooid volledig‑ijzer precursor ontvangt (de L‑cluster), helpt die om te zetten in de gerijpte vorm (de M‑cluster) en die vervolgens overdraagt aan het werkende nitrogenase‑enzym. Begrijpen hoe NifEN dit verkeer regelt kan helpen bij pogingen om microben te ontwerpen voor schonere productie van kunstmest of nieuwe koolstofgebaseerde brandstoffen.
Een bewegende machine zien met bevroren momentopnamen
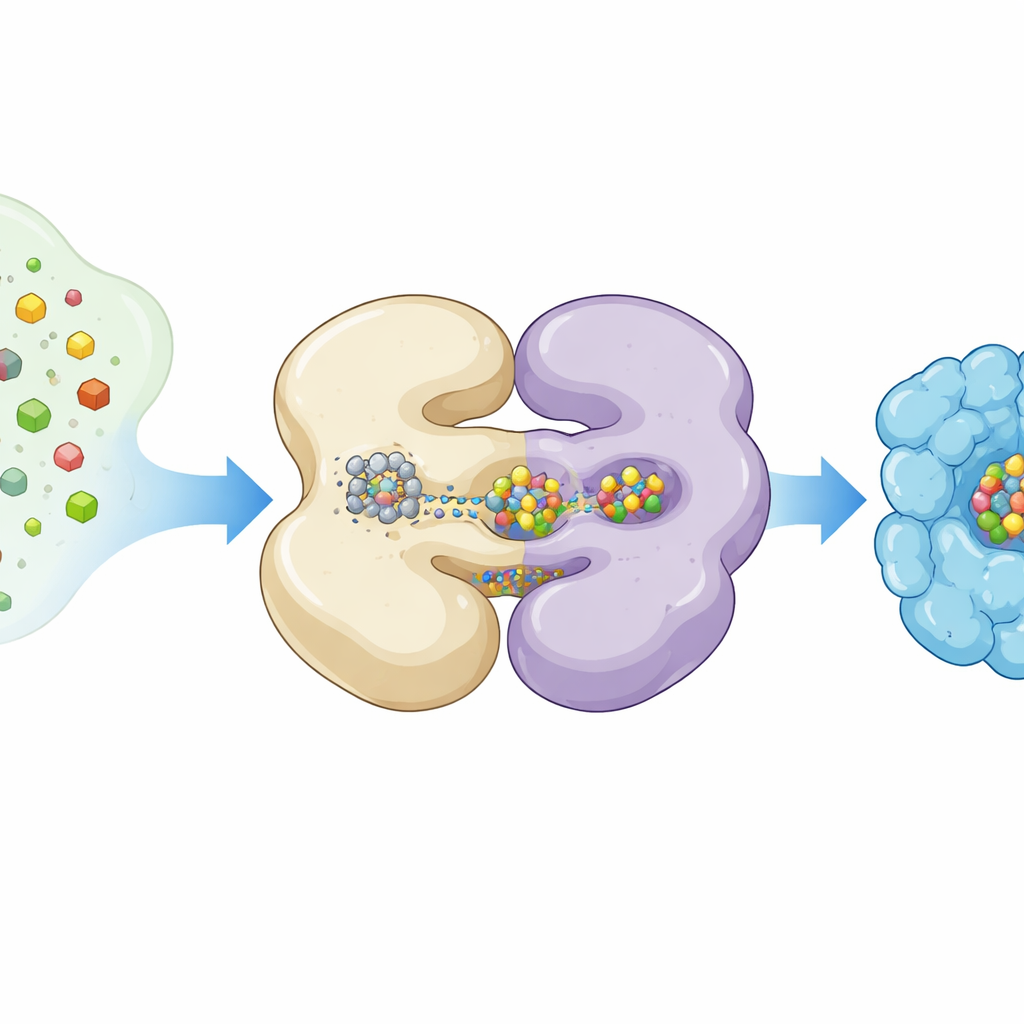
De auteurs gebruikten cryogene elektronenmicroscopie, een techniek die eiwitten afbeeldt bij extreem lage temperaturen, om NifEN in verschillende werkhoudingen vast te leggen. Ze brachten NifEN tot expressie in laboratoriumbacteriën op een manier waarbij sommige eiwitkopieën een L‑cluster droegen en andere leeg waren. Door miljoenen single‑particle beelden te sorteren reconstrueerden ze twee hoofdvormen: een "apo"‑vorm zonder de mobiele cluster en een "holo"‑vorm met de cluster gebonden op een interne plaats. Beide vormen delen een kern van vier subunits gerangschikt als twee paren, maar wanneer de L‑cluster aanwezig is, wordt de ene helft van NifEN merkbaar meer geordend en zwaaien meerdere helices naar binnen, alsof ze klemmen rond het metalen vrachtstuk.
Een verborgen tunnel voor metalen vracht
Vergelijking van de lege en beladen structuren toonde een opvallend kenmerk: een lange tunnel die door het NifEN‑dimeer loopt. In de lege toestand is deze doorgang breed en open; na binding van de cluster vernauwt hij wanneer het eiwit zijn lading vastgrijpt. Eerdere kristalstructuren hadden een alternatieve "buiten"‑positie voor de L‑cluster getoond nabij het eiwitoppervlak. Door alle waarnemingen te combineren concludeerden de onderzoekers dat de cluster ten minste twee stations op NifEN kan innemen — één begraven aan de binnenkant en één blootgesteld — en daartussen kan bewegen langs een gekromd pad dat wordt afgeschermd door verschuivingen in een flexibele domein. Deze beweging lijkt losser te zijn dan in het uiteindelijke nitrogenase‑enzym, waarvan de actieve cluster star op zijn plaats gehouden wordt, wat suggereert dat NifEN is ontworpen voor overdracht in plaats van langdurige katalyse.
Aangrijpende partners en een ononderbroken route
Om te begrijpen hoe NifEN zich verbindt met zijn upstream‑ en downstream‑partners combineerde het team hun experimentele structuren met AlphaFold 3‑computermodellen en elektronenmicroscopie met lagere resolutie van eiwitcomplexen. De modellen suggereren dat het enzym NifB, dat de L‑cluster uit kleinere ijzer‑zwaveldelen maakt, aanmeert in een dal op één vlak van NifEN. Vanaf die plek is een continue tunnel te volgen van NifB’s eigen metaalcentra direct in de NifEN‑tunnel en verder naar het interne L‑clusterstation. Aan de tegenovergestelde zijde van NifEN bevindt zich een ander aangrijpingsvlak dat NifH herbergt, het eiwit dat molybdeen en een organische zijgroep invoegt om de cofactor te voltooien. In deze configuratie zit de L‑cluster op de oppervlaktesite, ideaal gepositioneerd voor modificatie. Mutaties van sleutelaminozuren die de voorgestelde route bekleden verstoren het laden, de beweging of de rijping van de cluster, wat experimentele ondersteuning biedt voor dit lopende‑bandmodel.
Waarom een flexibel skelet ertoe doet
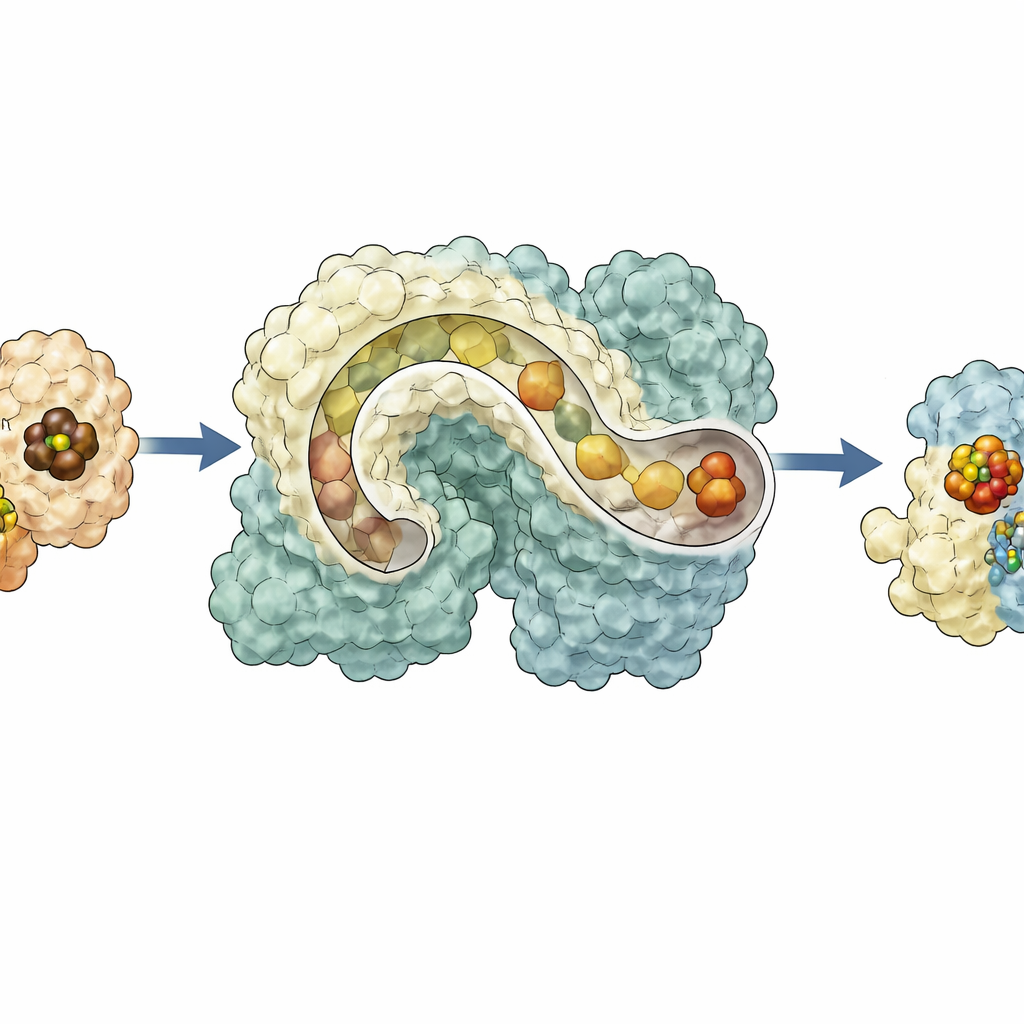
Gezamenlijk schetsen de resultaten NifEN als een dynamisch knooppunt dat aan de ene kant een metaalcore van NifB ontvangt, die vervolgens naar een interne ‘bergruimte’ wordt verplaatst, en die daarna aan de tegenovergestelde kant presenteert voor afwerking door NifH voordat de gerijpte cluster weer naar binnen wordt geleid ter overdracht aan nitrogenase. Dit conformatie‑afhankelijke verkeersschema verklaart hoe meerdere gevoelige stappen binnen een enkel eiwitkader gecoördineerd kunnen worden en geeft aanwijzingen hoe oude enzymen mogelijk geëvolueerd zijn van meer flexibele skeletten naar de hedendaagse sterk gespecialiseerde katalysatoren. Voor niet‑specialisten laat het werk zien dat zelfs op nanoschaal de natuur vertrouwt op assemblagelijnen, tunnels en bewegende onderdelen om de moleculaire gereedschappen te bouwen die de mondiale stikstofcyclus, voedselproductie en mogelijk toekomstige groene technologieën ondersteunen.
Bronvermelding: Neumann, B., Brandon, K.A., Quechol, R. et al. Structural insights into metallocluster trafficking in the nitrogenase assembly scaffold NifEN. Nat Catal 9, 281–294 (2026). https://doi.org/10.1038/s41929-026-01489-9
Trefwoorden: nitrogenase, assemblage van metaalclusters, NifEN‑skelet, kryo‑elektronenmicroscopie, biologische stikstoffixatie