Clear Sky Science · nl
Het combineren van federated learning en een reizend model verbetert prestaties en opent kansen voor digitale gezondheidsgelijkheid
Waarom het delen van medische inzichten zonder data te delen ertoe doet
De moderne geneeskunde leunt steeds vaker op kunstmatige intelligentie om patronen te vinden in scans en medische dossiers. Patiëntgegevens zijn echter gevoelig en mogen vaak de instelling waar ze verzameld zijn niet verlaten. Dit schept een spanningsveld: hoe kunnen ziekenhuizen wereldwijd samenwerken om krachtige AI-tools te trainen, zonder ruwe patiëntgegevens over grenzen of naar grote centrale servers te sturen? Deze studie introduceert een nieuwe manier om dat te doen, met als doel niet alleen nauwkeurigheid, maar ook eerlijkheid tussen rijke, goed uitgeruste ziekenhuizen en kleinere, minder bemiddelde klinieken.
Twee methoden om een AI te trainen zonder data te verplaatsen
Vandaag bestaan er twee hoofdaanpakken waarmee ziekenhuizen gezamenlijk AI kunnen trainen terwijl de gegevens lokaal blijven. Bij federated learning traint elk ziekenhuis parallel een eigen lokale kopie van een model; deze lokale modellen worden vervolgens samengevoegd tot een gedeeld "globaal" model op een centrale server. Bij een reizend model is er slechts één model dat van ziekenhuis naar ziekenhuis gaat en op elke locatie op zijn beurt wordt bijgesteld. Beide methoden beschermen de privacy, maar hebben nadelen. Federated learning kan moeite hebben wanneer sommige ziekenhuizen zeer weinig data hebben of niet alle patiëntgroepen zien; het combineren van zwakke of ongelijke lokale modellen kan leiden tot een globaal model dat vooral grote, welvarende locaties weerspiegelt. Het reizende model is robuuster tegen deze ongelijkheden, maar kan trager en lastiger te beheren zijn.
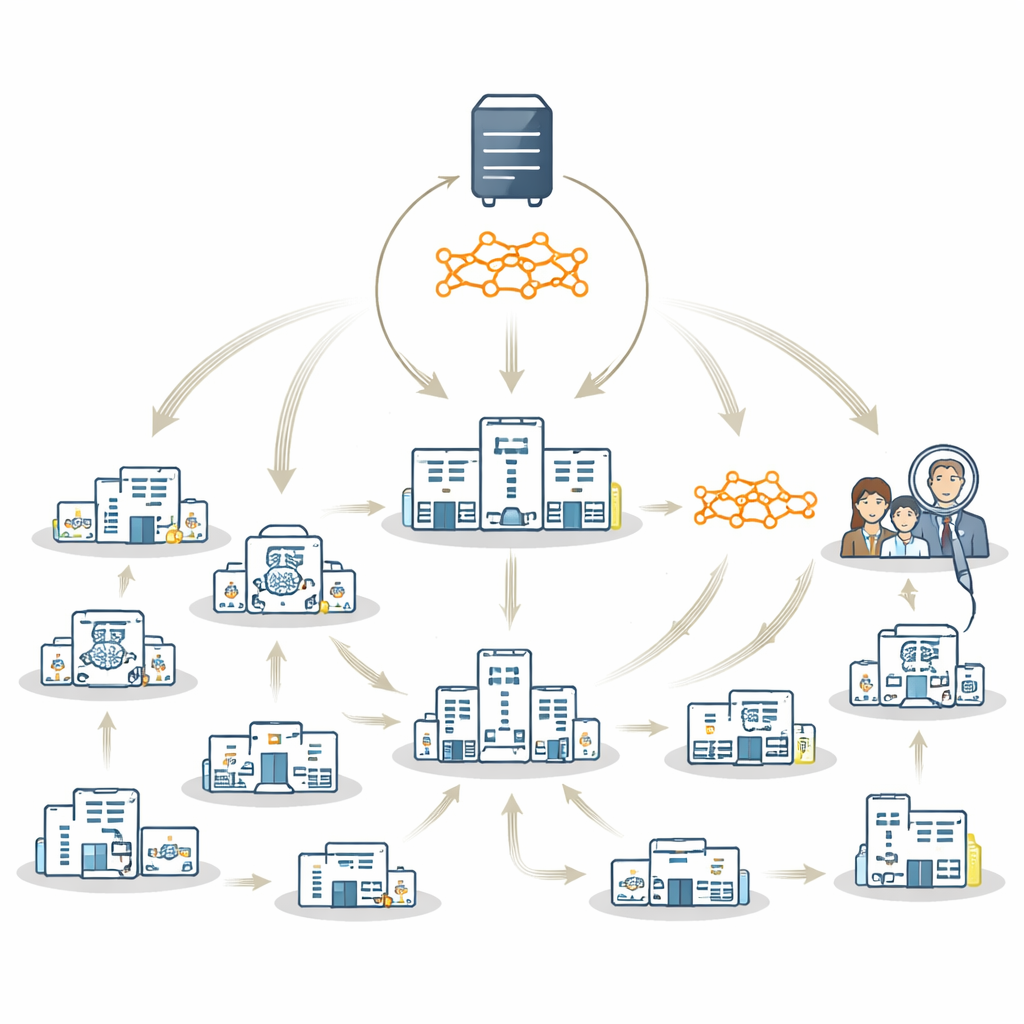
Een hybride strategie die het beste van beide werelden benut
De auteurs stellen FedTM voor, een hybride trainingsschema dat de sterke punten van federated learning en het reizende model combineert. De training verloopt in twee fasen. Eerst is er een "opwarmfase" waarin alleen de grootste ziekenhuizen, met meer volledige en evenwichtige datasets, het model parallel trainen met standaard federated learning-technieken. Dit levert een sterke beginversie van het model op. Daarna volgt een "verfijningsfase", waarin dit opgewarmde model elke locatie na elkaar bezoekt, inclusief zeer kleine klinieken die misschien maar een paar hersenscans of zelfs slechts één patiënt hebben. In deze tweede fase wordt het model geleidelijk aangepast terwijl het reist, waarbij kennis van elke locatie wordt opgenomen zonder dat de data ooit de lokale controle hoeven te verlaten.
De methode testen op hersenscans bij Parkinson
Om FedTM te testen, gebruikten de onderzoekers 1.817 MRI-hersenscans afkomstig van 83 beeldvormingslocaties wereldwijd om een AI-systeem te trainen dat mensen met de ziekte van Parkinson kan onderscheiden van gezonde personen. Dit is een bijzonder uitdagende setting: meer dan de helft van de locaties leverde minder dan tien scans, slechts ongeveer een derde had zowel patiënt- als controlegegevens, en de scanprotocollen verschilden sterk. Onder deze realistische omstandigheden slaagde puur federated learning er niet goed in de taak te leren, terwijl een puur reizend model beter presteerde maar nog ruimte voor verbetering liet. FedTM, vooral wanneer de opwarming de zeven grootste en meest evenwichtige locaties betrof, overtrof duidelijk beide methoden: de area under the ROC-curve, een gebruikelijke maat voor classificatiekwaliteit, steeg van 77% bij alleen het reizende model naar ongeveer 82% met FedTM, met vergelijkbare verbeteringen voor andere klinisch belangrijke metrics zoals sensitiviteit, specificiteit en F1-score.
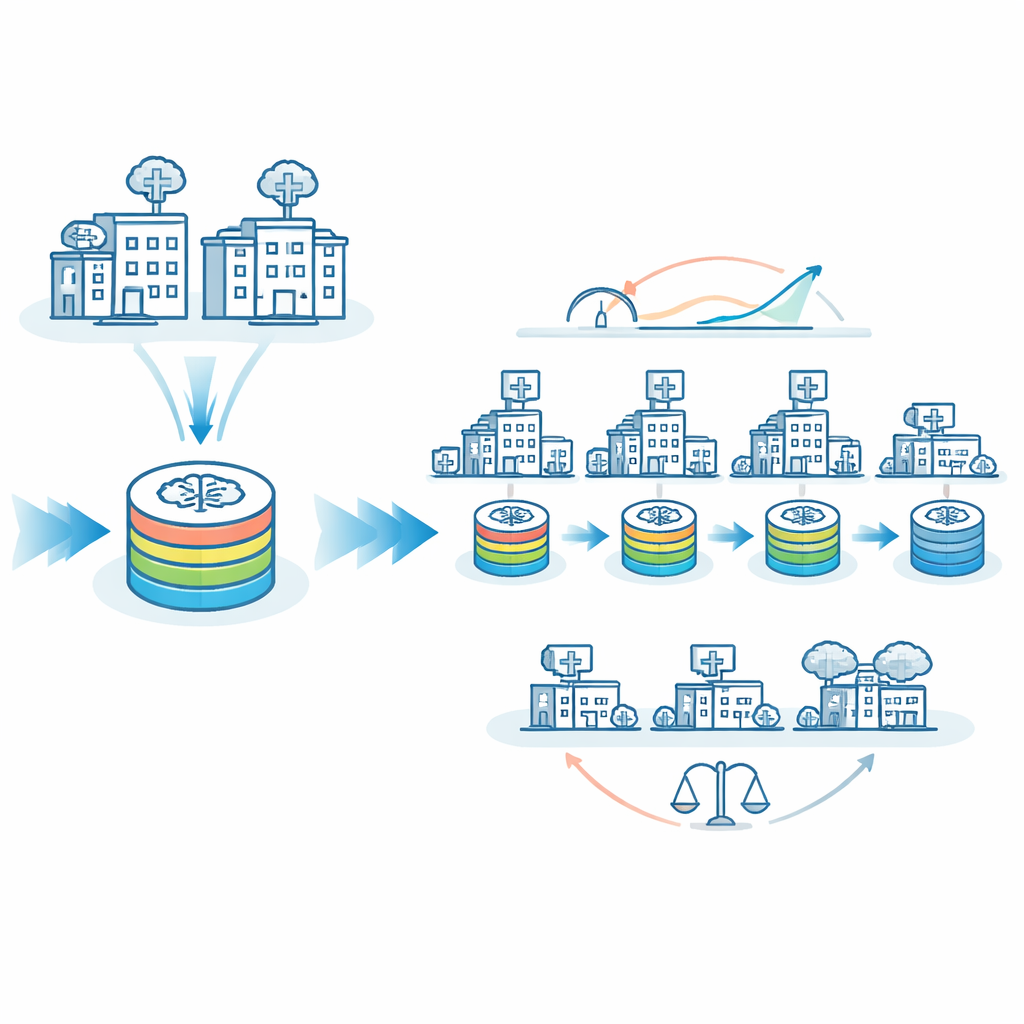
AI rechtvaardiger maken voor grote en kleine ziekenhuizen
Een belangrijke zorg bij medische AI is gelijkheid: werkt een model even goed voor patiënten in kleine, landelijke of slecht uitgeruste ziekenhuizen als voor die in grote academische centra? Het team onderzocht hoe vaak de AI foutief voorspelde bij "grotere" versus "kleinere" locaties. Met alleen het reizende model verschilden de foutclassificatiepercentages met ongeveer 8 procentpunt tussen deze groepen. Met FedTM, goed afgesteld, werden de foutpercentages voor grotere en kleinere locaties vrijwel identiek, rond de 26%. Met andere woorden, het model werd niet alleen nauwkeuriger in het algemeen, maar ook gelijkmatiger in prestaties. FedTM verplaatste ook het grootste deel van de zware rekenlast naar de opwarmfase bij beter uitgeruste sites, waardoor het aantal trainingscycli dat kleine locaties moesten draaien bijna gehalveerd werd, terwijl de totale trainingstijd vergelijkbaar bleef.
Wat dit betekent voor wereldwijde digitale gezondheidszorg
FedTM biedt een praktische route naar AI-tools die privacy respecteren, prestaties verbeteren en voordelen eerlijker over de wereld verdelen. Door zelfs locaties met zeer weinig data invloed te laten hebben op het eindmodel, kan dit kader helpen verzekeren dat mensen in onderbedeelde of afgelegen gebieden niet worden buitengesloten bij de ontwikkeling van nieuwe diagnostische hulpmiddelen. Hoewel de studie zich concentreerde op één type hersenscan en één ziekte, kan de aanpak in principe worden aangepast aan veel andere medische vraagstukken. Naarmate zorgsystemen steeds meer mobiele apparaten en wearables inzetten en regelgeving data‑soevereiniteit benadrukt, kunnen hybride strategieën zoals FedTM essentieel worden voor het bouwen van betrouwbare, inclusieve en verantwoorde medische AI.
Bronvermelding: Souza, R., Stanley, E.A.M., Ohara, E.Y. et al. Combining federated learning and travelling model boosts performance and opens opportunities for digital health equity. npj Digit. Med. 9, 294 (2026). https://doi.org/10.1038/s41746-026-02483-y
Trefwoorden: federated learning, reizend model, Parkinsons ziekte, medische beeldvorming AI, gezondheidsgelijkheid