Clear Sky Science · nl
Een deep-learningmodel dat gestructureerde gegevens en klinische tekst integreert om recidief van atriumfibrilleren te voorspellen
Waarom dit belangrijk is voor mensen met onregelmatige hartslagen
Atriaalfibrilleren, een veelvoorkomend hartritmestoornis, keert vaak terug zelfs nadat patiënten een katheterablatie hebben ondergaan, een invasieve ingreep bedoeld om het hartritme te herstellen. Veel mensen en hun artsen blijven achter met de vraag: wie loopt het grootste risico op terugkeer, en wie kan gerust zijn? Deze studie laat zien hoe moderne kunstmatige intelligentie zowel cijfermatige gegevens als doktersnotities in het medisch dossier kan doorzoeken om nauwkeuriger de kans op terugkeer van atriumfibrilleren te voorspellen, wat mogelijk kan helpen bij het bepalen van vervolgzorg en het voorkomen van herhaalde ingrepen.
Een hardnekkig hartritmestoornis die vaak terugkeert
Katheterablatie wordt veel toegepast om atriumfibrilleren te behandelen door kleine gebieden binnen het hart weg te branden of te bevriezen die de abnormale ritmes veroorzaken of in stand houden. Toch krijgt 30–50% van de patiënten binnen een jaar opnieuw onregelmatige hartslagen, soms met behoefte aan een nieuwe ingreep. Bestaande risicoscores, vooral gebaseerd op een handvol metingen zoals de grootte van de hartkamers en het type atriumfibrilleren, geven slechts een gedeeltelijk beeld. Ze negeren doorgaans gedetailleerde informatie over hoe de procedure is uitgevoerd, hoe het hart op echografie uitzag, en nuances van de algehele conditie van de patiënt die in tekstverslagen verborgen raken. Daardoor hebben artsen nog steeds moeite om te bepalen wie echt intensieve monitoring of aanvullende preventieve behandeling nodig heeft.
Routineziekenhuisgegevens omvormen tot een slimmer voorspellingsinstrument
Onderzoekers in China verzamelden gegevens van 2.508 patiënten die tussen 2015 en 2024 een ablatie wegens atriumfibrilleren ondergingen in vijf ziekenhuizen. De typische patiënt was 65 jaar oud; ongeveer één op de vijf had een recidief van abnormaal ritme tijdens een mediaan follow-up van bijna drie jaar. Voor elke persoon verzamelde het team gestructureerde gegevens — zoals leeftijd, bloeddruk, bloedwaarden, grootte van de hartkamers en bestaande risicoscores — evenals ongestructureerde tekst, waaronder 24‑uurs hartmonitoroverzichten, echorapporten en gedetailleerde procedurenotities van elektrofysiologen. Vervolgens bouwden ze een dubbelvertakt deep-learningmodel: de ene tak verwerkte de numerieke en categorische gegevens, terwijl de andere grote taalmodellen gebruikte om vrije-tekstverslagen om te zetten in kwantitatieve kenmerken die met de cijfers konden worden gecombineerd.
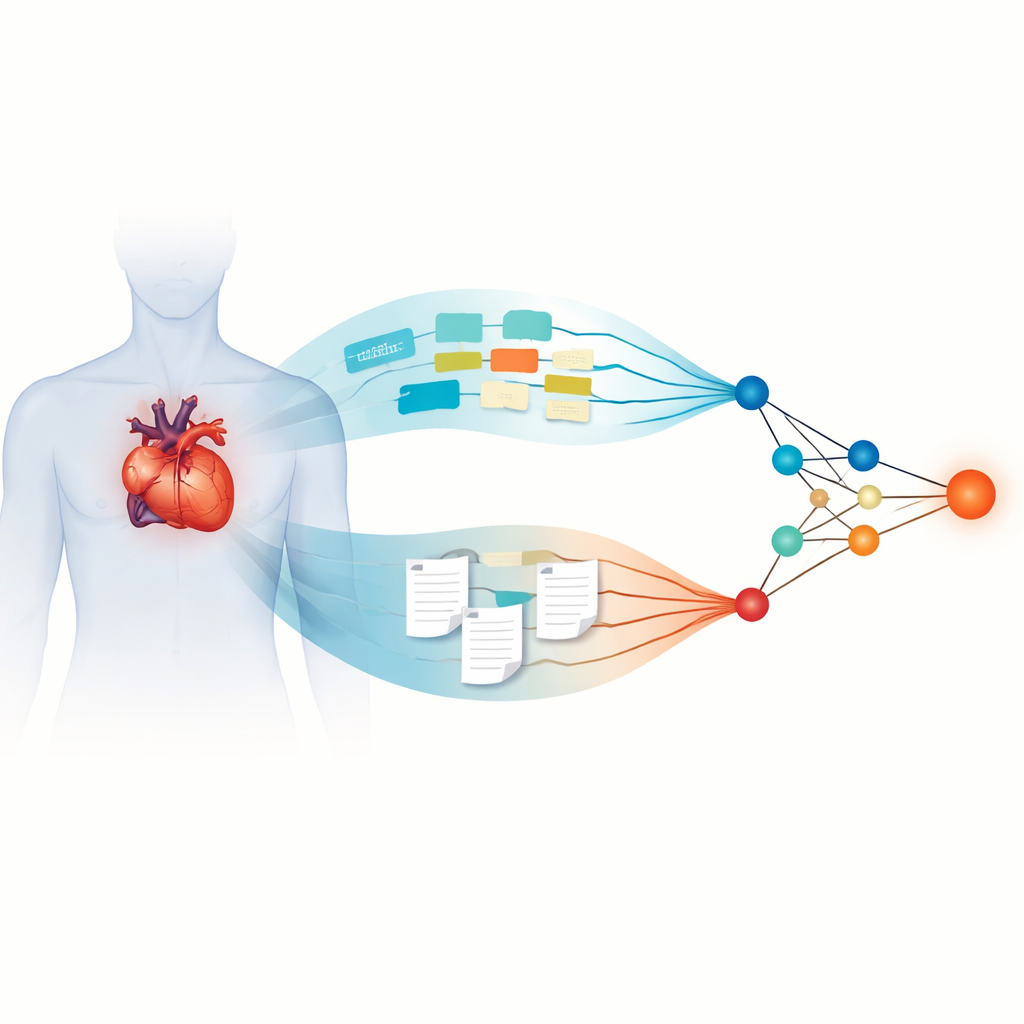
Hoe geavanceerde taalmodellen doktersnotities lezen
De teksttak van het systeem maakte gebruik van vier moderne grote taalmodellen, oorspronkelijk getraind op enorme collecties geschreven materiaal en daarna aangepast aan medische taal. Deze modellen werden fijn afgesteld op gede-identificeerde ziekenhuisverslagen zodat ze gespecialiseerde termen en patronen beter konden begrijpen. De studie vergeleek verschillende taalmodellen om te zien welke tekstkenmerken het beste recidief voorspelden. De uitblinker was MedGemma, een model specifiek geoptimaliseerd voor medische inhoud. Toen de tekstkenmerken daarvan werden samengevoegd met de tak voor gestructureerde gegevens, toonde het resulterende “MedGemma‑Fusion” model opvallende nauwkeurigheid, met area under the receiver‑operating curve boven 0,90 in training, validatie en onafhankelijke testziekenhuizen. Dit betekende dat het model betrouwbaar patiënten kon onderscheiden die vrij zouden blijven van aritmie van degenen die dat niet zouden zijn.
In het zwarte doosje van AI kijken
Om te begrijpen wat het model precies gebruikte om voorspellingen te doen, pasten de onderzoekers interpretatiehulpmiddelen toe die de invloed van elk invoerkenmerk schatten. Bij de gestructureerde gegevens hadden bekende klinische factoren zoals hoe lang de patiënt al met atriumfibrilleren leefde, de grootte van het linkeratrium en of het ritme intermitterend of persistent was het grootste gewicht. Vanuit de tekstkant kwamen sleutelbegrippen gerelateerd aan ablatieprocedures — zoals beschrijvingen van de longvenen en elektrische potentialen — naar voren, wat stappen weerspiegelt die centraal zijn voor succesvolle behandeling. Termen gerelateerd aan hartbeweging in echorapporten waren ook van belang, wat consistent is met het idee dat veranderingen in de atriale beweging wijzen op langdurige schade. Ter vergelijking droegen samenvattingen van 24‑uurs hartmonitoren relatief weinig bij, waarschijnlijk omdat veel patiënten met intermitterend atriumfibrilleren tijdens korte monitorperiodes normale ritmes vertonen.
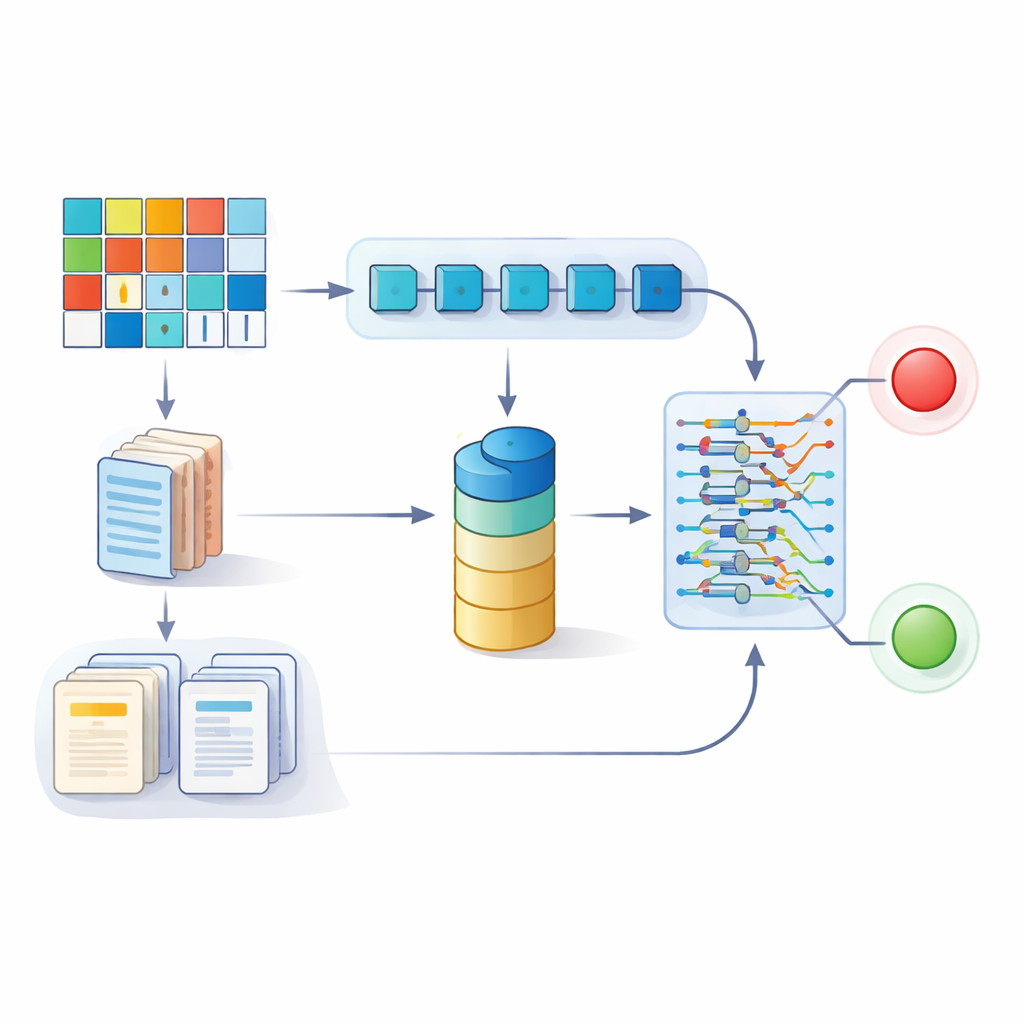
Van onderzoeksmodel naar beslissingen aan het bed
Naast ruwe nauwkeurigheid testte het team hoe goed hun instrument mensen in hoge‑ en lage‑risicogroepen kon indelen met behulp van overlevingsanalyses. Patiënten die door MedGemma‑Fusion als hoog risico werden aangemerkt, hadden duidelijk hogere recidiefpercentages in de tijd. Besliskrompeanalyse suggereerde dat het gebruik van het model om de zorg te sturen bij veel redelijke drempels meer netto‑voordeel zou bieden dan vertrouwen op traditionele scores of enkelvoudige metingen. De auteurs benadrukken echter belangrijke kanttekeningen: de studie is retrospectief, de steekproefomvang — hoewel groot voor een enkel project — is bescheiden voor deep learning, en de rapportagestijlen verschilden tussen ziekenhuizen. Toekomstige versies van grote taalmodellen en bredere tests in andere zorgsystemen zullen nodig zijn voordat dergelijke hulpmiddelen routine worden. Niettemin illustreert dit werk hoe het combineren van alledaagse cijfers in het dossier met de nuance die verborgen ligt in narratieve verslagen voorspellingen kan verscherpen en mogelijk uiteindelijk kan helpen de vervolgzorg en behandelingsintensiteit te personaliseren voor mensen met atriumfibrilleren.
Bronvermelding: Jia, S., Yin, Y., Guan, Y. et al. A deep learning model integrating structured data and clinical text for predicting atrial fibrillation recurrence. npj Digit. Med. 9, 253 (2026). https://doi.org/10.1038/s41746-026-02436-5
Trefwoorden: atriaalfibrilleren, katheterablatie, deep learning, klinische tekstmining, risicovoorspelling