Clear Sky Science · nl
Kwantisering van PET-activatie in adipose weefsel met behulp van niet-geconstraste CT-scans
Waarom het scannen van vet zonder extra straling ertoe doet
Artsen weten dat niet al het lichaamsvet hetzelfde is. Een speciaal type, bruin vet, helpt energie te verbranden en hangt samen met een betere hart- en metabole gezondheid. De beste manier om te zien hoe actief dit vet op dit moment is, vereist een PET-scan: duur, tijdrovend en met extra straling. Deze studie stelt een eenvoudige maar krachtige vraag: kunnen we vergelijkbare informatie halen uit de gewone CT-scans die veel patiënten al krijgen, door kunstmatige intelligentie te gebruiken om het ontbrekende metabolische plaatje aan te vullen?
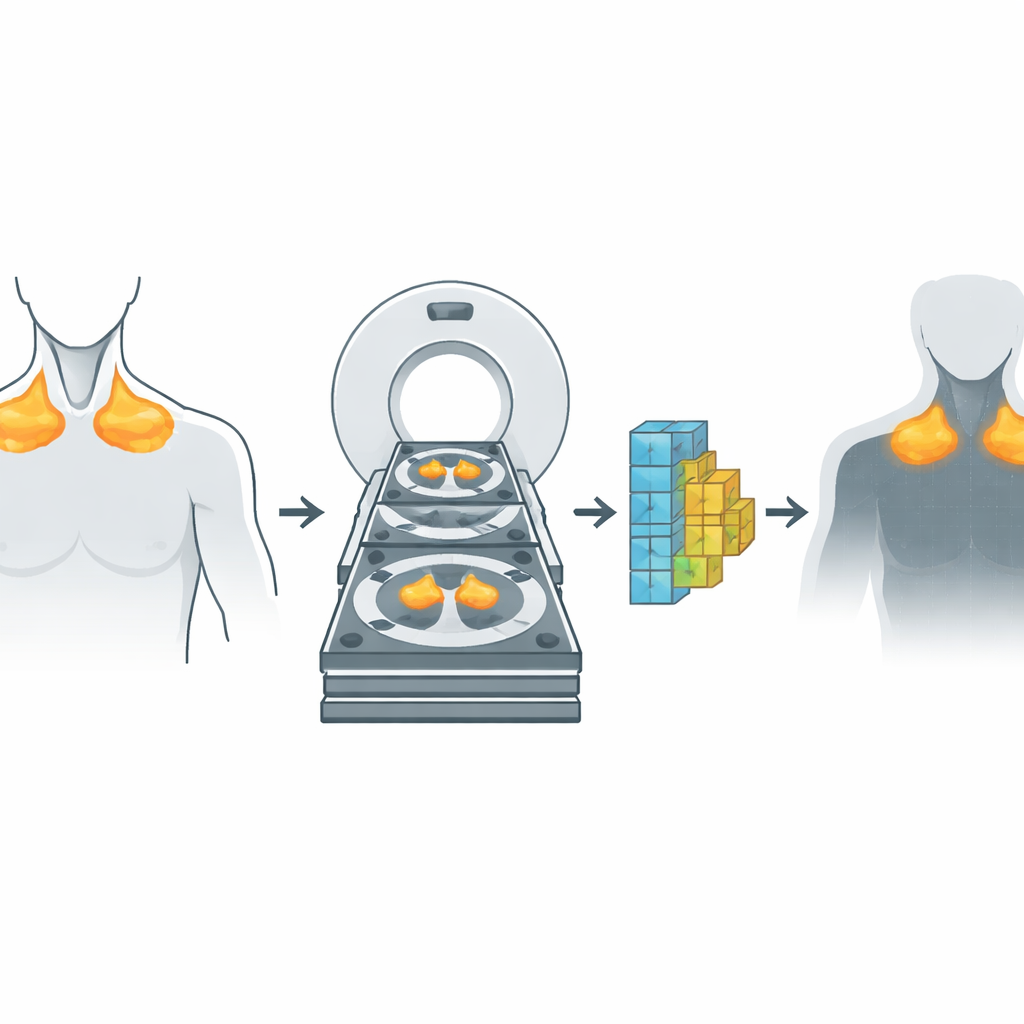
Twee soorten scans, één slimmer beeld
PET- en CT-scans leggen heel verschillende informatie vast. CT toont gedetailleerde anatomie: botten, organen en vetstructuren met hoge resolutie. PET toont functie en laat zien waar cellen suiker verbruiken, een teken van metabole activiteit. Traditioneel vertrouwen artsen op PET om actief bruin vet op te sporen omdat het sterk oplicht wanneer het brandt. De onderzoekers brachten deze werelden samen door gepaarde PET/CT-scans te verzamelen van twee groepen volwassenen – één groep gericht op onderzoek naar bruin vet en een andere bestaande uit patiënten met longkanker. Voor elke persoon brachten ze zorgvuldig de PET- en CT-beelden op elkaar zodat elk punt in het lichaam zowel qua structuur als functie overeenkwam, met speciale aandacht voor vet in de nek en rond de aorta in de bovenborstkas, waar bruin vet vaak voorkomt.
Een neurale netwerk leren PET te imiteren
Met deze gepaarde beelden trainde het team een type deep learning-model genaamd een conditional generative adversarial network. In essentie vroegen ze het netwerk naar een stapel CT-slices te kijken en te genereren hoe een PET-beeld eruit zou zien in hetzelfde gebied. Het model werd aangescherpt om alleen op vet te letten, door weefsel te isoleren binnen de dichtheidswaarden die kenmerkend zijn voor adipose weefsel. Door het systeem te dwingen zich uitsluitend op vet te richten, verminderden ze afleiding door nabijgelegen structuren zoals het hart, lymfeklieren of tumoren. Ze evalueerden ook verschillende trainingsstrategieën: één model opgebouwd uit de bruin-vetcohort, een tweede uit de longkankergroep en een derde die beide combineerde, om te zien hoe goed elke aanpak generaliseerde naar nieuwe patiënten.
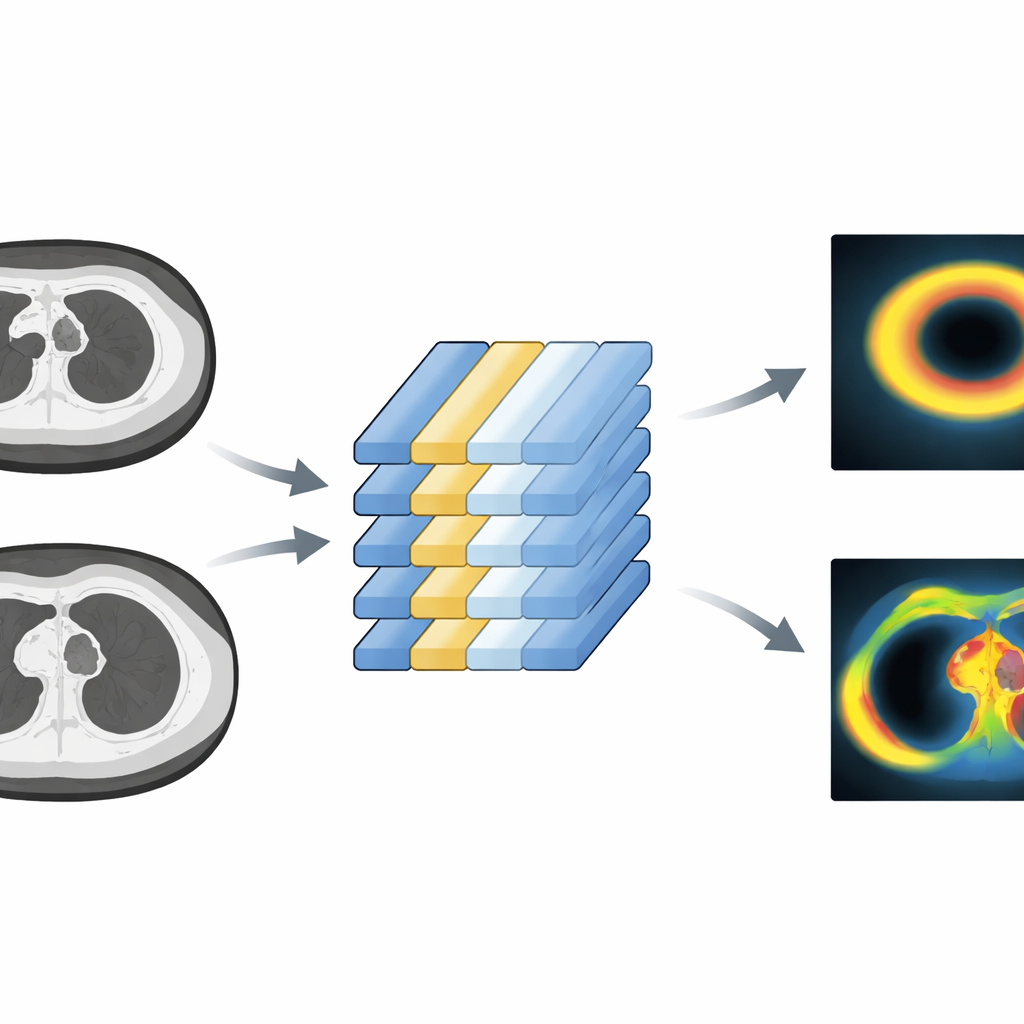
Hoe dicht komt de synthetische PET bij het echte werk?
Om succes te beoordelen vergeleken de onderzoekers de door het model voorspelde metabolische activiteit in vet met de werkelijke PET-metingen. Ze gebruikten verschillende statistische toetsen die zowel naar individuele beeldpunten als naar gemiddelden over gedefinieerde vetregio’s keken. In het algemeen volgden de voorspellingen de echte PET-waarden goed, met kleine gemiddelde fouten en redelijk sterke correlaties in zowel de nek als de bovenborst. De overeenstemming bleef niet alleen behouden binnen de dataset die voor training werd gebruikt, maar ook toen het model werd getest op de onafhankelijke longkankergroep, ondanks dat die scans meer variatie in beeldkwaliteit en patiëntkenmerken vertoonden. Een aanvullende analyse waarbij kleine stukjes van het CT-beeld selectief werden vervaagd liet zien dat het verstoren van vetrijke gebieden de prestatie van het model het meest schaadde, wat suggereert dat het had geleerd te vertrouwen op fysiologisch betekenisvolle structuren in plaats van irrelevante achtergrond.
Beperkingen, kanttekeningen en wat nog werk vereist
De methode is niet perfect en de auteurs zijn terughoudend over de grenzen ervan. De prestaties namen enigszins af in de meer heterogene longkankergroep, waarschijnlijk door verschillen in scanprotocollen en de aanwezigheid van tumoren en ontsteking, die ook PET-signalen veranderen. Het model probeert niet bruine vetactiviteit te scheiden van andere bronnen van opname binnen vet, en het werd alleen getraind op twee lichaamsregio’s, dus het gedrag op andere plaatsen blijft onbekend. Kleine mismatches tussen PET- en CT-uitlijning kunnen het netwerk ook misleiden, vooral wanneer sterke PET-signalen van nabijgelegen weefsels in vet leken te lekken op de trainingsbeelden. Tot slot verbeterden veelgebruikte beeldtrucs, zoals het herschikken van de helderheidsverdeling van PET-waarden om zeldzame hete plekken beter zichtbaar te maken, de training niet en maakten die soms instabieler, zodat de auteurs vasthielden aan standaard, fysiologisch betekenisvolle PET-maten.
Wat dit betekent voor patiënten en toekomstige zorg
Ondanks deze onzekerheden toont de studie aan dat routinematige, niet-geconstraste CT-scans getransformeerd kunnen worden tot PET-achtige kaartjes van metabole activiteit in vet, zonder enige radioactieve tracer te injecteren. Die mogelijkheid kan de deur openen naar grootschalige onderzoeken naar hoe actief vet samenhangt met gewichtsbeheersing, diabetes en hartziekten, en dat alles met scans die veel patiënten al om andere redenen krijgen. Hoewel het huidige hulpmiddel gericht is op onderzoek en niet op diagnose, wijst het op een toekomst waarin één structurele scan stilletjes kan dubbel dienen als venster naar weefselfunctie, waardoor artsen niet alleen begrijpen hoeveel vet iemand heeft, maar hoe ‘levend’ dat vet is.
Bronvermelding: Cano-Espinosa, C., Subrize, M.W., Franquet, E. et al. Quantification of PET activation in adipose tissue from non-contrast CT scans. npj Digit. Med. 9, 209 (2026). https://doi.org/10.1038/s41746-026-02392-0
Trefwoorden: bruin vetweefsel, deep learning beeldvorming, PET CT, metabole gezondheid, lichaamssamenstelling