Clear Sky Science · nl
Het ontcijferen van de ERS–CAF-immunoregulatoire as met multimodale AI en de pan-kanker prognostische en therapeutische voorspellende waarde
In tumoren kijken zonder scalpel
Oncologen erkennen steeds meer dat wat een tumor omringt net zo belangrijk kan zijn als de tumor zelf. Maar die verborgen omgeving herhaaldelijk bemonsteren met biopsieën is invasief en vaak onpraktisch. Deze studie laat zien hoe kunstmatige intelligentie (AI) routinematige medische scans en microscoopbeelden kan lezen om moeilijk te meten immuun- en littekenachtige processen binnen tumoren af te leiden, mogelijk waardoor alledaagse beeldvorming functioneert als een soort "digitale biopsie" die werkt bij verschillende kankersoorten.
De verborgen ondersteunende cellen die kanker vormen
Veel solide tumoren zijn omhuld door een stevige, vezelige laag die wordt gevormd door gespecialiseerde ondersteunende cellen, fibroblasten genoemd. Wanneer deze cellen onder stres staan in de eiwitfabriek van de cel (het endoplasmatisch reticulum), nemen ze een agressieve, kankerondersteunende toestand aan. Bij chordoom, een zeldzame botkanker, bouwen deze gestresste fibroblasten een dicht extracellulair matrix en helpen ze immuuncellen buiten te houden, waardoor behandelingen minder effectief zijn. Vergelijkbare fibrotische, immuun-arme omgevingen komen ook voor bij andere kankers zoals pancreatische en colorectale tumoren, wat suggereert dat deze biologie niet uniek is voor één ziekte. Het probleem is dat de huidige methoden om deze gestresste fibroblasten en hun immuun-blokkerend gedrag te meten afhankelijk zijn van weefselmonsters en complexe moleculaire tests, die moeilijk te herhalen zijn en belangrijke tumorregio’s kunnen missen.
AI leren onzichtbare biologie te zien
De onderzoekers vroegen zich af of standaard MRI-scans vóór operatie en routinematige H&E-pathologievlinders al visuele aanwijzingen bevatten over deze gestresste-fibroblast immuunbarrière. Ze creëerden drie numerieke “referentiescores” uit tumor-RNA-sequencing: één die vastlegt hoe actief het stressprogramma in fibroblasten is, één die samenvat hoe sterk deze cellen lijken te signaleren naar immuuncellen, en één die beschrijft hoe divers de omliggende immuun- en ondersteunende celpopulaties zijn. In plaats van duizenden genen te voorspellen, werd hun AI getraind om slechts deze drie biologisch zinvolle scores uit beelden af te leiden. Hiervoor combineerde het team twee takken: één die MRI-textuur- en vormkenmerken analyseert, en een andere die duizenden kleine regio’s in de digitale snede scant en een taalgestuurde attentiemechaniek gebruikt om te focussen op gebieden die overeenkomen met deskundige beschrijvingen van fibrotisch, immuun-arm weefsel.
Scans en preparaten vermengen voor sterkere signalen
Bij 126 chordoompatiënten met gematchte MRI, pathologievlinders, RNA-data en follow-up presteerde het gefuseerde AI-model beter dan modellen die alleen MRI of alleen preparaten gebruikten. De voorspellingen van de drie moleculaire scores kwamen goed overeen met de RNA-gebaseerde metingen en bleven goed gekalibreerd over verschillende ziekenhuizen en scanners. Toen pathologen onafhankelijk fibrotische en immuun-uitgesloten regio’s markeerden, lichtten de AI’s “hotspots” vaak in dezelfde gebieden op, wat suggereert dat het echte biologie volgde en niet alleen tumorgrootte. Het model vatte ook prognose: hoger voorspelde stress-fibroblast- en signaal-scores werden geassocieerd met slechtere overleving, terwijl grotere voorspelde diversiteit van de micro-omgeving gedeeltelijke bescherming bood. Het toevoegen van deze door AI afgeleide scores aan routinematige klinische factoren verbeterde het vermogen om hoge- en lage-risicopatiënten in de tijd te scheiden.
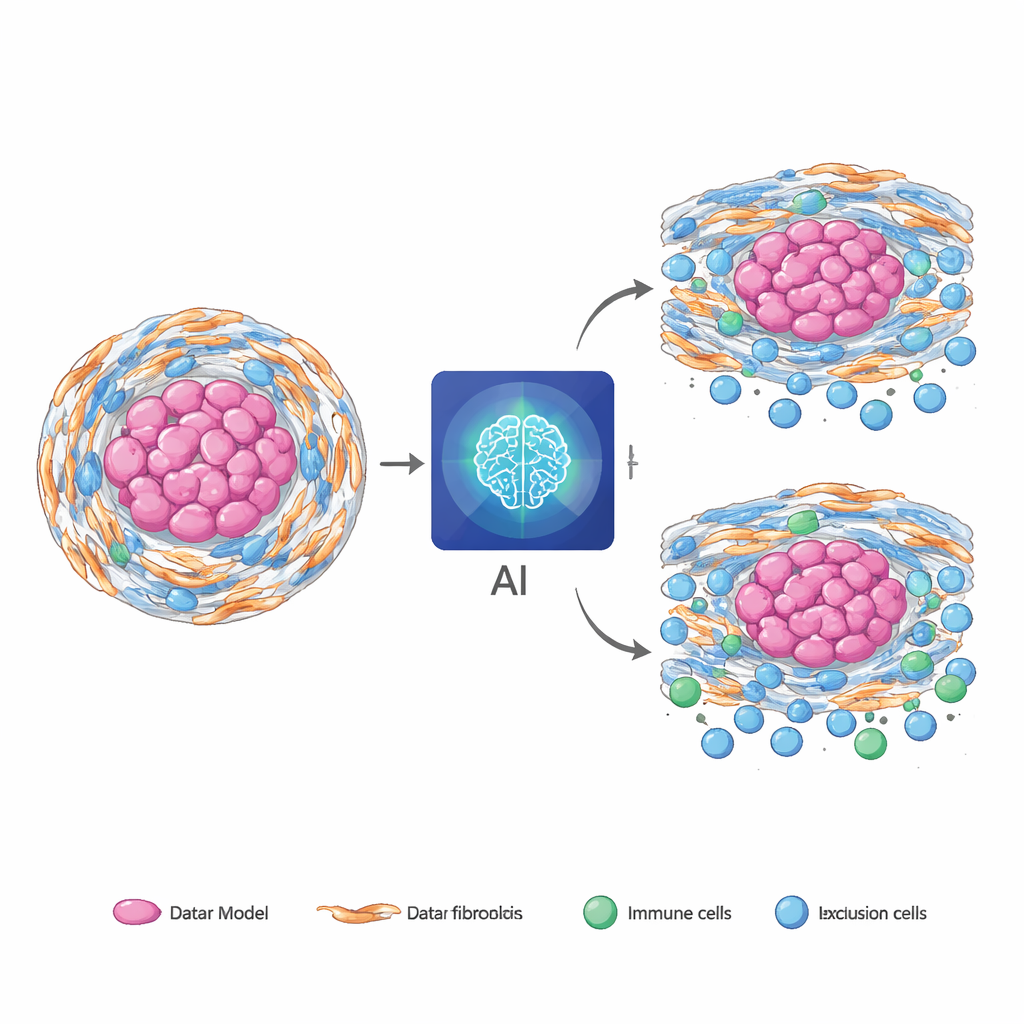
Van zeldzame tumoren naar veelvoorkomende kankers
Een cruciale test was of een model dat volledig op chordoom is getraind “as is” kon worden toegepast op andere, meer voorkomende kankers. Zonder hertraining toegepast op pancreas-, maag- en colorectale tumoren uit grote openbare datasets, toonde de alleen-preparaatversie van het model nog steeds een betekenisvolle overeenstemming tussen zijn beeldgebaseerde voorspellingen en vers berekende RNA-gebaseerde scores. Bij sommige van deze kankers verbeterden de AI-scores de voorspelling van patiëntoverleving bovenop standaard klinische informatie en hielpen ze te onderscheiden welke patiënten waarschijnlijker baat zouden hebben bij chemotherapie. Om de aanpak gemakkelijker inzetbaar te maken waar digitale pathologie beperkt is, destilleerde het team het volledige multimodale model tot een alleen-MRI-versie die het grootste deel van de voorspellende kracht behield terwijl het sneller draaide en minder rekenkracht gebruikte.
Wat dit voor patiënten kan betekenen
Gezamenlijk ondersteunen de resultaten het idee dat routinematige medische beelden stilletjes informatie coderen over gestresste ondersteunende cellen, immuunuitsluiting en micro-omgevingsdiversiteit — kenmerken die normaal dure moleculaire tests vereisen. Hoewel het huidige werk retrospectief is en prospectieve validatie nodig heeft, wijst het op een toekomst waarin een standaardscan en -preparaat niet-invasief tumoren met een vijandige, fibrotische immuunbarrière kunnen signaleren, kunnen helpen bepalen welke patiënten baat hebben bij aanvullende tests of gerichte therapieën, en dit over meerdere kankersoorten kunnen doen zonder extra belasting voor patiënten.
Bronvermelding: Zheng, BW., Xia, C., Tang, M. et al. Decoding the ERS–CAF immunoregulatory axis via multimodal AI and its pan-cancer prognostic and therapeutic predictive value. npj Digit. Med. 9, 199 (2026). https://doi.org/10.1038/s41746-026-02388-w
Trefwoorden: tumormicroomgeving, kankerbeeldvorming, kunstmatige intelligentie, fibroblasten, immunotherapie