Clear Sky Science · nl
Algorithmische beslissing over antibiotica bij urineweginfecties met voorschrijver-geïnformeerde voorspelling van behandelingswaarde
Slimmere antibiotica voor veelvoorkomende infecties
Urineweginfecties (UWI's) behoren tot de meest voorkomende redenen voor het voorschrijven van antibiotica. Het kiezen van het juiste middel is echter een evenwichtsoefening: artsen moeten de infectie genezen, ernstige bijwerkingen vermijden en de maatschappij beschermen tegen toenemende antibioticaresistentie. Deze studie introduceert een nieuw type beslissingsalgoritme dat clinici ondersteunt door grootschalige ziekenhuisgegevens te combineren met de werkelijke prioriteiten van artsen zelf, en zo helpt antibiotica te kiezen die zowel effectief voor de patiënt als veiliger voor de bredere gemeenschap zijn.
Het probleem met krachtige middelen
De moderne geneeskunde vertrouwt op antibiotica, maar overmatig gebruik van brede, zogenaamde “zware” middelen leidt tot een wereldwijde crisis van antimicrobiële resistentie. De Verenigde Naties hebben een doel gesteld: tegen 2030 zou 70% van het wereldwijde antibioticagebruik afkomstig moeten zijn van smallere, eerstelijnsmedicijnen die de Wereldgezondheidsorganisatie als “Access”-antibiotica classificeert. In de praktijk neigen veel clinici naar bredere middelen, aangeduid als “Watch” of “Reserve”, omdat ze vrezen dat een smallere optie kan falen bij resistente bacteriën, vooral bij ernstig zieke patiënten. Daardoor ruilen we vaak lange-termijn risico’s op resistentie in voor kortetermijn gemoedsrust, zonder duidelijke hulpmiddelen om te beoordelen wanneer een veiliger, smallerer middel net zo goed zou werken.
Een algoritme leren denken als een clinicus
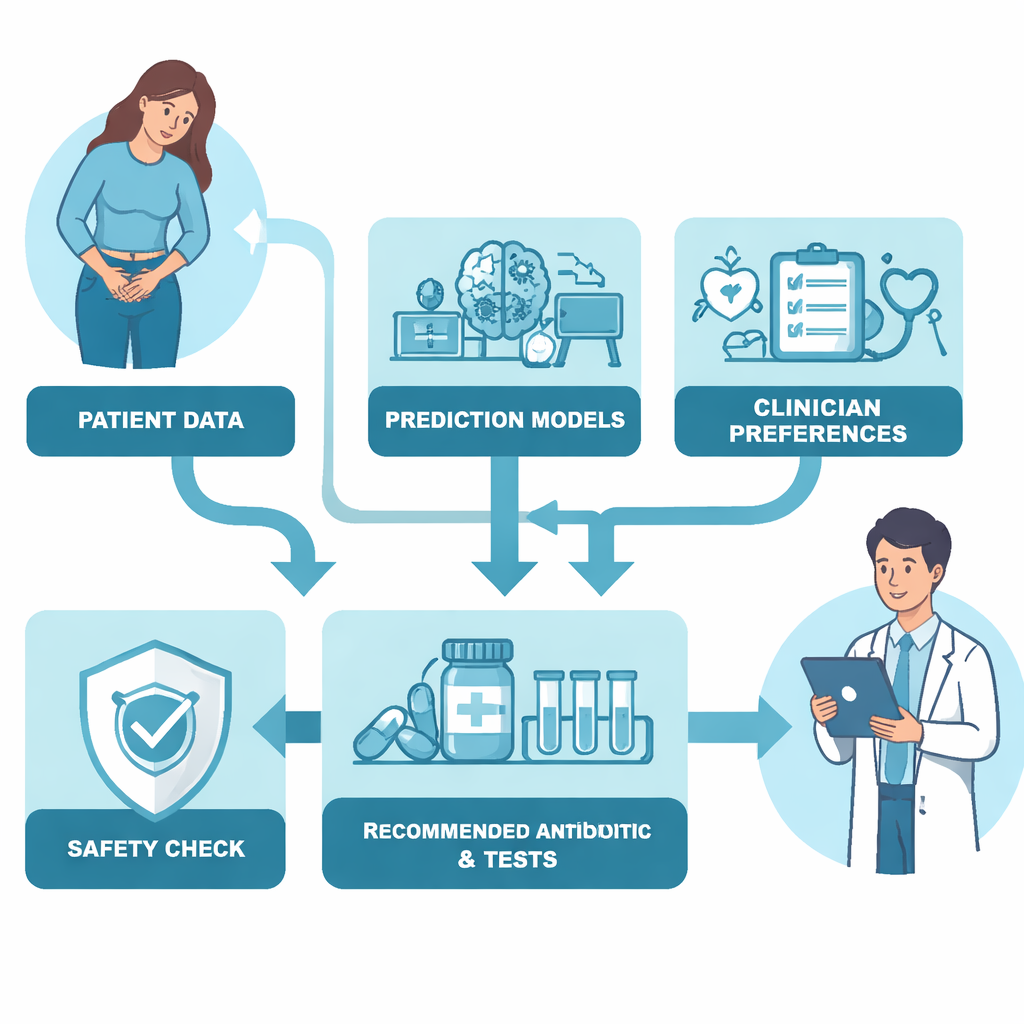
De onderzoekers bouwden een beslissingsalgoritme voor antibiotica bij UWI's met gedetailleerde elektronische dossiers van bijna 94.000 opgenomen patiënten in Boston. Eerst trainden ze voorspellingsmodellen om voor 13 verschillende antibiotica te schatten hoe waarschijnlijk het was dat de UWI-veroorzakende bacteriën gevoelig zouden zijn, en hoe groot de kans was dat behandeling problemen zou veroorzaken zoals Clostridioides difficile-infectie of ernstige medicatietoxiciteit. Vervolgens vroegen ze 49 Britse clinici uit verschillende specialismen een online rangschikoefening te doen, waarbij ze kozen tussen fictieve antibiotica die verschilden in eigenschappen zoals bijwerkingsrisico, geschiktheid voor UWI's, kosten, of het Access- of Watch/Reserve-middelen waren, en of ze in tablet- of intraveneuze vorm kwamen. Door deze ranglijsten te analyseren kwantificeerde het team hoe sterk artsen elke eigenschap waardeerden — bijvoorbeeld hoeveel zij orale, low-toxicity en UWI-gerichte middelen verkozen boven risicovollere of krachtigere opties.
Een vangnet toevoegen voor zeer zieke patiënten
Het uiteindelijke algoritme combineerde deze twee ingrediënten: datagedreven voorspellingen en waardeoordelen van clinici. Voor elke patiënt berekende het een “behandelingswaarde” voor elk antibioticum, rekening houdend met de voorspelde kans dat het middel zou werken, de kans op ernstige bijwerkingen, de Access/Watch/Reserve-classificatie en of het oraal of intraveneus was. Cruciaal is dat het algoritme ook een veiligheidsmechanisme inbouwde op basis van hoe ziek de patiënt leek op de Spoedeisende Hulp. Naarmate de ernst van de ziekte toenam, gaf het algoritme automatisch meer gewicht aan het agressief bestrijden van de infectie en aan de beschikbaarheid van een intraveneuze optie. Met andere woorden: bij licht zieke patiënten probeerde het smallere, orale middelen te bevoordelen, maar naarmate patiënten zieker werden, werd het geleidelijker bereid om sterkere, intraveneuze antibiotica te gebruiken om falen van de behandeling te voorkomen.
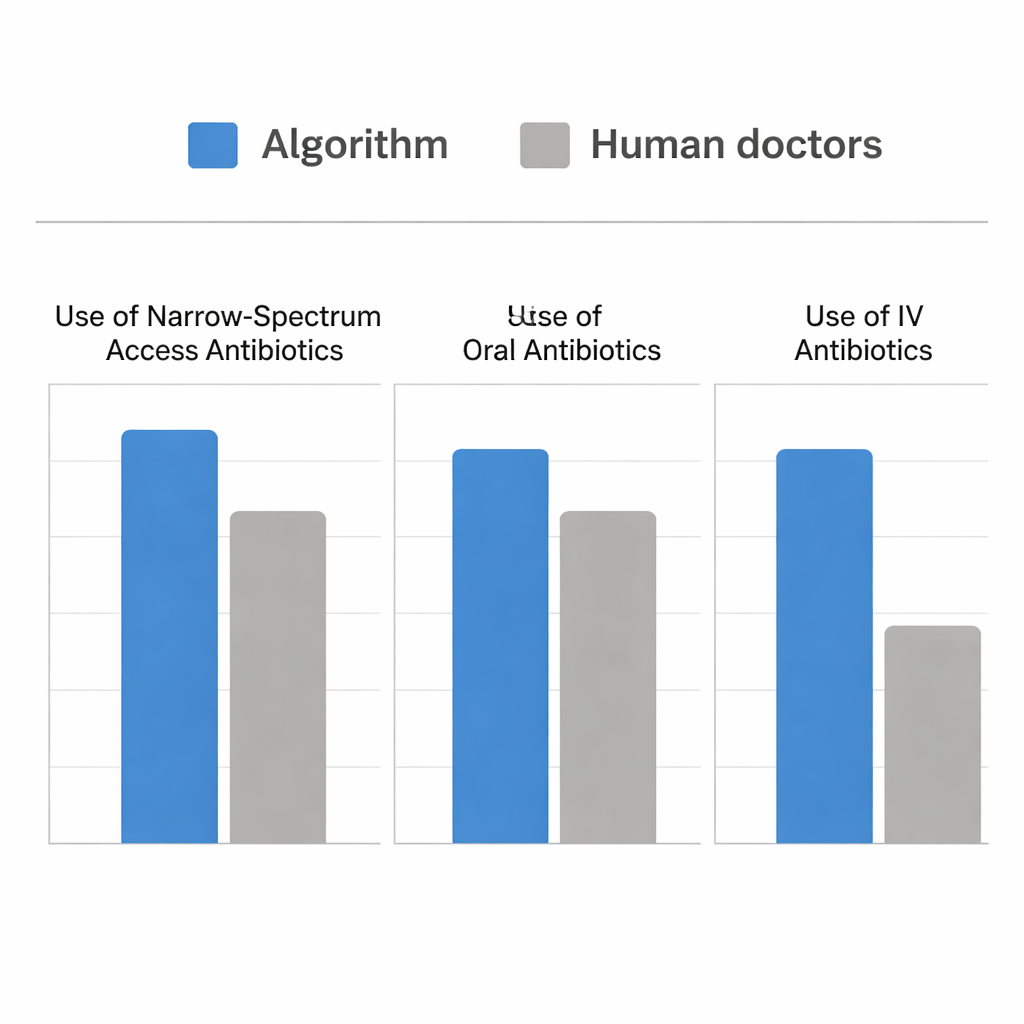
Hoe het algoritme het opnam tegen artsen
Het team voerde daarna een simulatie uit met echte gevallen van de Spoedeisende Hulp waarbij patiënten UWI's en urinekweken hadden. Ze vergeleken de antibiotica die menselijke clinici daadwerkelijk hadden gegeven met de middelen die het algoritme zou hebben gekozen op het moment dat de kweek werd afgenomen. Beide benaderingen waren vergelijkbaar goed in het kiezen van een antibioticum dat de bacterie van de patiënt zou dekken. Het algoritme deed dit echter terwijl het veel meer small-spectrum Access-middelen en veel meer orale behandelingen koos, en minder intraveneuze antibiotica gebruikte. Voor zieker patiënten gedroeg het algoritme zich vergelijkbaar met menselijke voorschrijvers, door gepast te verschuiven naar intraveneuze en krachtigere middelen. Waar het verschilde, was dat het extra kansen herkende — vooral bij matig zieke patiënten — om veilig te behandelen met orale, Access-categorie middelen zoals nitrofurantoïne en ampicilline-sulbactam in plaats van standaard te kiezen voor bredere opties.
Wat dit betekent voor de dagelijkse zorg
Voor de niet-specialistische lezer is de kernboodschap dat dit systeem artsen niet vervangt; het werkt eerder als een rekenmachine voor complexe risico–batenafwegingen waar clinici al om geven maar die ze niet precies in hun hoofd kunnen doorrekenen. Door de prioriteiten van clinici te verbinden met grootschalig bewijs over hoe antibiotica presteren, kan het algoritme behandelingen voorstellen die even effectief zijn voor individuele patiënten maar vriendelijker voor het lichaam en de volksgezondheid — pillen boven infusen waar veilig, en smallere middelen boven laatste-redmiddelopties wanneer mogelijk. Als dergelijke tools in meer omgevingen gevalideerd worden, zouden ziekenhuizen en zorgsystemen dichterbij de mondiale doelen voor verantwoord antibioticagebruik kunnen komen, zonder de veiligheid van ernstig zieke mensen met een infectie in gevaar te brengen.
Bronvermelding: Howard, A., Green, P.L., Zhong, Y. et al. Algorithmic antibiotic decision-making in urinary tract infection using prescriber-informed prediction of treatment utility. npj Digit. Med. 9, 136 (2026). https://doi.org/10.1038/s41746-026-02369-z
Trefwoorden: urineweginfectie, antibioticabeleid, klinische besluitvormingondersteuning, antimicrobiële resistentie, machine learning in de geneeskunde