Clear Sky Science · nl
Annotatie‑vrije 3D-reconstructie en kwantificatie van de netvliesmicrovasculatuur met RADAR
Gezondheid zien via de achterkant van het oog
De kleine bloedvaatjes achter in onze ogen doen veel meer dan alleen het netvlies voeden. Omdat ze niet‑invasief zichtbaar zijn, vormen ze een levend kaartje van de fijne bloedvaten in het lichaam en geven ze vroege aanwijzingen voor aandoeningen zoals diabetes, nierziekte en hartklachten. Deze studie introduceert een nieuwe rekenmethode, RADAR genaamd, die oogscangegevens omzet in gedetailleerde driedimensionale modellen van deze minuscule vaten — zonder afhankelijkheid van arbeidsintensieve hand‑annotaties of kwetsbare kunstmatige‑intelligentie‑training.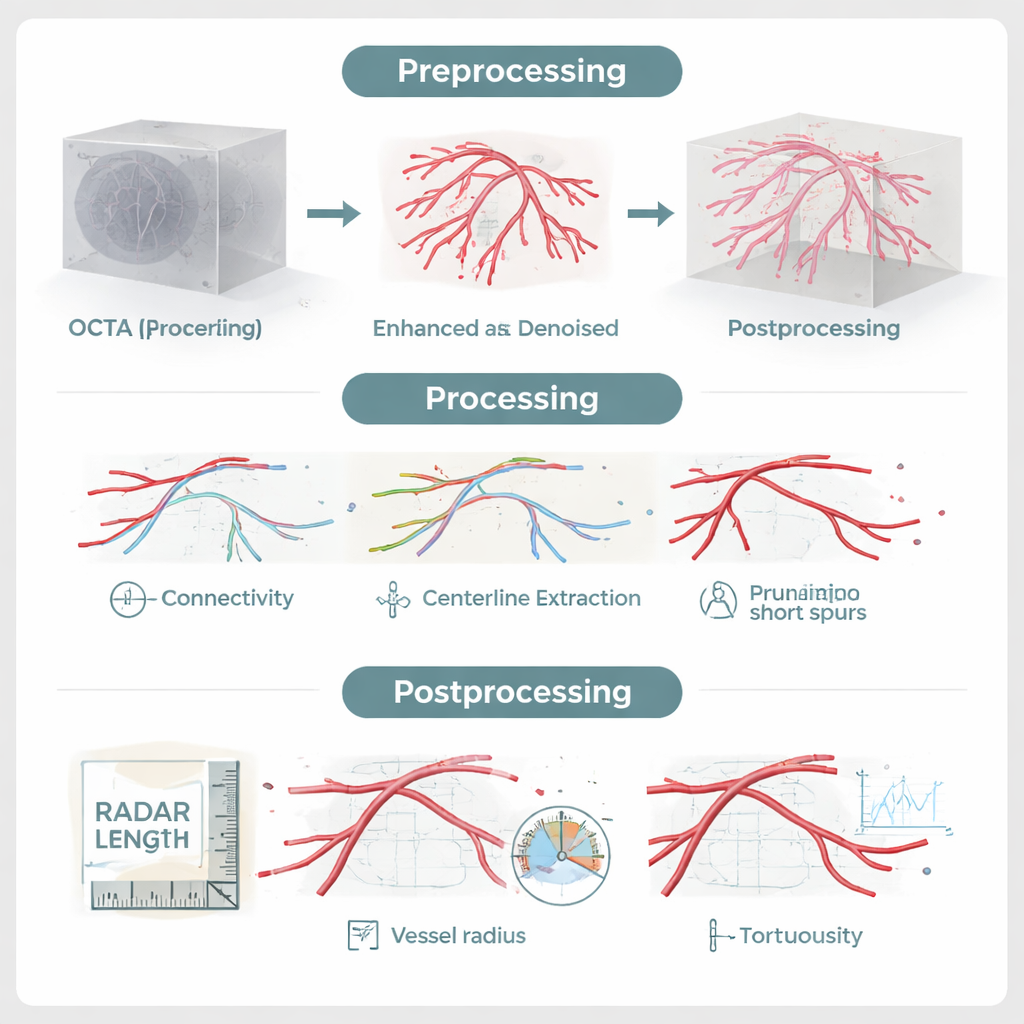
Waarom platte beelden belangrijke aanwijzingen verbergen
Moderne oogscanners, bekend als optical coherence tomography angiography (OCTA), kunnen een volledige 3D‑volume van de bloedstroom in het netvlies vastleggen. Toch worden deze rijke datasets in de kliniek meestal samengeperst tot platte, bovenaanzicht‑beelden. Wanneer alle vaatlagen op één vlak worden geprojecteerd, overlappen structuren op verschillende dieptes, worden kleine gaten afgedekt en kan subtiel verlies van capillairen uit beeld verdwijnen. Dat is een ernstige beperking, omdat vroeg letsel door diabetes en andere ziekten vaak begint in de fijnste capillairen lang voordat duidelijke tekenen van retinopathie of gezichtsverlies optreden.
Een kaart gebouwd op natuurkunde, niet op giswerk
De meeste recente pogingen om het vaatnetwerk uit OCTA‑scans te halen, gaan uit naar deep learning, waarbij neurale netwerken patronen leren uit duizenden voorgeannoteerde voorbeelden. Deze benaderingen kunnen goed werken maar hebben nadelen: ze vereisen grote, zorgvuldig geannoteerde datasets, kunnen falen wanneer de scanner of het imaging‑protocol verandert, en gedragen zich vaak als een “black box.” RADAR kiest een andere weg. Het is een modelgebaseerde pijplijn die vastlegt hoe vaten er in drie dimensies uit zouden moeten zien en zich zouden moeten gedragen — continue, gebogen buizen die vertakken en weer samenkomen — in plaats van te proberen alles uit data te leren. Een gespecialiseerd denoisingfilter versterkt signalen van buisvormige structuren terwijl hun kronkels en bochten behouden blijven, en een connectiviteitsstap gebruikt waarschijnlijkheidsgebaseerde paden om onderbrekingen veroorzaakt door ruis of beweging te overbruggen, geleid door de lokale richting van vaten in plaats van door eenvoudige helderheidsdrempels.
Van wirwar van pixels naar meetbare netwerken
Nadat de vaten versterkt en weer verbonden zijn, extraheert RADAR hun centrale “skelet”, identificeert het vertakkingspunten en eindpunten, en snoeit het kleine uitsteeksels weg die waarschijnlijk artefacten zijn. Wat overblijft is een zuiver 3D‑graf van de retinale circulatie. Vanuit dit model kan de software direct klinisch relevante kenmerken meten: het aantal vaatsegmenten, hun totale lengte en oppervlak, gemiddelde breedte en hoe kronkelig (tortueus) ze zijn. Cruciaal is dat dit apart kan voor de oppervlakkige, midden‑ en diepe lagen van het netvlies, nadat het vaatnetwerk is uitgelijnd op de individuele netvliesanatomie. Validatie tegen nauwgezette handmatige 3D‑tracing toonde aan dat RADAR’s segmentaties zeer nauwkeurig zijn, en het hele proces — van ruwe scan tot volledige set cijfers — duurt ongeveer zes minuten per oog. 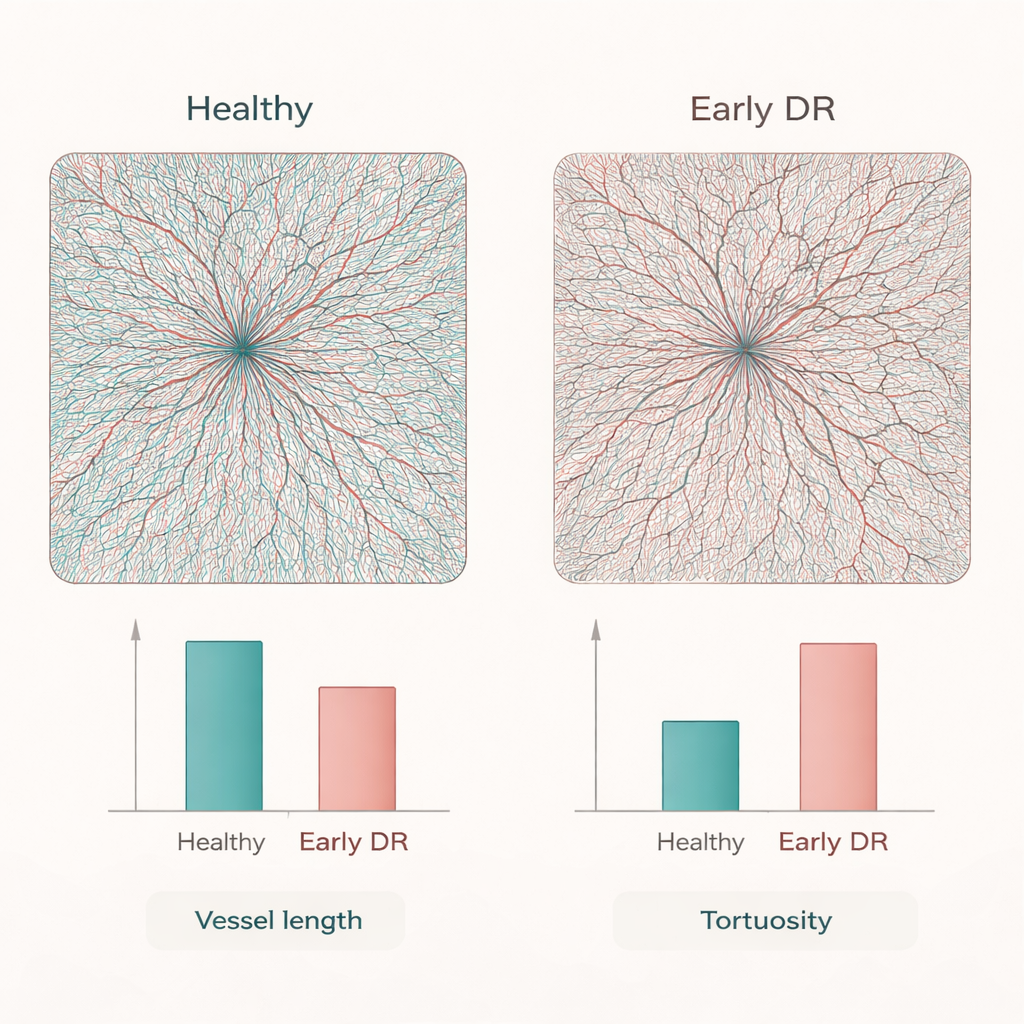
Wat verandert bij vroege diabetische oogaandoening
Om de waarde in de praktijk te testen, pasten de onderzoekers RADAR toe op OCTA‑scans van 50 gezonde volwassenen en 50 patiënten met vroege diabetische retinopathie. Op standaard platte beelden leken beide groepen vergelijkbaar. In tegenstelling daarmee toonden de 3D‑reconstructies dat diabetische ogen al minder en kortere vaatsegmenten hadden, een kleiner totaal vatoppervlak en meer eindpunten met minder vertakkingspunten — tekenen van capillaire uitval en een vereenvoudigd netwerk. Tegelijkertijd waren de overblijvende vaten, vooral de kleinere, meer gedraaid. Door deze veranderingen te condenseren tot gemakkelijk te interpreteren metriek, zoals de verhouding van segmenten tot vertakkingspunten of tortuositeitspatronen per vaatgrootte, ontdekte RADAR ziektegerelateerde hermodellering die waarschijnlijk gemist zou worden met de huidige 2D‑methoden.
Wat dit voor patiënten kan betekenen
Voor niet‑specialisten is de kernboodschap dat deze techniek oogscans omzet in een zeer gedetailleerde 3D‑kaart van de kleinste bloedvaten, waarmee vroeg letsel zichtbaar wordt lang voordat het gezichtsvermogen wordt aangetast. Omdat het niet afhankelijk is van handmatige annotatie of retraining voor elke nieuwe scanner, kan RADAR op grotere schaal over klinieken worden uitgerold om de microvasculaire gezondheid in de tijd te volgen, artsen helpen diabetische oogaandoeningen eerder te detecteren en mogelijk risico’s op bredere cardiovasculaire problemen signaleren. Op de lange termijn kunnen zulke 3D “vasculaire vingerafdrukken” van het oog routine markers worden die preventie en behandeling begeleiden ruim voordat onomkeerbare schade optreedt.
Bronvermelding: Zhang, H., Liu, X., Wu, J. et al. Annotation-free 3D reconstruction and quantification of retinal microvasculature by RADAR. npj Digit. Med. 9, 181 (2026). https://doi.org/10.1038/s41746-026-02366-2
Trefwoorden: netvliesmicrovasculatuur, OCTA, 3D-reconstructie, diabetische retinopathie, vasculaire biomarkers