Clear Sky Science · nl
LLM-gestuurd samenwerkingskader voor kennisverrijkte beoordeling en behandeling van kankerpijn
Waarom slimmere pijnzorg ertoe doet
Kankerpijn is niet slechts een onaangenaam bijverschijnsel — het kan iemands laatste maanden of jaren domineren en slapen, bewegen en zelfs eenvoudige gesprekken bemoeilijken. Hoewel er krachtige pijnstillers bestaan, is veilig en effectief gebruik ervan ingewikkeld, vooral omdat bij elke patiënt de kanker, andere aandoeningen en medicijnen verschillen. Dit artikel beschrijft OncoPainBot, een nieuw kunstmatig-intelligentiekader gebouwd op grote taalmodellen (LLM’s) dat artsen moet helpen complexe dossiers door te lopen, up-to-date richtlijnen te volgen en veiliger, meer gepersonaliseerde pijnplannen voor mensen met kanker op te stellen.
Een lastig probleem in de dagelijkse oncologische zorg
Pijn bij kanker heeft veel oorzaken: tumoren die op botten of zenuwen drukken, operaties, chemotherapie en radiotherapie. Tot 70% van de mensen met vergevorderde kanker heeft ernstige pijn, maar verlichting blijft vaak onvolledig. Artsen moeten opioïden, niet-opioïde middelen en aanvullende behandelingen combineren en tegelijkertijd letten op gevaarlijke bijwerkingen, vooral bij patiënten met fragiele lever- of nierfunctie. Huidige pijnbeoordelingsinstrumenten vertrouwen sterk op korte schalen en vrij-tekstnotities, die per zorgverlener en per ziekenhuis kunnen verschillen. Daardoor kunnen behandelbeslissingen sterk variëren en kunnen kansen om het comfort te verbeteren gemist worden.
Medische tekst omzetten in bruikbare inzichten
LLM’s zoals ChatGPT en Claude kunnen lange, rommelige documenten lezen en samenvatten, wat ze aantrekkelijk maakt voor medisch werk. Maar gewone “chatbots” zijn onveilig voor kankerpijn omdat ze details kunnen verzinnen, geneesmiddelconflicten kunnen missen of de nieuwste richtlijnen kunnen negeren. OncoPainBot pakt deze problemen aan door LLM’s te combineren met een gecureerde kennisbasis opgebouwd uit pijnrichtlijnen van grote kankerorganisaties en door het werk te verdelen over vier samenwerkende “agenten”, die elk een echte klinische rol weerspiegelen. Eén agent haalt sleutelgegevens over iemands pijn uit elektronische dossiers, een andere redeneert welk type pijn aanwezig is, een derde stelt een behandelplan op en een vierde voert een veiligheidscontrole uit gericht op geneesmiddelinteracties, orgaanfunctie en monitoringbehoeften.
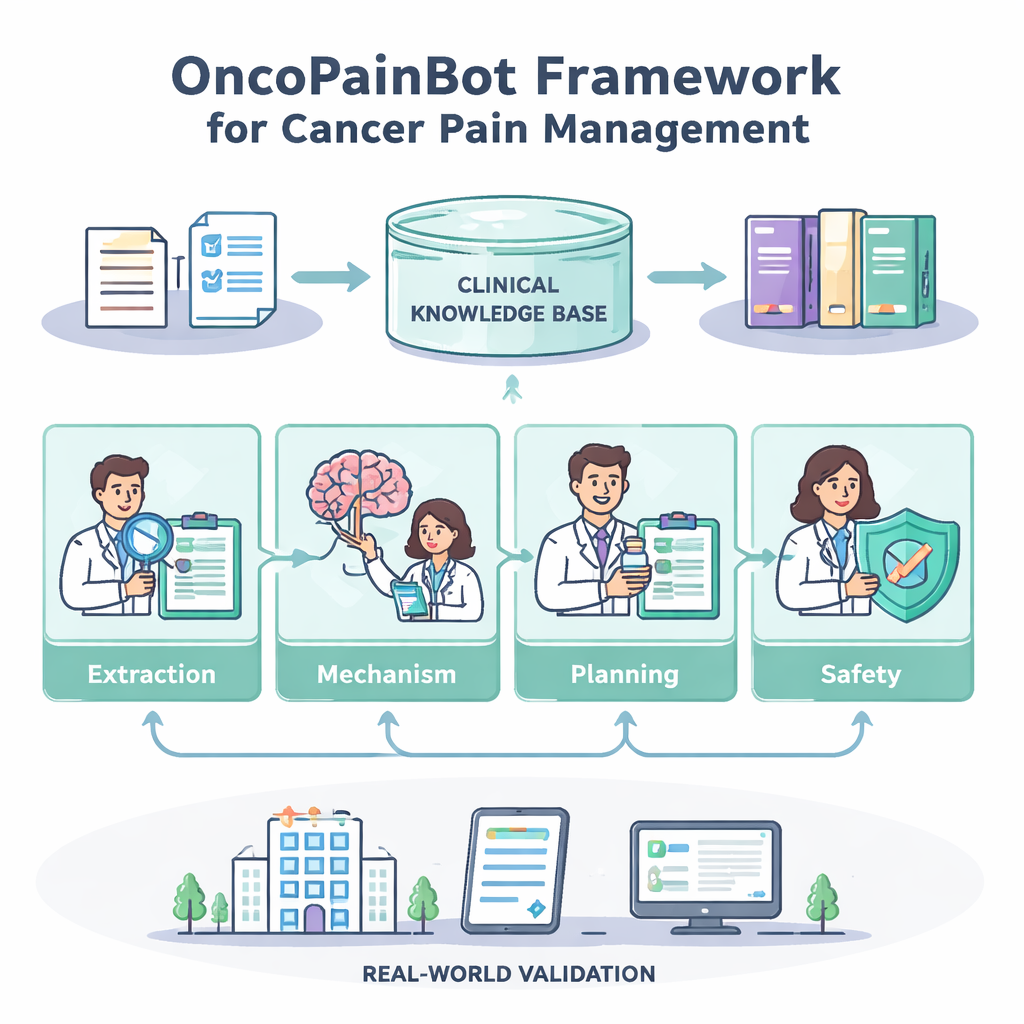
Hoe het viertal samenwerkt
De Pain-Extraction-agent leest vrij-tekstnotities en zet die om in een gestructureerd beeld: waar de pijn zit, hoe hevig die is, wat het verergert of verlicht en welke medicijnen al geprobeerd zijn. De Pain-Mechanism Reasoning-agent gebruikt dat beeld vervolgens om af te leiden of de pijn voornamelijk door weefselschade, zenuwschade of een mengvorm wordt veroorzaakt — een belangrijke aanwijzing bij de keuze van de juiste medicijnen. Daarna raadpleegt de Treatment-Planning-agent de op richtlijnen gebaseerde kennisbasis via een techniek die retrieval-augmented generation heet, waardoor het model specifieke, actuele passages kan ophalen in plaats van alleen op zijn geheugen te vertrouwen. Het stelt stapsgewijze plannen voor — meestal gegrondvest op de ‘pijnladder’ van de Wereldgezondheidsorganisatie — inclusief startdoseringen, manieren om die aan te passen en rescue-doseringen voor plotselinge pijnpieken. Ten slotte fungeert de Safety-Check-agent als een voorzichtige apotheker: hij scant op doseringsproblemen, risicovolle combinaties en ontbrekende laboratoriumgegevens en markeert gevallen waarin de gegevens te dun zijn om een stevige aanbeveling te ondersteunen.
Het systeem op de proef gesteld
Om het beste onderliggende taalmodel te kiezen, vergeleken de onderzoekers zeven toonaangevende systemen op meerdere medische vraag-en-antwoordtesten. Claude 4 bleek het meest accuraat, zij het niet het snelst, en werd daarom geselecteerd als het “brein” van OncoPainBot. Vervolgens evalueerden ze verschillende manieren om dit brein aan de richtlijnenbibliotheek te koppelen en ontdekten dat een “Hybride” retrievalstrategie — met zowel trefwoordmatching als diepere semantische zoekopdrachten — de meest betrouwbare antwoorden opleverde. Met deze opzet draaiden ze OncoPainBot op 516 echte kankerpijndossiers uit een groot Chinees ziekenhuis. De schriftelijke rapporten van het systeem kwamen in taal en inhoud sterk overeen met de aantekeningen van clinici, en de pijnbehandelingsvoorstellen stemden in ongeveer 84% van de gevallen overeen met de daadwerkelijke voorschriften van artsen. Belangrijk is dat de meeste mismatches voortkwamen uit subtiele, patiëntspecifieke nuances — zoals niet-gedocumenteerde opioïde-tolerantie of complexe orgaanfalen — in plaats van duidelijk verkeerde medicijnkeuzes.
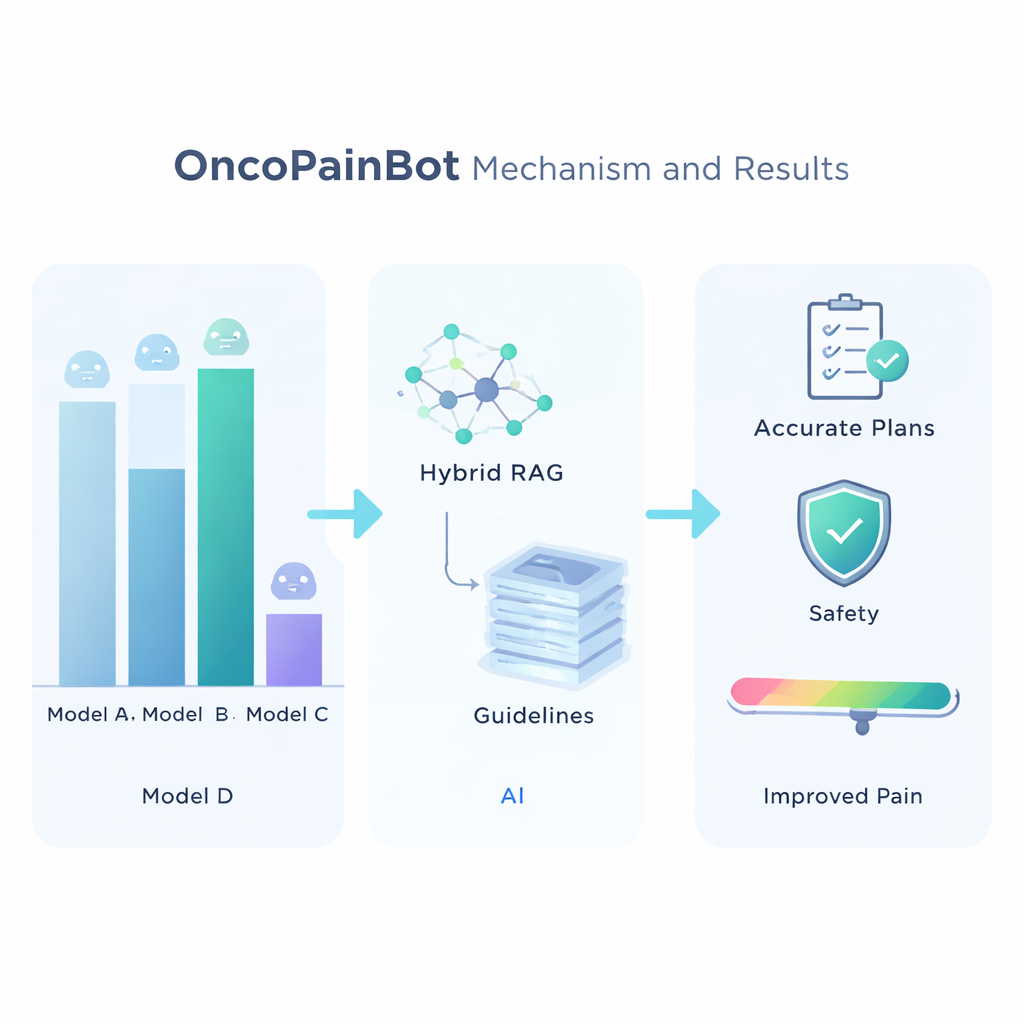
Wat dit voor patiënten kan betekenen
Voor mensen die met kanker leven is de belofte van OncoPainBot niet dat een machine hun behandeling overneemt, maar dat het hun zorgteam een scherper, consistenter second opinion geeft. Het kader is ontworpen als een ‘clinician-in-the-loop’-hulpmiddel: het licht pijnkenmerken uit die anders in notities begraven zouden raken, suggereert richtlijnconforme opties en vestigt de aandacht op veiligheidsproblemen, terwijl de uiteindelijke beslissingen aan menselijke artsen worden overgelaten. De auteurs benadrukken dat hun werk nog in een vroeg, retrospectief stadium verkeert en slechts in één centrum is getest; realtimeproeven in meerdere ziekenhuizen zijn nog nodig. Desondanks suggereren hun resultaten dat zorgvuldig ontworpen AI — gegrond in solide bewijs en transparante redenering — kan helpen om de zorg voor kankerpijn te standaardiseren, gevaarlijke doseringsfouten te verminderen en, belangrijker, de kans te vergroten dat patiënten minder tijd lijden en meer tijd leven.
Bronvermelding: Liu, H., Hu, Y., Li, D. et al. LLM-driven collaborative framework for knowledge-enhanced cancer pain assessment and management. npj Digit. Med. 9, 180 (2026). https://doi.org/10.1038/s41746-026-02362-6
Trefwoorden: behandeling van kankerpijn, klinische besluitvormingsondersteuning, grote taalmodellen, opioïde therapie, retrieval-augmented generation