Clear Sky Science · nl
Toepassing en vooruitzichten van kunstmatige intelligentie in beeldvorming voor de diagnose van prostaatkanker
Waarom slimmer scannen belangrijk is voor de gezondheid van mannen
Prostaatkanker is een van de meest voorkomende kankers bij mannen, en vroegtijdige opsporing kan het verschil betekenen tussen een relatief klein gezondheidsprobleem en een levensbedreigende aandoening. Deze review beschrijft hoe kunstmatige intelligentie (AI) wordt geïntegreerd in moderne medische scans om prostaatkanker sneller te vinden, de ernst te beoordelen en bij te houden of behandelingen werken. Voor lezers biedt het een inkijk in hoe computers stille partners worden in de spreekkamer, artsen helpen sneller en consistenter beslissingen te nemen en tegelijk nieuwe vragen oproepen over data, rechtvaardigheid en vertrouwen.
Van vage schaduwen naar datarijke beelden
Artsen gebruiken verschillende beeldvormingstechnieken om naar prostaatkanker te zoeken. Echografie is snel en goedkoop maar heeft moeite om kanker te onderscheiden van goedaardige vergroting of ontsteking. Magnetische resonantiebeeldvorming (MRI) geeft gedetailleerde beelden van zacht weefsel en is nu de standaardtest voor klinisch significante prostaatkanker, maar kost tijd om te interpreteren en zelfs experts zijn het vaak niet eens. PET/CT-scans, met tracers die binden aan een eiwit genaamd PSMA op kankercellen, zijn uitstekend in het opsporen van uitzaaiingen naar botten en lymfeklieren, maar kunnen zeer kleine plekjes missen en zijn kostbaar. AI vervangt deze machines niet; het werkt bovenop de beelden die zij produceren. Algoritmen reinigen en segmenteren eerst de scans en halen daarna subtiele patronen in helderheid, textuur en vorm naar boven. Deze onzichtbare aanwijzingen, gecombineerd met laboratoriumresultaten zoals PSA-waarden, worden gebruikt om modellen te trainen die verdachte gebieden kunnen markeren, het kanker risico schatten en suggereren waar te biopteren of hoe behandelrespons te beoordelen.
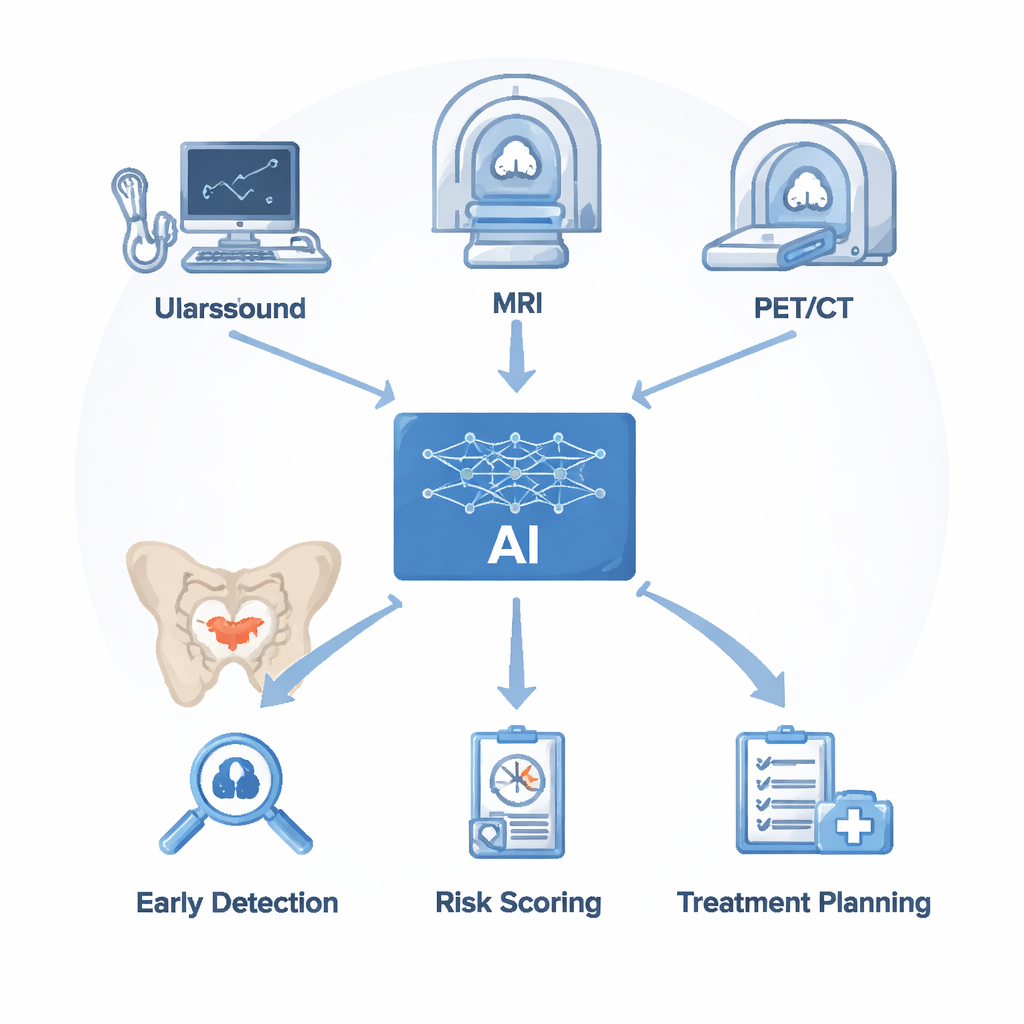
Computers leren zien wat radiologen missen
Bij echografie leren AI-systemen van honderden voorbeelden om kwaadaardige regio’s te herkennen die in de achtergrond kunnen wegvallen. Deep-learningmodellen kunnen automatisch de prostaat lokaliseren en waarschijnlijke tumoren realtime markeren, soms gelijkwaardig aan of beter dan ervaren sonografen, met behoud van snelheid en minder gemiste kleine laesies. Radiomics gaat een stap verder door echobeelden om te zetten in grote reeksen cijfers die weefselpatronen vastleggen die te complex zijn voor het menselijk oog. Machine-learningmodellen die op deze kenmerken zijn gebouwd, presteren aantoonbaar beter dan traditionele echografie en alleen PSA, vooral bij mannen met PSA‑waarden in de verwarrende ‘grijze zone’, waar oudere methoden bijna de helft van de gevallen fout classificeren. Vergelijkbare ideeën drijven AI op MRI aan, waar geavanceerde netwerken de prostaat en zijn interne zones automatisch omcirkelen, het handmatig contouren terugbrengen van ongeveer 20 minuten tot net iets meer dan een minuut en de overeenstemming tussen verschillende lezers aanzienlijk verbeteren.
Scherpere risicoschattingen en slimmer volgen van behandelingen
AI blinkt vooral uit wanneer het informatie uit meerdere MRI-sequenties samenvoegt die anatomie, waterbeweging en bloedstroom tonen. Transformer-gebaseerde modellen, overgenomen uit taalverwerking, combineren deze inputs om waarschijnlijkheidskaarten van klinisch belangrijke tumoren te produceren. In tests op grote patiëntengroepen hebben zulke systemen gelijk of beter gepresteerd dan ervaren radiologen, vooral bij kleine tumoren onder een centimeter die mensen vaak over het hoofd zien. Bij dynamische contrast-MRI kunnen tijdreeksmodellen de veranderende helderheidscurven van geïnjecteerde kleurstof lezen om in te schatten hoe lek de bloedvaten van de tumor zijn—een aanwijzing die samenhangt met agressievere ziekte en hogere kans op terugkeer. In PSMA PET/CT detecteren driedimensionale netwerken, getraind op gehele lichaamsscans, automatisch bot- en lymfekliermetastasen, meten ze de totale tumorbelasting en relateren die aan hoe lang patiënten progressievrij blijven. Andere AI-hulpmiddelen vergelijken scans voor en kort na hormoon- of chemotherapie en voorspellen behandeluitkomsten van enkele maanden veel vroeger dan traditionele regels die op eenvoudige uptake-veranderingen zijn gebaseerd.
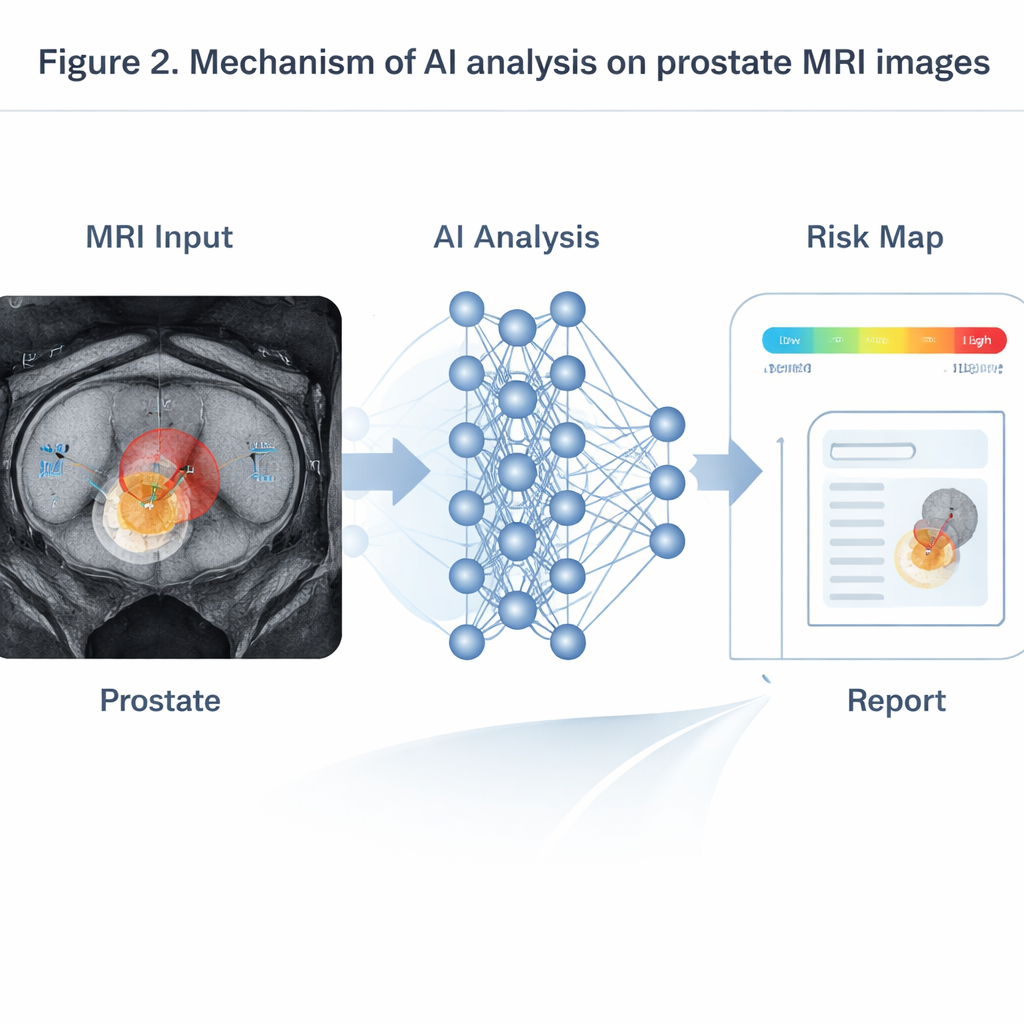
Hobbels: datalekken, black boxes en eerlijk gebruik
Ondanks deze vooruitgang kent de praktische inzet serieuze obstakels. Hoogwaardige, goed gelabelde beeldgegevens zijn nog steeds beperkt en scheef verdeeld richting grote academische ziekenhuizen, terwijl scans uit kleinere centra en diverse populaties ondervertegenwoordigd zijn. Subtiele verschillen tussen scannermerken, instellingen en beeldkwaliteit kunnen ertoe leiden dat modellen die op één plek zijn getraind, elders falen. Veel krachtige AI-systemen werken als ‘black boxes’ en geven een risicoscore zonder duidelijke verklaring, wat het vertrouwen van artsen ondermijnt—vooral wanneer de computer het niet eens is met de ervaring. De review wijst ook op zorgen over privacy, beperkingen bij data‑deling en het risico dat modellen minder goed presteren voor bepaalde groepen, wat gezondheidsverschillen kan vergroten als daar niet zorgvuldig op wordt gestuurd en gecorrigeerd.
Betrouwbare partners bouwen in de kliniek
Vooruitkijkend zien de auteurs AI eerder als een betrouwbare teamgenoot dan als een mysterieuze orakel. Ze schetsen inspanningen om grote, gedeelde datasets tussen ziekenhuizen op te bouwen en tegelijkertijd privacy te bewaren via technieken zoals federated learning, waarbij alleen modelupdates—niet ruwe patiëntgegevens—worden uitgewisseld. Nieuwe ‘uitlegbare AI’-tools proberen te tonen welke beeldregio’s een beslissing hebben gestuurd en deze te koppelen aan bekende pathologie, waardoor artsen concrete redenen krijgen om het eens of oneens te zijn. In plaats van alles‑in‑één modellen zullen op maat gemaakte systemen zich richten op specifieke taken: screening in drukke klinieken, het sturen van biopsieën, het monitoren van behandeling of het opvolgen van hoogrisicopatiënten. Het combineren van beeldvorming met genetische en klinische gegevens kan prognose verder verfijnen en therapie personaliseren. Voor patiënten is de kernboodschap bemoedigend: mits deze technische, ethische en reglementaire uitdagingen goed worden aangepakt, kan AI-verrijkte beeldvorming leiden tot vroegere detectie, minder onnodige biopsieën, snellere antwoorden en meer op maat gemaakte behandelplannen voor prostaatkanker.
Bronvermelding: Wang, X., Zhong, S., Fang, K. et al. Application and prospect of artificial intelligence in diagnostic imaging of prostate cancer. npj Digit. Med. 9, 168 (2026). https://doi.org/10.1038/s41746-026-02354-6
Trefwoorden: beeldvorming prostaatkanker, kunstmatige intelligentie, MRI en echografie, PSMA PET/CT, radiomics