Clear Sky Science · nl
Integratie van multi-omics en machine learning ontcijfert systematisch cellulare heterogeniteit en fibrotische regelnetwerken bij de voortgang van MASLD naar MASH
Waarom dit onderzoek naar leverziekte ertoe doet
Vetsleverziekte die samenhangt met obesitas en type 2-diabetes is nu een van de meest voorkomende leverproblemen wereldwijd. Voor veel mensen blijft de aandoening mild, maar bij een substantieel deel verslechtert zij sluipend tot een agressieve vorm met ontsteking en littekenvorming die kan leiden tot cirrose en leverkanker. Artsen hebben nog steeds moeite te voorspellen wie zal verergeren en om dit gevaarlijke stadium vroegtijdig op te sporen zonder biopsie. Deze studie gebruikt geavanceerde "multi-omics"-instrumenten en kunstmatige intelligentie om in te zoomen op individuele levercellen, en onthult een nieuw herkend immuunceltype en signaleringspad die waarschijnlijk schadelijke littekenvorming stimuleren, en stelt bloedgebaseerde markers voor die op termijn mogelijk niet-invasief hoogrisicopatiënten kunnen signaleren.

Van eenvoudige vetophoping naar gevaarlijke leverschade
De onderzoekers richtten zich op de overgang van metabool dysfunctie-geassocieerde steatotische leverziekte (MASLD), vaak aangeduid als vetslever, naar de ernstigere verwant, metabool dysfunctie-geassocieerde steatohepatitis (MASH). MASLD komt extreem veel voor en treft meer dan een derde van de volwassenen wereldwijd, vooral mensen met obesitas of diabetes. De meeste mensen met MASLD hebben vetafzettingen in de lever maar weinig schade. Bij MASH daarentegen raken levercellen beschadigd, neemt ontsteking toe en vormt zich littekenweefsel. Ongeveer één op de vijf tot één op de drie mensen met MASH zal uiteindelijk cirrose of leverkanker ontwikkelen. Huidige bloedtesten en beeldvorming kunnen niet nauwkeurig zien welke microscopische celveranderingen zich in het orgaan afspelen, waardoor ze vaak het venster voor vroege interventie missen.
De lever cel voor cel bekijken
Om dit probleem aan te pakken combineerde het team verschillende krachtige datatypes uit openbare studies. Ze verzamelden single-cell RNA-sequencinggegevens van meer dan een half miljoen individuele levercellen, spatial transcriptomics die behoudt waar die cellen in het weefsel zitten, bulk-gene-activiteitsprofielen van volledige biopsieën, en chromatine-toegankelijkheidskaarten die laten zien welke DNA-stukken open en actief zijn. Met geavanceerde software groepeerden ze de cellen in zeven brede typen, waaronder levercellen, immuuncellen en ondersteunende cellen genaamd hepatische stercellen. Ze vergeleken gezonde lever, MASLD, en vroege en gevorderde MASH, en brachten in kaart hoe de samenstelling van cellen en hun communicatienetwerken veranderden naarmate de ziekte verslechterde.
Littekenvormende immuun- en ondersteunende cellen die samenwerken
Er verscheen een opvallend patroon: immuuncellen bekend als monocyten en macrofagen, samen met hepatische stercellen, waren veel talrijker in MASH dan in eerdere stadia en neigden ertoe in dezelfde regio’s van aangedaan weefsel te clusteren. Dieper gravend deelden de wetenschappers stercellen op in vijf subtypen, variërend van rustende tot volledig geactiveerde en gladspierachtige vormen. Toen de lever verschoven van MASLD naar MASH, namen rustige stercellen af en geactiveerde, littekenproducerende stercellen toe, waarmee een duidelijk pad van rust naar fibrotische staat zichtbaar werd. Ruimtelijke analyses toonden dat deze geactiveerde stercellen dicht bij de verrijkte macrofagen lagen, wat wijst op een nauwe samenwerking bij het vormen van leverlittekens.
Een nieuw uitgelicht macrofaagtype en een fibrotische signaleringsas
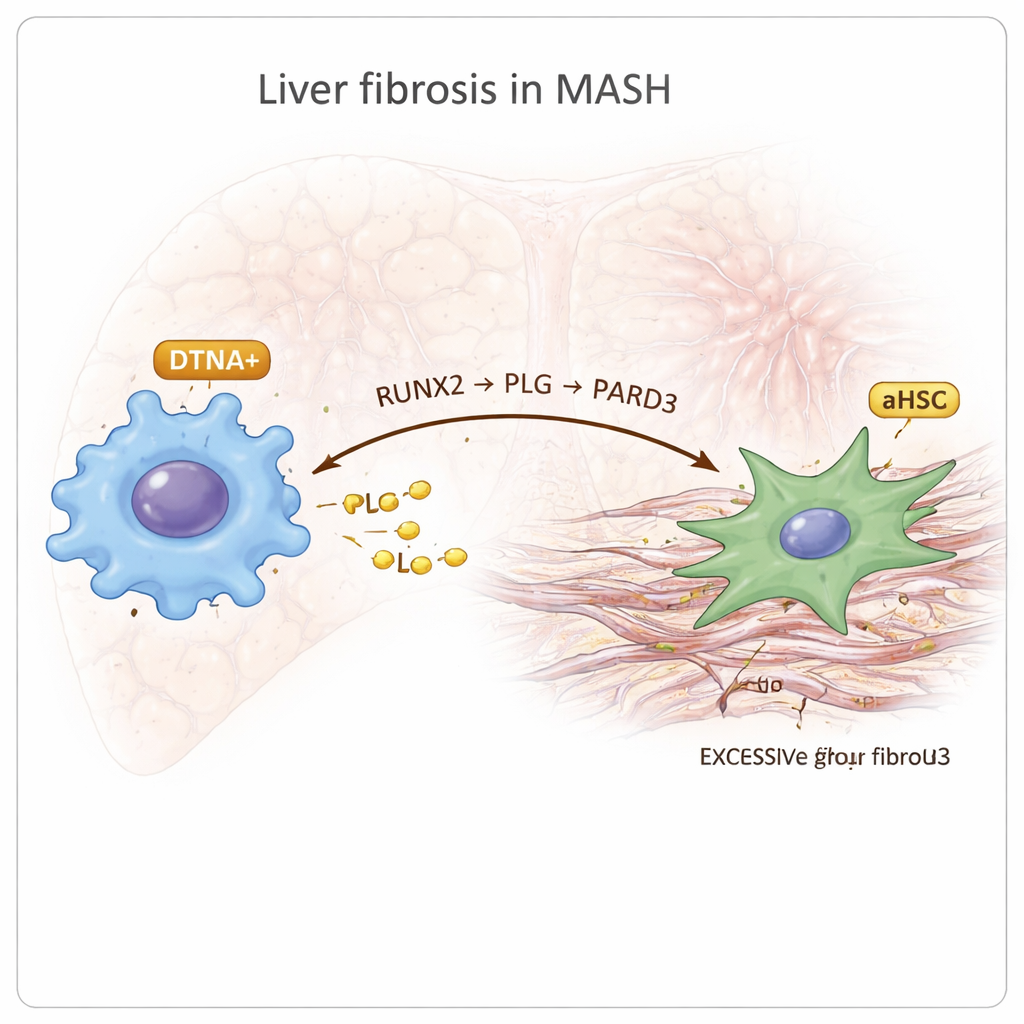
Onder de immuuncellen ontdekten de onderzoekers een duidelijk macrofaagsubgroep gemarkeerd door een gen genaamd DTNA dat specifiek verrijkt was in MASH. Deze DTNA-positieve macrofagen vertoonden kenmerken van zogeheten M2-polarisatie, wat vaak wordt geassocieerd met chronische ontsteking en weefselremodellering, samen met aanwijzingen voor lage zuurstof en sterke ontstekingssignalering. Door het reconstrueren van ontwikkelings"trajecten" concludeerden zij dat deze cellen ontstaan uit residentiële Kupffer-cellen in de lever. Analyse van regelnetwerken wees op een transcriptiefactor genaamd RUNX2 als een hoofdschakel in deze macrofagen. Verdere kaartlegging van cel–celcommunicatie suggereerde dat DTNA-positieve macrofagen communiceren met geactiveerde stercellen via een keten die zij de RUNX2–PLG–PARD3-as noemen: RUNX2 verhoogt de productie van het eiwit PLG in macrofagen, PLG signaleert vervolgens naar stercellen die PARD3 tot expressie brengen, en deze interactie wordt gekoppeld aan intensere fibrose en veranderde bloedstollingsactiviteit.
Van celkaarten naar mogelijke tests en behandelingen
Om te onderzoeken of deze ontdekkingen patiënten konden helpen, trainde en testte het team 113 verschillende machine learning-modellen op grote bulk-gene-expressiedatasets van mensen met MASLD of MASH. Een Elastic Net-model presteerde het beste, en over meerdere onafhankelijke cohorten kwam één gen naar voren als de sterkste voorspeller: DTNA. Hogere activiteit van DTNA en zijn partnergenen, waaronder RUNX2, markeerde consequent patiënten met MASH in plaats van eenvoudige vetslever. De auteurs doorzochten ook bestaande geneesmiddendatabanken en vonden verschillende medicijnen die mogelijk inwerken op de nieuw beschreven RUNX2–PLG–PARD3-route, wat wijst op hergebruikmogelijkheden, hoewel deze ideeën nog laboratorium- en klinische toetsing vereisen.
Wat dit betekent voor mensen met vetsleverziekte
In gewone taal laat deze studie zien dat niet alle leverimmuuncellen en ondersteunende cellen hetzelfde zijn, en dat een specifieke samenwerking tussen een nieuw belicht macrofaagsubtype en littekenvormende stercellen mogelijk een belangrijke motor is die vetslever richting gevaarlijke littekenvorming drijft. Het werk suggereert dat het meten van markers zoals DTNA in bloed of weefsel artsen op termijn zou kunnen helpen identificeren welke patiënten met vetslever het grootste risico lopen door te groeien naar MASH, zonder uitsluitend op invasieve biopsieën te vertrouwen. Het legt ook nadruk op een specifiek signaalpad, de RUNX2–PLG–PARD3-as, als een veelbelovende doelwitroute voor geneesmiddelen die gericht zijn op het vertragen of omkeren van leverfibrose. Hoewel deze bevindingen zich nog in de onderzoeksfase bevinden en verdere validatie behoeven, bieden ze een scherper stappenplan om complexe cellulaire data om te zetten in praktische hulpmiddelen voor vroege diagnostiek en gerichte behandeling.
Bronvermelding: Wen, W., Liu, Z., Tan, W. et al. Integrating multi-omics and machine learning systematically deciphers cellular heterogeneity and fibrotic regulatory networks in the progression from MASLD to MASH. npj Digit. Med. 9, 167 (2026). https://doi.org/10.1038/s41746-026-02352-8
Trefwoorden: vetsleverziekte, MASH, macrofaag, leverfibrose, multi-omics