Clear Sky Science · nl
Gemaskerde auto-encoding, generaliseerbare voortraining en geïntegreerde experts voor verbeterde glioma-segmentatie
Waarom slimmer scannen belangrijk is bij hersentumoren
Hersentumoren die gliomen worden genoemd behoren tot de dodelijkste vormen van kanker, maar artsen besteden nog steeds veel tijd aan het handmatig uittekenen van tumorgrenzen op MRI-scans. Deze zorgvuldige afbakening stuurt chirurgie en bestraling, maar kan 15–20 minuten per patiënt duren en moet in de loop van de tijd telkens opnieuw worden uitgevoerd. De studie introduceert MAGPIE, een kunstmatig-intelligentiesysteem dat leert van tienduizenden hersenscans zonder menselijke labels en vervolgens slechts een handvol deskundig gelabelde gevallen nodig heeft om gliomen betrouwbaar in kaart te brengen. Voor patiënten kan dit snellere, consistentere behandelplanning betekenen, zelfs in ziekenhuizen die geen grote, gecureerde datasets hebben.
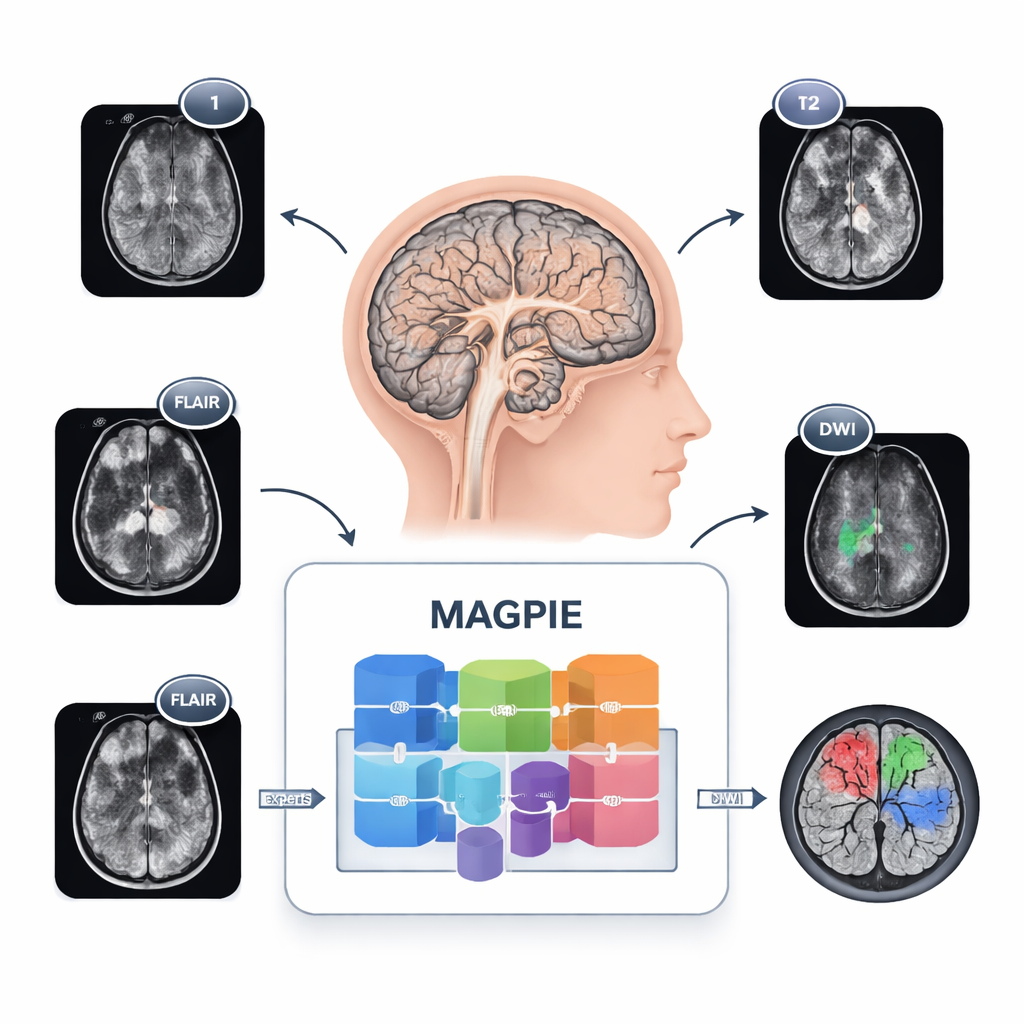
Tumoren op een nieuwe manier waarnemen
Gliomen zijn moeilijk in kaart te brengen omdat ze geen nette bollen vormen. Kankercellen verspreiden zich langs hersenbanen, waardoor vage randen en kleine satellietplekjes ontstaan die lastig te zien zijn. Verschillende ziekenhuizen gebruiken ook uiteenlopende MRI-instellingen en combinaties van sequenties, waardoor een hulpmiddel dat ergens is getraind het elders moeilijk kan krijgen. MAGPIE pakt dit allemaal tegelijk aan. Het werd eerst blootgesteld aan 43.505 niet-gelabelde hersen-MRI-scans afkomstig uit vele studies en scannertypen. Tijdens deze fase leerde het algemene patronen van gezond en ziek hersenweefsel door te proberen ontbrekende delen van beelden te reconstrueren en door verschillende geaugmenteerde weergaven van hetzelfde brein te vergelijken, waardoor het zich richtte op stabiele, betekenisvolle kenmerken in plaats van broze pixel-details.
Meerdere experts het werk laten delen
In plaats van als één monolithisch model te functioneren, bevat MAGPIE een "mengsel van experts". Wanneer het een nieuwe scan analyseert, activeert het per regio van het beeld slechts een kleine subset van acht gespecialiseerde sub-netwerken. Tijdens training delen deze experts het werk vanzelf op: sommigen worden gevoelig voor de heldere, actief groeiende rand van de tumor; anderen richten zich op de dode kern; weer anderen leren de wazige ring van zwelling rond de tumor; en enkelen concentreren zich voornamelijk op normaal hersenachtergrond en grenzen. De auteurs laten dit zien door te meten hoe sterk de activiteit van elk expert overlapt met de verschillende tumorzones die radiologen hebben getekend. Deze taakverdeling verbetert de nauwkeurigheid terwijl de rekencapaciteit beheersbaar blijft—ongeveer de helft van de parameters van het model is actief voor een gegeven patch.
Omgaan met rommelige, real-world scans
Clinische MRI-protocollen zijn verre van uniform. Sommige patiënten hebben vier sequenties, anderen minder; machines van verschillende fabrikanten produceren subtiel verschillende beelden. Het ontwerp van MAGPIE behandelt elke MRI-sequentie als een afzonderlijke "token" en leert ter plekke hoeveel gewicht aan elke sequentie moet worden toegekend, in plaats van te verwachten dat er een vaste set inputs in een vaste volgorde is. Deze kanaal-agnostische aanpak betekent dat het systeem zich kan aanpassen als bijvoorbeeld een contrastversterkte sequentie ontbreekt maar FLAIR wel aanwezig is. Het model gebruikt ook geavanceerde attention-mechanismen die het zowel "ver kunnen zien", waarbij verspreiding over lange afstanden langs witte-stofbanen wordt vastgelegd, als "nauwkeurig kunnen zien", waarbij zeer kleine laesies van slechts een paar millimeter worden opgespoord.
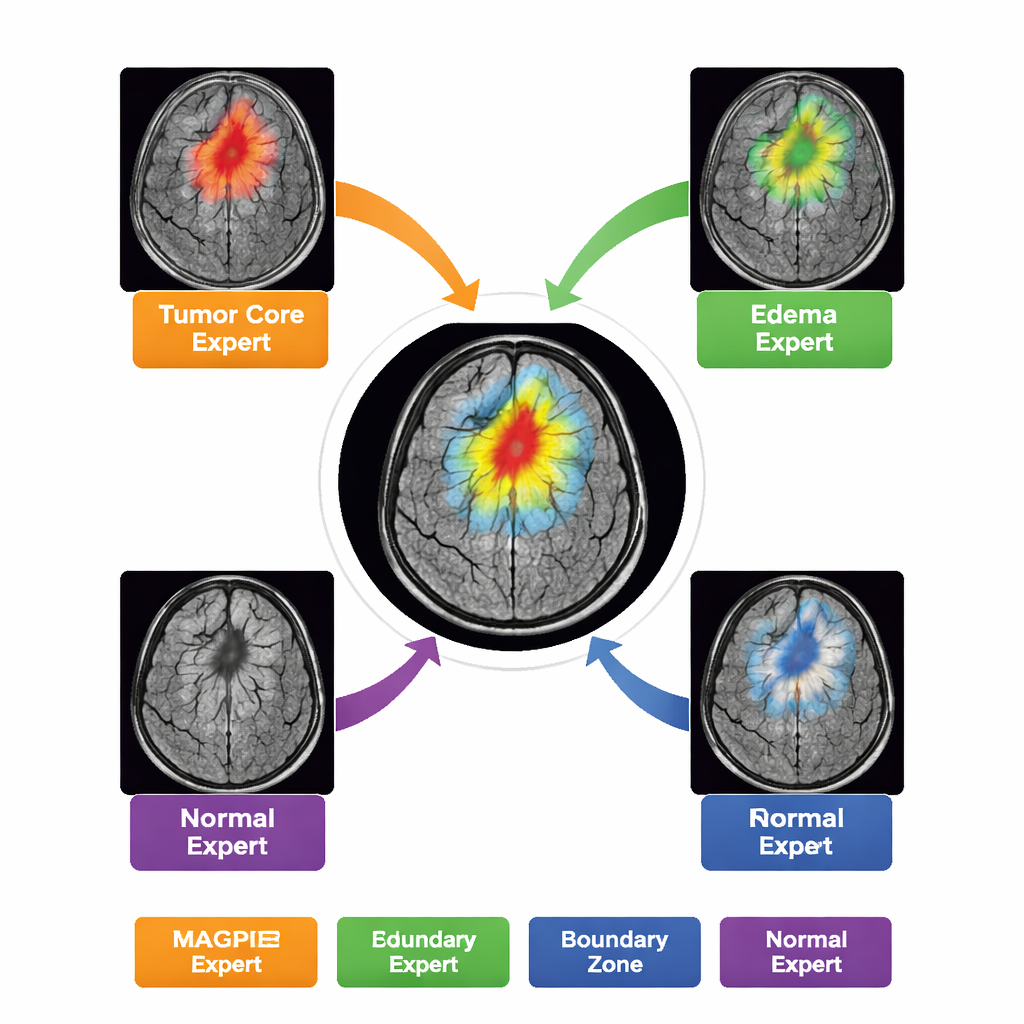
Meer doen met veel minder labels
Na voortraining finetuneden de onderzoekers MAGPIE op slechts 20 volledig gelabelde glioma-gevallen en vergeleken het met standaardmodellen die onder dezelfde condities vanaf nul waren getraind. Op een belangrijke benchmark voor hersentumoren (BraTS21) behaalde MAGPIE een Dice-score—een veelgebruikte overlapmaat in medische beeldvorming—van ongeveer 61%, waarmee het de beste vanaf-het-nul-trainede versie met ongeveer 2,6 procentpunt versloeg en ook beter presteerde dan een sterke eerdere zelfgestuurde methode zonder schadelijke "negatieve transfer". Op uitdagende out-of-distribution data—scans van verschillende ziekten, scannertypen en beeldinstellingen—bleef het beter standhouden en bereikte meer dan 70% Dice op een dataset met witte-stoflaesies zonder extra afstemming. Cruciaal is dat dit prestatieniveau normaal gesproken ongeveer 400 gelabelde gevallen vereist; MAGPIE bereikt het met slechts ongeveer 5% van die inspanning.
Wat dit kan betekenen voor patiënten en klinieken
Voor niet-experts is de kernboodschap dat MAGPIE een berg niet-gelabelde MRI-scans verandert in een krachtig hulpmiddel dat zeer weinig deskundige training nodig heeft om klinisch nuttig te worden. Het kan complexe hersentumoren met realistische grenzen afbakenen, kleine satellietplekken detecteren die andere systemen missen, en betrouwbaar blijven werken wanneer scans van onbekende machines komen of bepaalde sequenties ontbreken. Die combinatie kan de annotatietijd van radiologen met ongeveer 95% verminderen, de drempel verlagen voor kleinere ziekenhuizen om geavanceerde imaging-AI in te zetten, en meer precieze chirurgie- en bestralingplanning ondersteunen. Hoewel verdere validatie bij zeldzame tumortypes en laaggradige gevallen nog nodig is, laat deze studie zien hoe zorgvuldig ontworpen zelfgestuurd leren robuuste, data-efficiënte segmentatie van hersentumoren dichter bij de dagelijkse klinische praktijk kan brengen.
Bronvermelding: Xie, M., Xiao, Q., Wu, H. et al. Masked autoencoding, generalizable pretraining, and integrated experts for enhanced glioma segmentation. npj Digit. Med. 9, 163 (2026). https://doi.org/10.1038/s41746-026-02347-5
Trefwoorden: glioma-segmentatie, hersen-MRI, zelfgestuurd leren, mengsel van experts, AI voor medische beeldvorming