Clear Sky Science · nl
AXL–SHC1-signaleringsas medieert adaptieve resistentie tegen HER2-gerichte tyrosinekinaseremmers bij HER2-afwijkende long- en maagkankers
Waarom sommige tumoren nieuwe medicijnen te slim af zijn
Gerichte kankertherapieën hebben de behandeling voor veel patiënten veranderd door zich te richten op de specifieke moleculen die tumorgroei aansturen. Toch zijn volledige en blijvende remissies zelfs met deze precisiegeneesmiddelen zeldzaam. Deze studie stelt een dringende vraag voor mensen met long- en maagkanker die worden aangedreven door een gen dat HER2 heet: waarom laten tumoren die aanvankelijk krimpen bij HER2-blokkerende pillen vrijwel altijd een hardnekkige kern van cellen achter die later een terugval aanjagen — en hoe zouden artsen die ontsnappingsroute van meet af aan kunnen afsluiten?
Een nadere blik op door HER2 aangedreven tumoren
HER2 is een signaleringsknooppunt dat cellen helpt groeien en overleven. Wanneer het verandert of overexpressie vertoont, kan het normale cellen in borst, maag of long transformeren tot kankercellen. Verschillende moderne geneesmiddelen, tyrosinekinaseremmers (TKI's) genoemd, zijn ontworpen om HER2 binnen kankercellen uit te schakelen. Deze middelen, waaronder mobocertinib en andere, kunnen tumoren doen krimpen en de progressie vertragen. Bij long- en maagkankers zijn de voordelen echter vaak tijdelijk. Een klein deel van de kankercellen weet de aanvankelijke medicijnaanval te doorstaan in een medicijntolerante toestand en evolueert later tot volledig resistente tumoren. Begrijpen wat deze overlevende cellen in leven houdt is essentieel voor het ontwerpen van slimmere eerstelijnsbehandelingen.
Een reserve-levenslijn genaamd AXL
De onderzoekers screenden HER2-veranderde long- en maagkanker-cel-lijnen om te achterhalen welke andere signaalwisselaars de cellen hielpen om HER2-gerichte TKI's te doorstaan. Ze identificeerden een receptor genaamd AXL als een sleutelspeler. Wanneer cellen werden blootgesteld aan HER2-blokkerende middelen, raakte AXL geactiveerd en bleef aangezet, zelfs terwijl de belangrijkste door HER2 gedreven signalen werden gedempt. Deze activatie hield een belangrijk overlevingspad, bekend als AKT–mTOR, draaiende. Het stilleggen van AXL met genetische middelen of het blokkeren ervan met experimentele medicijnen maakte de kankercellen opvallend gevoeliger voor meerdere HER2-gerichte TKI's, wat leidde tot verminderde celgroei en meer celdood in laboratoriumexperimenten.
Hoe hulp-eiwitten de ontsnapping bedraden
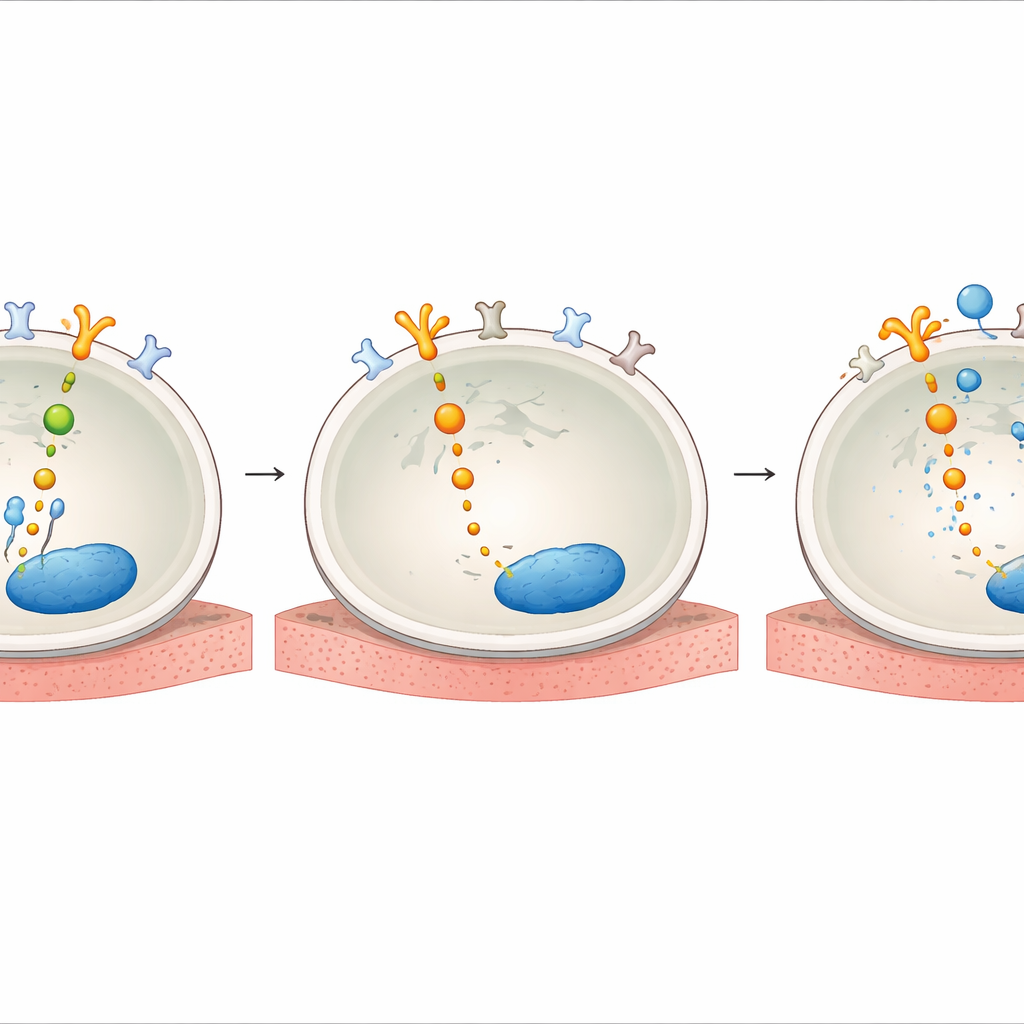
Het team onderzocht vervolgens hoe AXL zo’n invloedrijke rol onder medicijndruk krijgt. Ze vonden dat behandeling met HER2 TKI's de niveaus van GAS6 verhoogde, het natuurlijke partnermolecuul dat AXL op het celoppervlak activeert. Ze lieten ook zien dat AXL na medicijnblootstelling fysiek in verbinding trad met HER2 en diens verwanten EGFR en HER3, waardoor het effectief aansloot op dezelfde overlevingscircuit die HER2 normaal aanstuurt. Binnenin de cel fungeerden adapter-eiwitten genaamd SHC1 en SHCBP1 als bedradingknooppunten. Toen HER2 werd geblokkeerd, liet SHC1 SHCBP1 los en bond in plaats daarvan aan AXL, terwijl SHCBP1 naar de kern verhuisde en daar hielp de celcyclus vooruit te drijven. Het onderdrukken van SHC1 of SHCBP1 verzwakte de AKT-signaleringsroute en verminderde celsurvival, waarmee een AXL–SHC1–SHCBP1-as werd blootgelegd die groei in stand houdt wanneer HER2 is geremd.
Medicijntolerante cellen stoppen voordat ze voet aan de grond krijgen
Om te imiteren wat er bij patiënten gebeurt, lieten de wetenschappers kankercellen dagenlang groeien in aanwezigheid van mobocertinib en selecteerden ze een kleine populatie die het medicijn verdroeg. Deze medicijntolerante cellen groeiden langzaam maar waren duidelijk minder gevoelig voor de HER2-remmer dan de oorspronkelijke cellen. Hun overleving bleef sterk afhankelijk van AXL: het toevoegen van een AXL-blokker verminderde hun groei sterk en dempte AKT-activiteit. In muismodellen met HER2-veranderde, AXL-positieve longtumoren verkleinde de combinatie van mobocertinib met een AXL-remmer de tumoren meer, verminderde het het aantal delende cellen en verhoogde het de tekenen van geprogrammeerde celdood vergeleken met alleen de HER2-remmer — zonder extra toxiciteit. Tumoren die waren geconstrueerd om AXL in overmaat te produceren reageerden veel minder op mobocertinib alleen, maar reageerden opnieuw wanneer de AXL-remmer werd toegevoegd.
Wat dit kan betekenen voor toekomstige behandelingen
Belangrijk is dat weefselmonsters van patiënten met HER2-veranderde long- en maagkankers lieten zien dat ongeveer een kwart hoge AXL-niveaus had en dat de meeste patiënten op zijn minst enige AXL-expressie vertoonden. Dit suggereert dat een aanzienlijke groep patiënten baat zou kunnen hebben bij een behandelingsstrategie die vanaf dag één een HER2-gerichte TKI combineert met een AXL-remmer, in plaats van te wachten tot resistentie optreedt. In eenvoudige bewoordingen toont de studie aan dat veel door HER2 aangedreven tumoren een reserve-groeischakelaar — AXL — in gereedheid houden. Wanneer HER2 wordt geblokkeerd, neemt AXL het over en houdt kankercellen in leven. Het tegelijkertijd uitschakelen van beide schakelaars veroorzaakt dat veel meer kankercellen sterven en vertraagt of voorkomt de opkomst van medicijntolerante overlevers. Als dit wordt bevestigd in klinische onderzoeken, zou deze dubbele-aanvalsstrategie kunnen leiden tot langduriger controle van HER2-veranderde long- en maagkankers.
Bronvermelding: Ishida, M., Yamada, T., Katayama, Y. et al. AXL–SHC1 signaling axis mediates adaptive resistance to HER2-targeted tyrosine kinase inhibitors in HER2-aberrant lung and gastric cancers. npj Precis. Onc. 10, 142 (2026). https://doi.org/10.1038/s41698-026-01385-2
Trefwoorden: HER2-gerichte therapie, AXL-remmer, medicatieresistentie, longkanker, maagkanker