Clear Sky Science · nl
Respons op midostaurine bij AML wordt bepaald door een progenitor‑achtige celtoestand die selectief door SMAC‑mimetica wordt aangevallen
Waarom sommige leukemiemedicijnen hun werking verliezen
Voor veel mensen met een vorm van bloedkanker die acute myeloïde leukemie (AML) heet, brachten nieuwe gerichte middelen hoop—maar niet iedereen profiteert en responsen vervagen vaak. Deze studie stelt een eenvoudig maar cruciaal vraagstuk: waarom negeren sommige leukemiecellen een veelgebruikt middel, midostaurine, en kunnen we een slimme combinatietherapie vinden die deze hardnekkige cellen dwingt af te sterven?
Kijken voorbij de belangrijkste mutatie
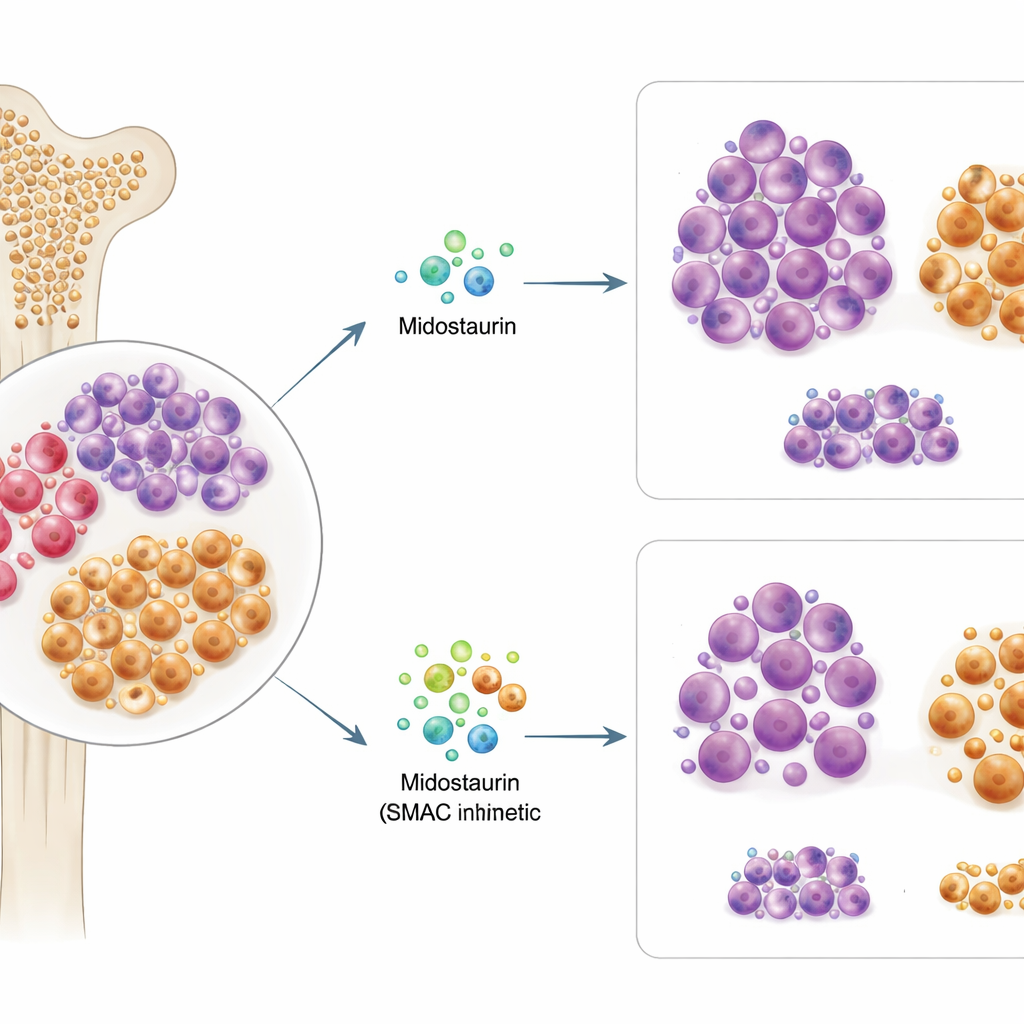
Ongeveer één op de drie AML‑patiënten heeft een verandering in het gen FLT3, dat de leukemiegroei aanjaagt en de reden is waarom midostaurine wordt voorgeschreven. De onderzoekers testten beenmerg‑ en bloedmonsters van 63 patiënten met FLT3‑gemuteerde AML en stelden de cellen in het lab bloot aan midostaurine en meer dan 500 andere kankermedicijnen. Ze vonden dat hoe gevoelig iemands cellen ex vivo waren voor midostaurine sterk overeenkwam met hoe die patiënt later in de kliniek reageerde. Verrassend genoeg voorspelden het precieze type FLT3‑mutatie of de abundantie ervan niet betrouwbaar het succes van midostaurine, wat suggereert dat genetica alleen niet verklaart wie baat heeft.
Een verborgen reservoir van hardnekkige "zaad"cellen
Diepergravend vergeleek het team de totale eiwit‑ en genactiviteitsprofielen tussen cellen die midostaurine‑gevoelig waren en die dat niet waren. Niet reagerende monsters waren verrijkt voor kenmerken van onrijpe, stam‑achtige progenitorcellen—cellen die dichter bij de wortel van bloedvorming staan en worden gedacht als “zaden” die de leukemie kunnen doen herstarten. Daarentegen leken reagerende monsters meer op gedeeltelijk gerijpte immuun‑ en myeloïde cellen. Met geavanceerde single‑cell‑methoden identificeerden de wetenschappers een specifieke populatie leukemiecellen gemarkeerd door oppervlakte-eiwitten CD38 en CD45RA die zich gedroegen als deze progenitor‑achtige zaden. Deze cellen toonden een ongewone organisatie van hun buitenmembraan, wat suggereert dat sleutel‑signaalmoleculen zodanig geordend waren dat overleving werd bevorderd.
Overlevingsbedrading: een switch in signaalroutes
Midostaurine is ontworpen om FLT3‑signaalgeving te blokkeren, wat normaal een keten van signalen voedt waaronder het molecuul STAT5 dat celgroei kan stimuleren. Toen het team signaalactiviteiten in cellijnen en patiëntmonsters na midostaurinebehandeling onderzocht, zagen ze twee duidelijke patronen. In midostaurine‑gevoelige cellen daalde STAT5‑activiteit snel, in overeenstemming met een effectieve FLT3‑uitschakeling. In resistente cellen daarentegen domineerde een andere route: PI3K/AKT, een klassieke overlevingsweg die cellen helpt weerstand te bieden tegen celdood. Deze resistente cellen behielden of verhoogden zelfs AKT‑activiteit na behandeling en vertoonden hogere niveaus van eiwitten die apoptose (geprogrammeerde celdood) blokkeren. Met andere woorden, de bedrading binnen deze progenitor‑achtige cellen leek omgeschakeld naar overleving, zelfs wanneer FLT3 werd geremd.
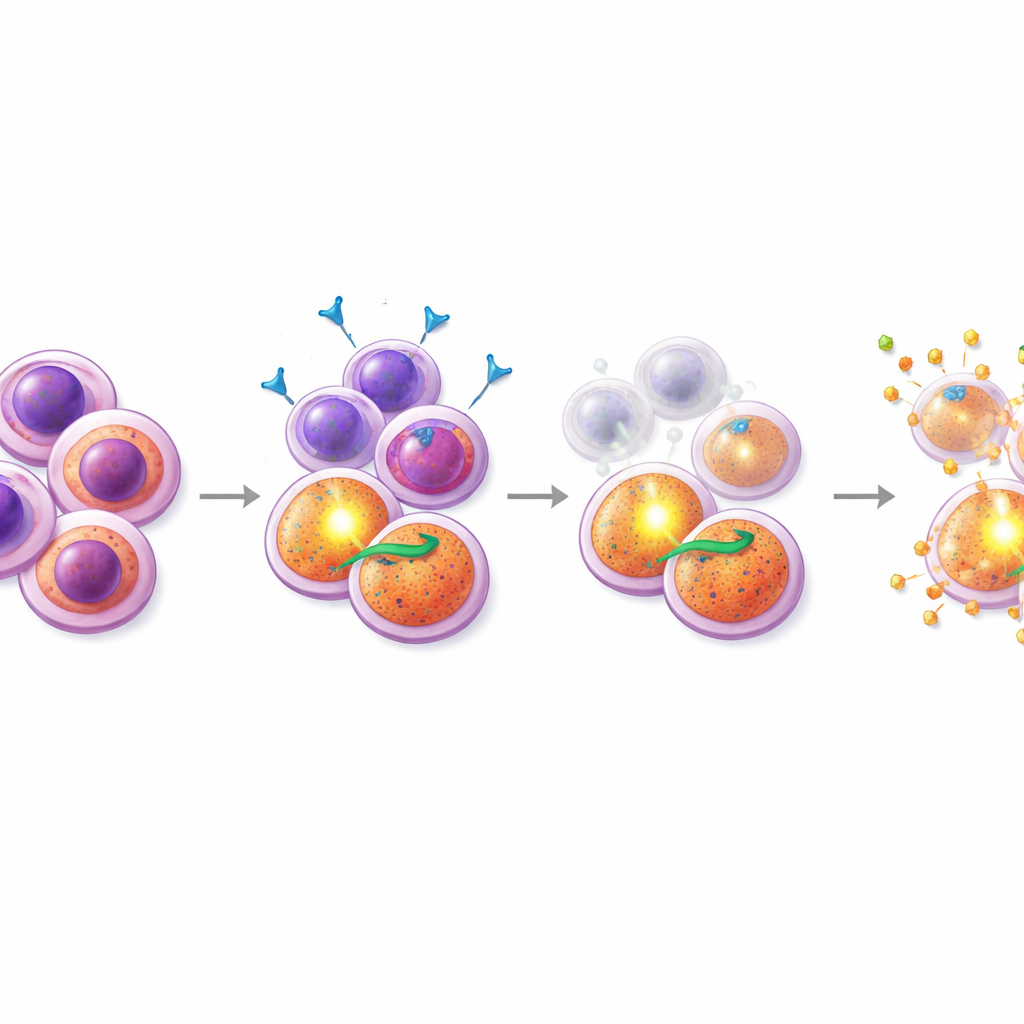
Een partnermiddel vinden dat de zwakke plek raakt
Gewapend met dit inzicht screenden de onderzoekers combinaties van midostaurine met honderden andere verbindingen, met de nadruk op middelen die celdood beïnvloeden. Eén opvallende groep waren SMAC‑mimetica, geneesmiddelen die de “inhibitor of apoptosis”‑eiwitten uitschakelen waarop PI3K/AKT‑gedreven cellen vertrouwen. In resistente patiëntmonsters en een resistente FLT3‑gemuteerde cellijn gaf het toevoegen van SMAC‑mimetica zoals birinapant aan midostaurine sterke synergie: samen doodden de middelen veel meer cellen dan elk afzonderlijk. Cruciaal waren gedetailleerde flowcytometrie‑experimenten die lieten zien dat de midostaurine–SMAC‑mimetica‑combinatie selectief de CD38+CD45RA+ progenitor‑achtige populatie uitputte en de karakteristieke oppervlakte‑markerniveaus verminderde, wat suggereert dat deze therapie specifiek de moeilijk te doden zaden aanpakt. Daarentegen waren combinaties met de goedgekeurde BCL‑2‑remmer venetoclax effectiever tegen een andere, CD34‑hoge subset en lieten ze niet hetzelfde gerichte effect op de resistente cellen zien.
Wat dit betekent voor patiënten
Dit werk suggereert dat resistentie tegen midostaurine niet alleen gaat over de FLT3‑mutatie zelf, maar ook over de “toestand” van de leukemiecellen—hun rijpheidsniveau, membraanorganisatie en favoriete overlevingsroutes. Een progenitor‑achtige CD38+CD45RA+ subset lijkt een belangrijk reservoir van resistentie te vormen, waarbij de signaalvoering verschuift van de gebruikelijke STAT5‑route naar een overlevingsvriendelijk PI3K/AKT‑programma. Door midostaurine te combineren met SMAC‑mimetica konden de onderzoekers deze cellen in het lab weer gevoelig maken en ze richting celdood sturen. Hoewel grotere klinische onderzoeken nog nodig zijn, wijzen de bevindingen op een toekomst waarin artsen functionele testen en celtoestandprofilering — niet alleen DNA‑sequencing — kunnen gebruiken om FLT3‑gerichte combinaties te kiezen die zowel de bulk van de leukemie als haar meest veerkrachtige zaden aanpakken.
Bronvermelding: Struyf, N., Gezelius, H., Lundmark, A. et al. Midostaurin response in AML is shaped by a progenitor-like cell state selectively targeted by SMAC mimetics. npj Precis. Onc. 10, 117 (2026). https://doi.org/10.1038/s41698-026-01363-8
Trefwoorden: acute myeloïde leukemie, FLT3‑remmers, medicijnresistentie, leukemische stamcellen, SMAC‑mimetica