Clear Sky Science · nl
Integratie van vloeibare biopsie en mutatie‑handtekeningen om precisie‑oncologie te bevorderen
Waarom een bloedtest voor de “vingerafdruk” van kanker ertoe doet
Kanker wordt vaak beschreven als een ziekte van het DNA, maar het tumor‑DNA van elke persoon is genetisch verschillend en kan in de loop van de tijd veranderen. Daardoor is het moeilijk voor artsen om de juiste behandeling te kiezen en om te bepalen wanneer een kanker terugkeert of resistent wordt tegen medicijnen. Dit artikel beschrijft een veelbelovende aanpak die een eenvoudige bloedtest, een zogenaamde vloeibare biopsie, combineert met gedetailleerde patronen van DNA‑schade die bekendstaan als mutatie‑handtekeningen. Samen zouden ze artsen in staat kunnen stellen het gedrag van een tumor gedurende de ziekte van een patiënt te volgen en therapieën nauwkeuriger op maat te maken dan ooit tevoren. 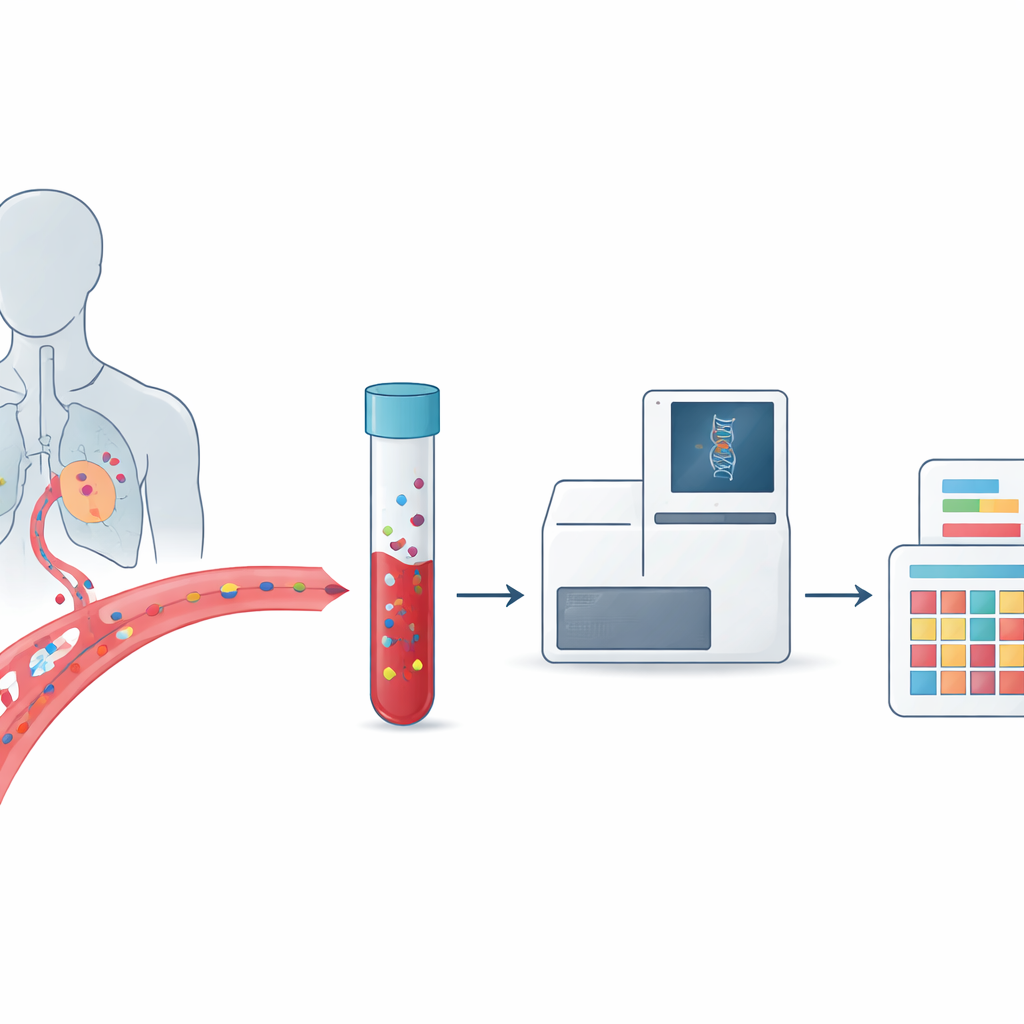
Op zoek naar aanwijzingen in een buisje bloed
Traditionele tumorbiopten vereisen het wegnemen van een stukje tumorweefsel via een operatie of naald, wat pijnlijk kan zijn, risico’s met zich meebrengt en lastig te herhalen is. Vloeibare biopsie volgt een andere route: ze zoekt naar sporen van kanker die tumoren in de bloedbaan en andere lichaamsvloeistoffen achterlaten. Die sporen omvatten intacte tumorcellen en korte fragmenten DNA die vrijkomen wanneer kankercellen afsterven. Omdat bloedmonsters regelmatig kunnen worden afgenomen en materiaal van meerdere tumorlocaties kunnen vangen, biedt vloeibare biopsie een bewegend beeld van hoe een kanker groeit, uitzaait en op behandeling reageert, in plaats van een enkele momentopname.
Van individuele mutaties naar algehele schadepatronen
De meeste huidige vloeibare‑biopsietests richten zich op het opsporen van specifieke mutaties in een korte lijst met genen die bepalend zijn voor het gebruik van gerichte geneesmiddelen. Niet alle tumoren dragen echter zulke “behandelbare” veranderingen, en kankers met veel uiteenlopende mutaties kunnen makkelijk buiten vaste genpanelen vallen. In het afgelopen decennium hebben krachtige DNA‑sequencinginstrumenten aangetoond dat de mutaties in een kankergenoom niet willekeurig zijn: ze vormen herkenbare patronen die worden bepaald door factoren zoals tabaksrook, ultraviolet licht, defecte DNA‑reparatie of zelfs chemotherapie. Deze terugkerende patronen, mutatie‑handtekeningen genoemd, fungeren als vingerafdrukken van de processen die het DNA beschadigd hebben gedurende de levensloop van de tumor.
De geschiedenis en kwetsbaarheden van de tumor lezen
Mutatie‑handtekeningen kunnen onthullen waar een kanker mogelijk is ontstaan en welke interne reparatiesystemen kapot zijn. Zo tonen longkankers bij rokers vaak een patroon dat gekoppeld is aan tabaksblootstelling, terwijl sommige colonkankers handtekeningen dragen van falende mismatch‑reparatie, een defect dat ze ook zeer gevoelig maakt voor bepaalde immunotherapieën. Andere handtekeningen wijzen op problemen in een DNA‑reparatiepad dat homologe recombinatie heet, wat tumoren bijzonder kwetsbaar kan maken voor platina‑therapieën en PARP‑remmers. Experimentele studies in cellen en diermodellen hebben bevestigd dat veel milieuchemicaliën en kankertherapieën onderscheidenbare mutationale sporen achterlaten die overeenkomen met die bij patiënten, wat de koppeling tussen handtekening en oorzaak versterkt. 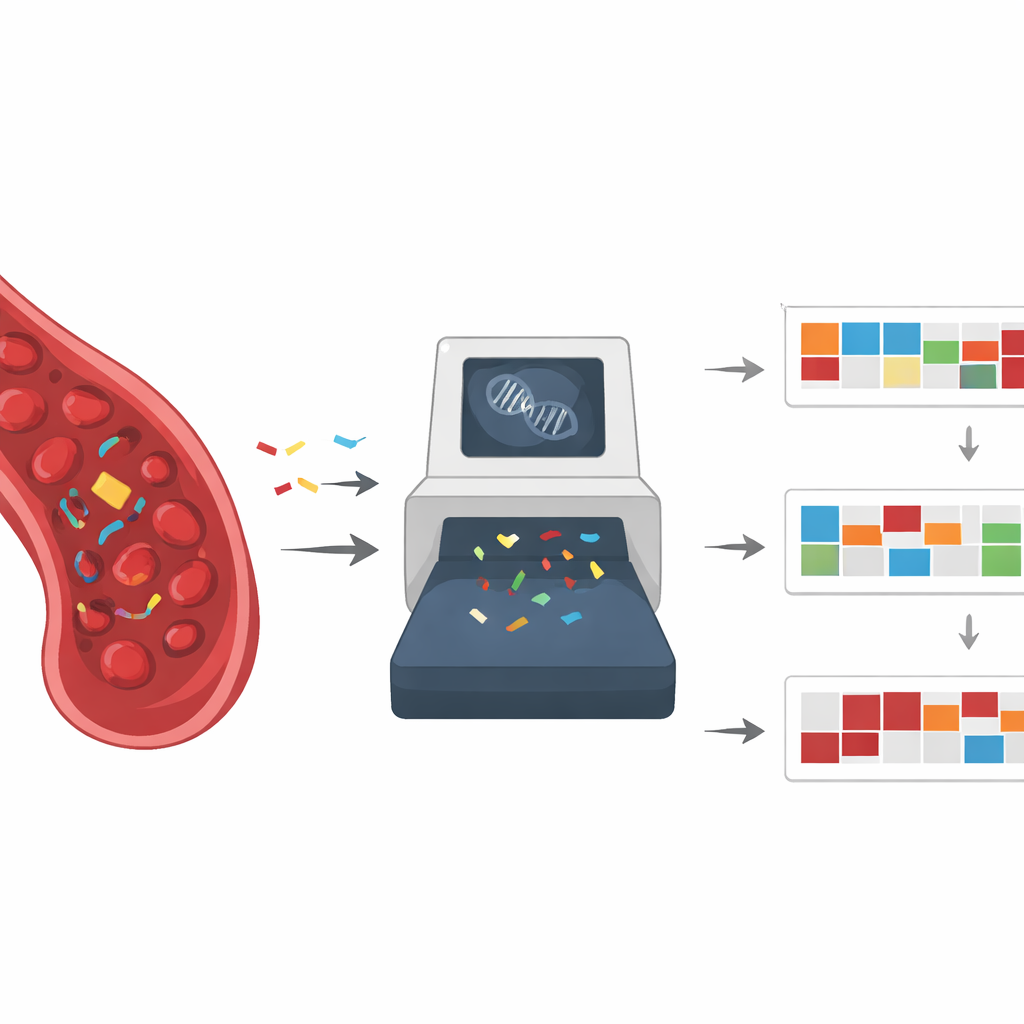
Bloedmonitoring combineren met DNA‑vingerafdrukken
Het kernidee van het artikel is om vloeibare biopsie en mutatie‑handtekeningen in één raamwerk samen te brengen. Door breed, genoomwijd te sequencen op tumor‑DNAfragmenten in het bloed, zouden artsen tegelijkertijd individuele mutaties en de algemene schadepatronen die ze hebben voortgebracht kunnen identificeren. Dit kan vroege detectie van kanker verbeteren, helpen het weefsel van herkomst aan te wijzen in raadselachtige gevallen en behandelkeuzes verfijnen, zelfs wanneer klassieke driver‑mutaties ontbreken. Herhaalde bloedafnames over maanden of jaren kunnen laten zien wanneer een tumor overschakelt op een nieuw mutationeel proces, bijvoorbeeld één dat wordt getriggerd door aanhoudende medicijnblootstelling, wat wijst op opkomende resistentie of het risico op een tweede therapiegerelateerde kanker.
Hobbels op weg naar dagelijks gebruik
Ondanks de belofte kent deze aanpak praktische uitdagingen. Sommige tumoren geven zeer weinig DNA af aan de bloedbaan, waardoor hun signalen moeilijk detecteerbaar zijn. Veel bekende handtekeningen missen nog een duidelijke biologische verklaring, en sommige patronen kunnen deels gevormd worden door technische eigenaardigheden van verschillende sequencingplatforms. Leeftijdsgerelateerde veranderingen in bloedvormende cellen kunnen hun eigen mutaties in het bloed‑DNA introduceren, waardoor het beeld verder verstoord raakt. Huidige methoden om handtekeningen uit plasma te halen vertrouwen vaak op complexe machine‑learningtools die grote trainingsdatasets vereisen en tot nu toe vooral zijn getest in retrospectieve onderzoeksstudies in plaats van in prospectieve klinische proeven.
Wat dit zou kunnen betekenen voor toekomstige kankerzorg
De auteurs concluderen dat het integreren van vloeibare biopsie met mutatie‑handtekeningen uiteindelijk de kankerzorg zou kunnen transformeren van een reeks eenmalige beslissingen naar een continu bijgewerkt proces. In plaats van alleen te vertrouwen op een weefselbiopt dat bij de diagnose is genomen, zouden clinici op termijn routinematig bloedtesten kunnen gebruiken om het zich ontwikkelende "handschrift" van DNA‑schade in de tumor van een patiënt te volgen. Dit zou screening kunnen verscherpen, diagnose verbeteren, therapiekeuze en -volgorde sturen en resistentie detecteren voordat die zichtbaar wordt op scans. Het realiseren van deze visie vereist gestandaardiseerde methoden, rigoureuze validatie en slimmere computermodellen, maar het concept wijst op een toekomst waarin kankerbehandeling niet alleen gericht is op de huidige mutaties van de tumor, maar ook geïnformeerd wordt door de krachten die ze hebben veroorzaakt.
Bronvermelding: Carrasco, R., Dreij, K. Integrating liquid biopsy and mutational signatures to advance precision oncology. npj Precis. Onc. 10, 114 (2026). https://doi.org/10.1038/s41698-026-01337-w
Trefwoorden: vloeibare biopsie, mutatie‑handtekeningen, circulerend DNA, precisie‑oncologie, kanker‑evolutie