Clear Sky Science · nl
Voorspellen van homologe recombinatie‑deficiëntie en behandelresponsen met een op CT gebaseerd foundation‑model: een preklinische studie
Waarom dit belangrijk is voor patiënten en artsen
Behandelingen tegen kanker die DNA beschadigen, zoals bepaalde chemotherapieën en nieuwe gerichte middelen, kunnen buitengewoon effectief zijn bij tumoren waarvan het herstelsysteem al verstoord is. De uitdaging is vast te stellen welke tumoren deze verborgen kwetsbaarheden hebben zonder te vertrouwen op herhaalde, invasieve biopsieën. Deze studie onderzoekt of gangbare medische scans van muizen, geïnterpreteerd door een krachtig kunstmatig‑intelligentie‑model, kunnen onthullen hoe kwetsbaar een tumor is en hoe goed deze zal reageren op een nieuw experimenteel middel.
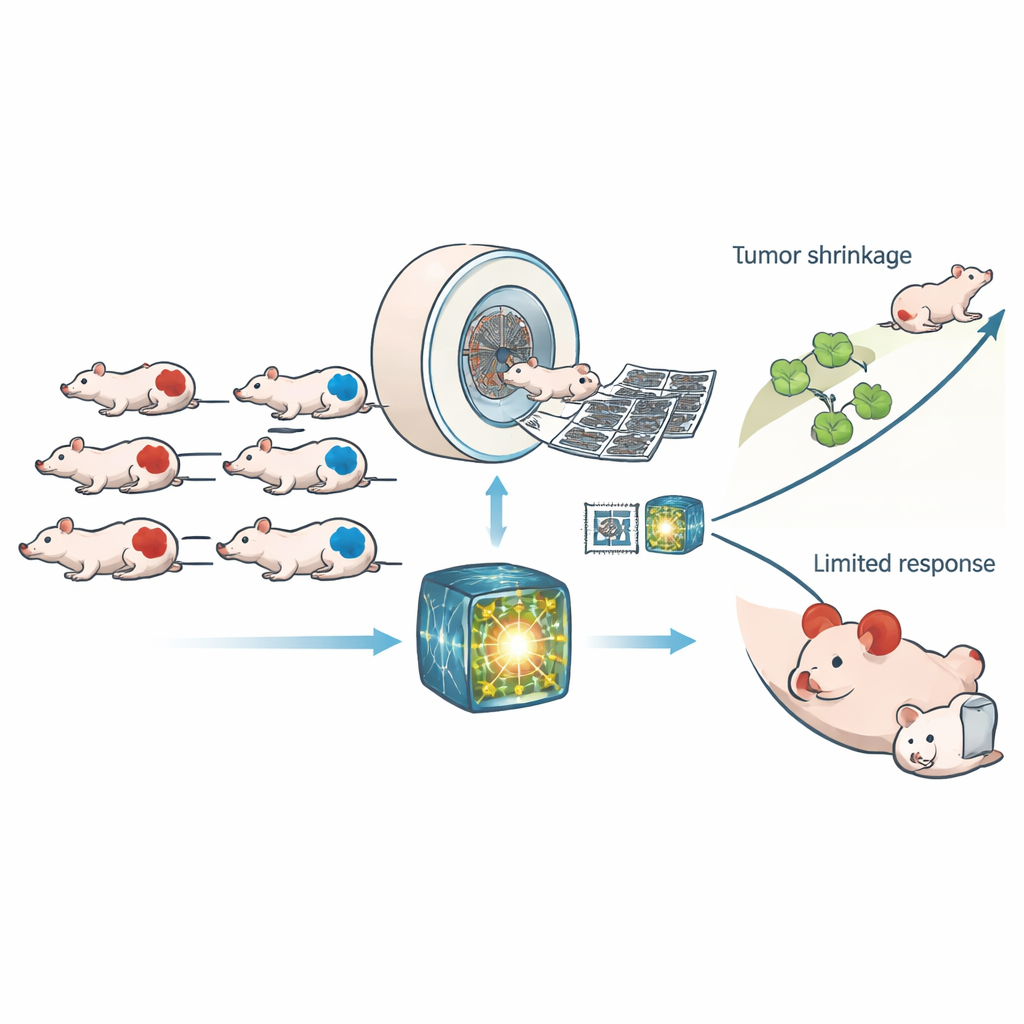
Een verborgen zwakke plek in kankercellen
Veel tumoren dragen defecten in een belangrijke DNA‑herstelroute die homologe recombinatie wordt genoemd. Wanneer deze route faalt, hopen zich beschadigingen in het genetisch materiaal op — een toestand bekend als homologe recombinatie‑deficiëntie, of HRD. HRD kan de kans op kankervorming vergroten, maar het vormt ook een achilleshiel: middelen die DNA verder beschadigen kunnen deze toch al onder druk staande cellen over de rand duwen en ze effectiever doden dan gezonde cellen. Vandaag de dag berust het identificeren van HRD meestal op genetische tests of gespecialiseerde laboratoriumassays die kostbaar en tijdrovend zijn en vaak weefselmonsters vereisen. De auteurs vroegen zich af of beeldvorming — hetzelfde soort driedimensionale röntgenscans dat veel klinieken gebruiken — een snelle, niet‑invasieve blik op HRD kan bieden.
Slimme scans in plaats van meer biopsieën
De onderzoekers werkten met 307 muizen die menselijke tumorgrafts droegen die óf HRD hadden óf normaal waren in hun herstelcapaciteit. Alle dieren ondergingen hoge‑resolutie computertomografie (CT)‑scans voor en na toediening van ofwel een controlemiddel of CP‑506, een experimenteel middel dat actief wordt in zuurstofarme delen van tumoren en DNA‑strengen met elkaar verbindt. In plaats van te vertrouwen op een handjevol handgemaakte beeldmetingen, gebruikte het team een modern "foundation‑model" dat op grote menselijke CT‑datasets is getraind om duizenden subtiele patronen uit elke scan te halen. Een eenvoudige classifier werd vervolgens getraind op deze patronen om te bepalen of een tumor HRD was, en dezelfde geleerde kenmerken werden hergebruikt om te voorspellen hoeveel DNA‑schade en groeivertraging CP‑506 zou veroorzaken.
Hoe goed het beeldvormingsmodel presteerde
Het foundation‑model presteerde duidelijk beter dan zowel traditionele radiomics als een standaard deep‑learning‑netwerk dat vanaf nul was getraind. Op nieuwe testscans wist het HRD‑ van niet‑HRD‑tumoren te onderscheiden met een area under the curve van ongeveer 0,88, een nauwkeurigheidsniveau dat bleef standhouden over verschillende CT‑energieinstellingen. Wanneer beide AI‑benaderingen het eens waren over het tumortype, steeg de prestatie nog verder. De op beelden gebaseerde HRD‑score van het model kwam in meerdere prostaat‑ en colorectale tumorlijnen nauwkeurig overeen met de werkelijke genetische status, hoewel één lijn met afwijkend herstelgedrag moeilijker te classificeren bleef. Belangrijk is dat de CT‑kenmerken die aan HRD gelinkt waren niet slechts statistische artefacten bleken: ze voorspelden ook hoeveel blijvende DNA‑schade CP‑506 48 uur na behandeling veroorzaakte en hoe lang het duurde voordat tumoren in een parallel experiment tot viermaal hun grootte teruggroeiden.
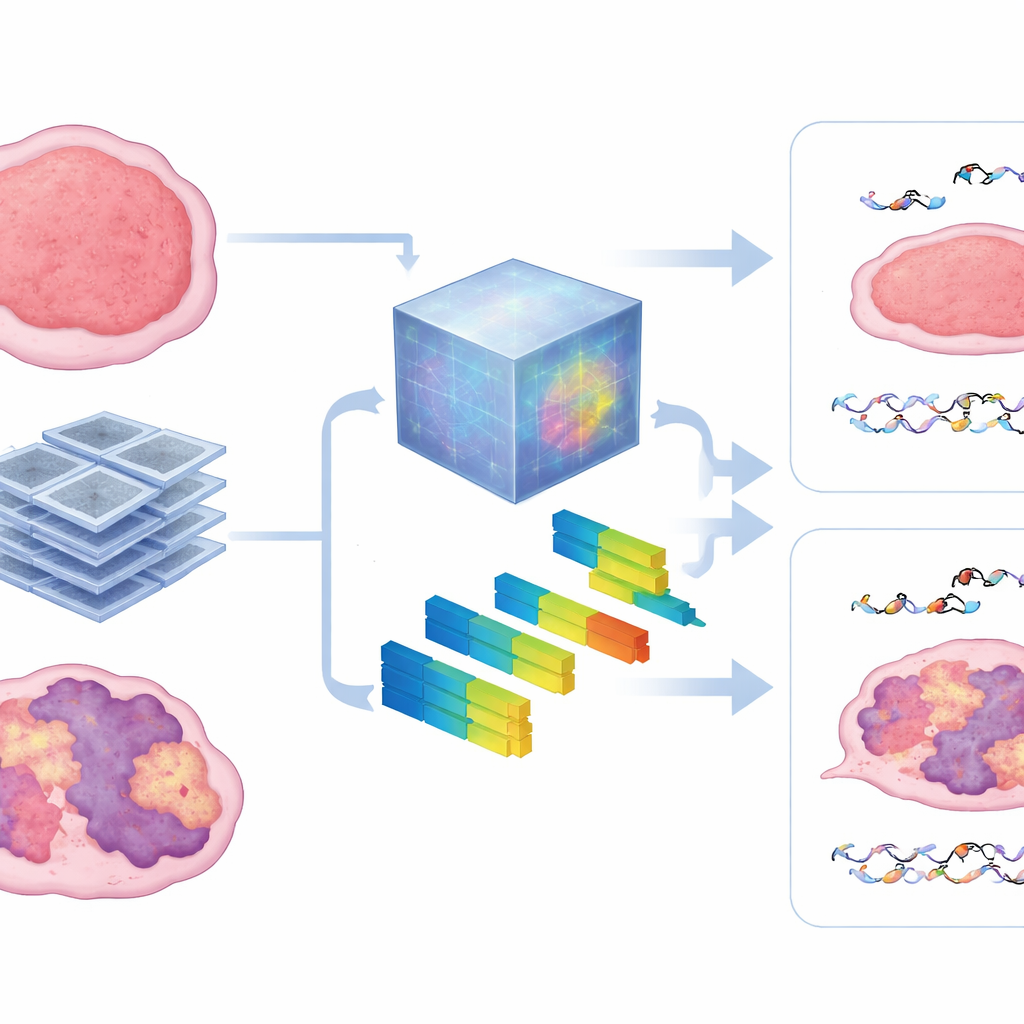
Wat de scans binnin de tumor onthullen
Om in de zwarte doos te kijken vergeleken de auteurs de patronen die het foundation‑model leerde met standaard radiomische kenmerken die beeldtextuur en intensiteit beschrijven. Ze vonden dat het model sterk leunde op maatregelen van heterogeniteit — hoe vlekkerig, grof of onregelmatig de tumor op CT leek. Tumoren met sterkere HRD‑handtekeningen vertoonden doorgaans meer gedesorganiseerde texturen, en dezezelfde kenmerken hielpen zowel microscopische DNA‑schade als macroscopische tumorgroeicontrole te voorspellen. De methode bleef robuust toen minder trainingsdata beschikbaar waren, wat suggereert dat dergelijke voorgetrainde modellen een belangrijke hindernis in dierstudies kunnen overwinnen, waar het verzamelen van grote beelddatasets moeilijk is.
Van muisexperimenten naar toekomstige patiëntenzorg
Dit preklinische werk toont aan dat een enkele CT‑scan, geïnterpreteerd met een krachtig, voorgetraind AI‑model, signalen van defect DNA‑herstel kan vastleggen en kan voorspellen hoe sterk een tumor op een DNA‑schadend middel zal reageren. Voor de niet‑specialist is de conclusie dat standaard ogende scans mogelijk binnenkort een dubbele functie vervullen — het lokaliseren van een tumor en het onthullen van hoe kwetsbaar deze is — zonder extra ingrepen. Voordat dit onderdeel van de routinezorg kan worden, moet de methode in menselijke patiënten worden getest en gevalideerd. Als die inspanningen slagen, zouden CT‑gebaseerde AI‑handtekeningen van HRD artsen kunnen helpen mensen preciezer aan behandelingen zoals CP‑506 en verwante therapieën te koppelen, waardoor uitkomsten verbeteren en anderen worden bespaard van ineffectieve, toxische middelen.
Bronvermelding: Kuang, S., Schuitmaker, L., Wu, M. et al. Predicting homologous recombination deficiency and treatment responses using a computed tomography-based foundation model: a preclinical study. npj Precis. Onc. 10, 121 (2026). https://doi.org/10.1038/s41698-026-01322-3
Trefwoorden: homologe recombinatie‑deficiëntie, kankerbeeldvorming, radiomics, foundation‑modellen, DNA‑schadende therapie