Clear Sky Science · nl
Ontwikkeling en validatie van een op kunstmatige intelligentie gebaseerd model voor het diagnosticeren van goedaardige, grensgeval- en kwaadaardige adnexale massa’s
Waarom dit belangrijk is voor de gezondheid van vrouwen
Ovarium- en andere adnexale massa’s komen vaak voor bij bekken-echografie, maar bepalen welke onschadelijk zijn en welke mogelijk vroegstadiumkanker aanwijzen blijft lastig, zelfs voor specialisten. Deze studie beschrijft een nieuw systeem op basis van kunstmatige intelligentie (AI), Clinical-OMTA, dat echobeelden leest en artsen helpt deze massa’s in drie belangrijke groepen te classificeren — goedaardig, grensgeval en kwaadaardig — zodat vrouwen de juiste behandeling krijgen en onnodige operaties worden vermeden.
Drie soorten gezwellen, drie totaal verschillende keuzes
Niet alle adnexale massa’s zijn gelijk. Goedaardige afwijkingen kunnen vaak worden afgewacht of met een eenvoudige ingreep worden verwijderd. Kwaadaardige tumoren zijn levensbedreigende kanker die specialistische chirurgie en chemotherapie vereisen. Grensgevaltumoren liggen ongemakkelijk tussenin: ze kunnen terugkeren maar treffen vaak jongere vrouwen die hun vruchtbaarheid willen behouden, waardoor chirurgen proberen alleen het noodzakelijke te verwijderen. Helaas kunnen deze drie categorieën er op echografie erg gelijkaardig uitzien. Met name grensgevaltumoren kunnen zowel een onschuldige cyste als een agressieve kanker nabootsen, wat behandelingsbeslissingen stressvol maakt voor patiënten en clinici.
Complexe scans omzetten in duidelijkere antwoorden
Echografie is meestal de eerste en meest beschikbare test voor adnexale massa’s, maar het interpreteren van de korrelige, sterk variabele beelden vergt veel ervaring. Bestaande scoresystemen en risicocalculators, zoals het veelgebruikte ADNEX-model, combineren specifieke echo-eigenschappen met eenvoudige klinische informatie zoals leeftijd en een bloedmarker (CA125), maar ze blijven afhankelijk van menselijke waarnemers die de beelden correct beschrijven. Recente ontwikkelingen in deep learning — een tak van AI die patronen rechtstreeks uit pixels leert — bieden de mogelijkheid om een deel van deze subjectiviteit te omzeilen door computers subtiele beeldsignaturen van verschillende tumorsoorten te laten herkennen.
Een AI-assistent getraind in veel ziekenhuizen
Voortbouwend op eerder werk ontwikkelden de auteurs Clinical-OMTA, een model met twee trajecten dat eerst goedaardig scheidt van niet-goedaardig en vervolgens grensgeval onderscheidt van kwaadaardig. Het systeem verwerkt grijstoon-echobeelden en kan ook leeftijd en CA125-waarden als optionele invoer gebruiken. Om het model te trainen en te testen stelde het team een grote, diverse dataset samen: 2381 vrouwen uit 23 ziekenhuizen in China, gescand met 38 typen echografietoestellen. De meeste gevallen hadden chirurgische bevestiging van de diagnose; een kleinere groep duidelijk goedaardige cysten werd bevestigd door minstens zes maanden echografische follow-up. De data werden verdeeld in trainingssets, interne testsets en twee volledig onafhankelijke externe testcohorten, inclusief zowel stilstaande beelden als korte videosweeps van de ovaria. 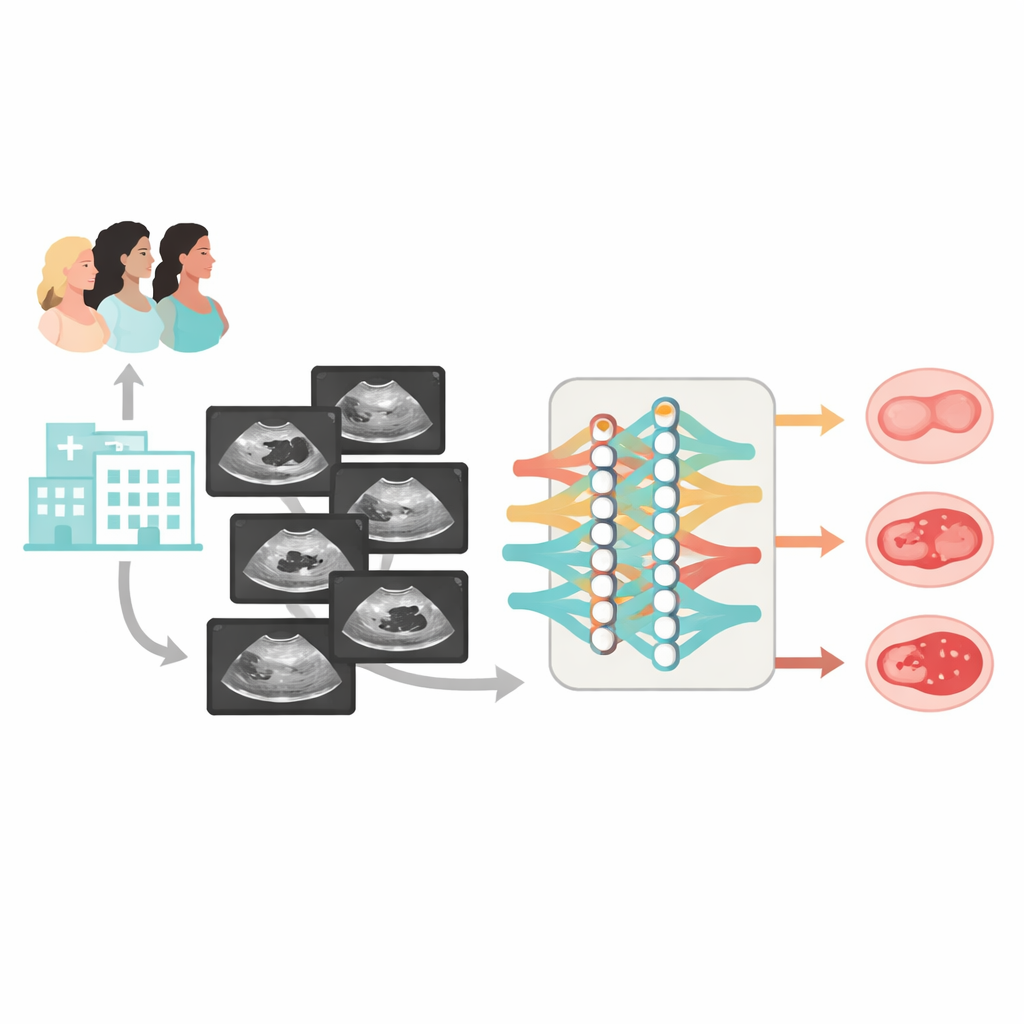
Hoe goed de AI presteerde in de praktijk
Op externe testbeelden onderscheidde Clinical-OMTA goedaardige, grensgeval- en kwaadaardige massa’s correct met een nauwkeurigheid vergelijkbaar met zowel het ADNEX-model als het oordeel van een ervaren echografie-expert. De prestaties waren stabiel over verschillende echografiemerken, scantomstandigheden (via de buik of vagina) en de twee externe ziekenhuizen, wat suggereert dat het model niet overdreven is afgestemd op één specifiek apparaat of centrum. Het systeem werkte ook goed op videoclips, niet alleen op stilstaande beelden. Interessant genoeg verbeterde het toevoegen van leeftijd en CA125 de beslissingen niet boven het gebruik van alleen echobeelden, wat eerdere bevindingen weerspiegelt dat deze bloedmarker weinig toevoegt wanneer hoogwaardige beeldvorming beschikbaar is. 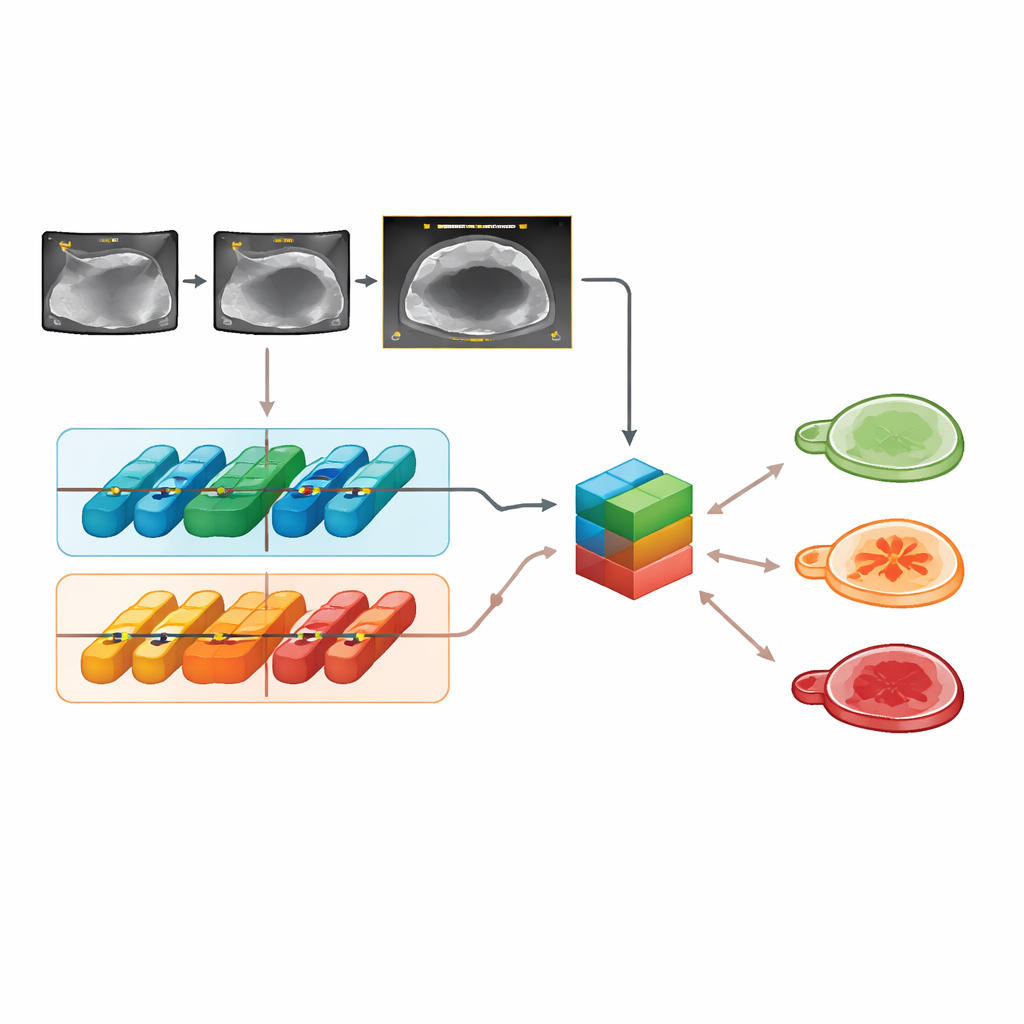
Helpt minder ervaren artsen, en de beperkingen
De onderzoekers vroegen vervolgens 11 radiologen — junior, middelbaar en zeer ervaren — om dezelfde gevallen te classificeren, eerst zonder hulp en daarna met de AI-uitvoer en heatmap-overlay’s die beeldregio’s markeren die het model belangrijk vindt. Met hulp van Clinical-OMTA steeg de nauwkeurigheid van junior-artsen met ongeveer 18–20 procentpunten, en ook de middelbare beoordelaars verbeterden sterk, tot bijna expertprestaties. De overeenstemming tussen beoordelaars, die voorheen slechts van fair tot matig was, nam toe tot zeer hoge niveaus wanneer ze het hulpmiddel gebruikten. Tegelijkertijd merken de auteurs op dat zo’n sterke afstemming mogelijk “automatiseringbias” weerspiegelt, waarbij clinici te veel vertrouwen op de AI, vooral bij de meest vage grensgevalgevallen. De auteurs benadrukken daarom dat heatmaps onderzoeksinstrumenten zijn, geen op zichzelf staande verklaringen, en dat AI-richtlijnen zorgvuldig moeten worden geïntegreerd in klinische opleiding en besluitvorming.
Wat dit betekent voor patiënten
Al met al laat Clinical-OMTA zien dat een AI-systeem dat getraind is op diverse echografiedata de prestaties van experts kan evenaren bij het classificeren van adnexale massa’s in goedaardig, grensgeval en kwaadaardig, terwijl het de vaardigheden en consistentie van minder ervaren radiologen aanzienlijk verbetert. Omdat het werkt op verschillende apparaten en in verschillende centra, zou het model uiteindelijk in scanners kunnen worden ingebouwd of als zelfstandige software kunnen worden gebruikt om artsen te ondersteunen in drukke of ondergefinancierde klinieken. De auteurs waarschuwen dat verdere prospectieve en internationale studies nodig zijn voordat routinematig gebruik verantwoord is, vooral in omgevingen met lagere kwaliteit apparatuur of niet‑gespecialiseerde operators. Toch wijst hun werk op een toekomst waarin meer vrouwen, ongeacht waar ze worden behandeld, kunnen profiteren van interpretaties van ovarium-echografieën op expertsniveau en meer op maat gemaakte, tijdige zorg.
Bronvermelding: Wu, Y., Dai, W., Li, X. et al. Development and validation of an artificial intelligence-based model for diagnosing benign, borderline, and malignant adnexal masses. npj Precis. Onc. 10, 106 (2026). https://doi.org/10.1038/s41698-026-01320-5
Trefwoorden: ovariële echografie, kunstmatige intelligentie, adnexale massa’s, grensgeval ovariële tumoren, klinische besluitvorming ondersteuning