Clear Sky Science · nl
Grootschaalse single-cell analyse en in silico perturbatie onthullen dynamische evolutie van HCC: van initiatie tot therapeutische targeting
Waarom het innerlijk van leverkanker ertoe doet
Hepatocellulair carcinoom, de meest voorkomende vorm van leverkanker, is berucht moeilijk te behandelen. Veel patiënten reageren slecht op de huidige medicijnen en tumoren komen vaak terug of verspreiden zich. Een belangrijke reden is dat elke tumor een chaotische mix is van verschillende cellen die in de loop van de tijd evolueren en voortdurend met hun omgeving communiceren. Deze studie maakt gebruik van krachtige single‑cell en spatiële gen‑leestechnologieën om die evolutie cel voor cel te volgen, van vroegtumorgroei tot gevorderde, therapie‑resistente ziekte, en om kwetsbare punten te identificeren die nieuwe therapieën zouden kunnen benutten.
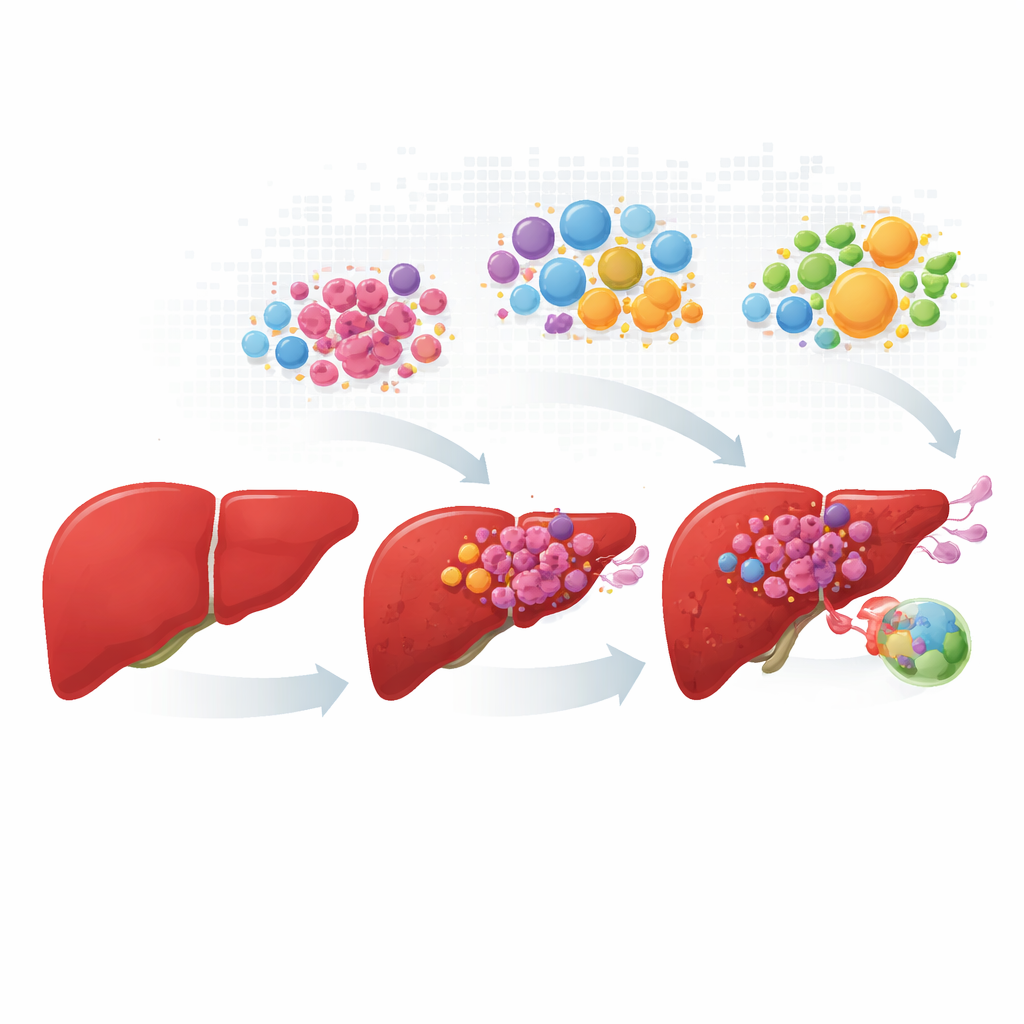
Volgen van kankercellen van vroege verandering tot verspreiding
De onderzoekers brachten gegevens van meer dan honderd patiënten samen en harmoniseerden die, inclusief normaal leverweefsel, primaire tumoren, groei in bloedvaten en lymfekliermetastasen. In plaats van elke tumor als een uniforme massa te beschouwen, profielden ze honderden duizenden individuele cellen en plaatsten ze deze vervolgens op echte weefselsneden. Kankercellen van de lever vielen in vier terugkerende “persoonlijkheden”. Eén groep behield veel normale leverfuncties en metabolische taken; de andere drie toonden stressgedreven groei, hoge activiteit van het MYC-groeipad, of invasief, ontstekingsgekoppeld gedrag. Deze vier toestanden verschenen in verschillende verhoudingen naarmate de ziekte vorderde, waarbij snelgroeiende en invasieve cellen domineerden in laesies van bloedvaten en lymfeklieren.
Vier tumorpersoonlijkheden met verschillende toekomst
De vier kankerceltoestanden waren niet alleen theoretische categorieën; ze correleerden met de uitkomst voor patiënten. Tumoren die rijk waren aan de leverachtige, metabolisch actieve toestand waren verbonden met betere overleving, terwijl tumoren die werden gedomineerd door de andere drie agressieve toestanden doorgaans slechtere uitkomsten hadden. Toch had zelfs de “goede” toestand een kanttekening: die was sterk verrijkt in patiënten die niet profiteerden van het leverkankermedicijn sorafenib, waarschijnlijk omdat deze cellen detox‑mechanismen behouden die medicijnen kunnen inactiveren. Door het herafspelen van hoe cellen langs ontwikkelingspaden bewegen, toonde het team aan dat invasieve, inflammatoire cellen kunnen afsplitsen naar meer gedifferentieerde of juist hoogdelendende toestanden, wat suggereert dat tumorcellen van identiteit kunnen wisselen en zo mogelijk therapieën gericht op één enkele toestand kunnen ontlopen.
De ondersteunende cast: immuun‑ en stromale medeplichtigen
Kankercellen staan er niet alleen voor. De studie toonde gespecialiseerde immuuncellen en steuncellen aan die ofwel tegen tumoren vechten of deze stilletjes helpen. Onder macrofagen, de opruimers en wachters van het weefsel, produceerden sommige typen inflammatoire signalen die anti‑tumorimmuniteit kunnen ondersteunen, terwijl andere metabolisch herschikt waren, behulpzame signalen onderdrukten en de aanleg van bloedvaten en invasie bevorderden. Deze “slechte” macrofagen breidden zich uit in gevorderde monsters. Evenzo vormden bepaalde endotheelcellen die bloedvaten bekleden en fibroblasten die het bindweefsel opbouwen, onderscheidbare subsets die gekoppeld waren aan een slechte prognose. In gevorderde ziekte creëerden een specifieke endotheel‑subtype en twee fibroblasttypen nauw verbonden knooppunten die het extracellulaire geraamte herstructureerden, nieuwe bloedvatvorming aanwakkerden en correleerden met de meest agressieve kankerceltoestanden.
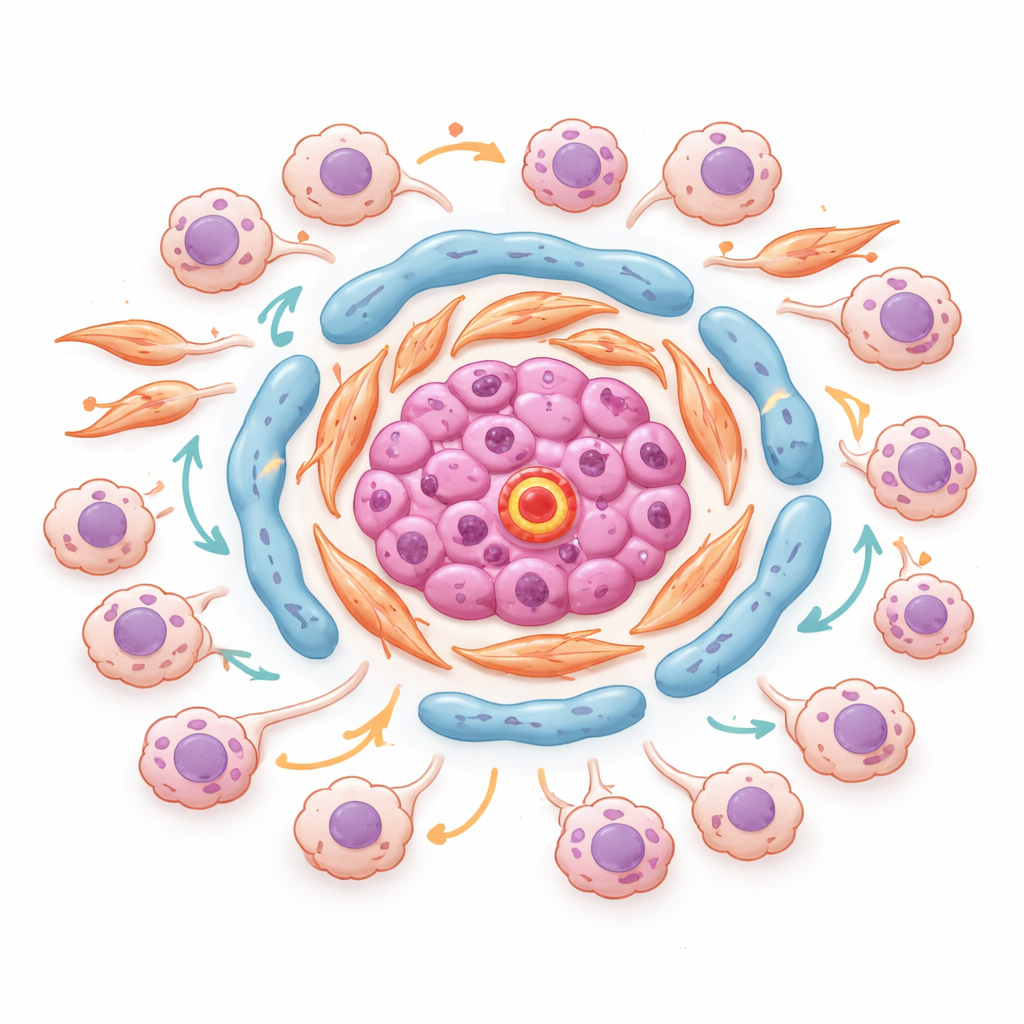
Gevaarlijke buurten binnen tumoren zichtbaar maken
Met spatiële transcriptomica, die genactiviteit meet zonder de kaart van de weefselpositie te verliezen, identificeerden de auteurs georganiseerde “buurten” binnen tumoren. In een representatieve tumor clusteren endotheelcellen rijk aan een molecuul genaamd ESM1 met lipidenhongerige en matrixproducerende fibroblasten in de kern van stromale eilanden. Rond deze kernen stapelden zich stressgedreven en invasieve kankercellen op, in regio’s met sterke TGF‑beta‑ en lage‑zuurstofsignalen. Sleuteltranscriptiefactoren die bepalen hoe cellen op stress en ontsteking reageren, werden gedeeld tussen deze kankertoestanden en waren het meest actief precies daar waar tumorcellen deze stromale knooppunten raakten. Dit suggereert dat specifieke microniches aan de grens tussen tumor en stroma actief kankercellen aanzetten om van toestand te veranderen, agressiever te worden en therapieresistentie te ontwikkelen.
Een gemeenschappelijke zwakke plek vinden voor nieuwe behandelingen
Om van beschrijving naar interventie te gaan, gebruikte het team een machine‑learningmodel getraind op miljoenen cellen om “virtuele knockouts” van genen te simuleren en te voorspellen welke veranderingen schadelijke cellen terug naar gezondere toestanden zouden kunnen duwen. Door macrofagen, endotheelcellen en kankercellen te vergelijken, vonden ze een kleine set genen waarvan het verwijderen hielp om alle drie te normaliseren. HSP90B1 sprong eruit: kankercellijnen zijn er sterk afhankelijk van, het wordt overgeproduceerd in levertumoren—met name in diegenen die resistent zijn tegen gerichte middelen en immunotherapie—en hoge niveaus voorspellen een slechtere overleving. HSP90B1 codeert voor een stressbehandelende chaperonne in de eiwitvouwwerkplaats van de cel die veel oppervlakte‑receptoren en signaalroutes ondersteunt. Omdat selectieve middelen tegen deze chaperonne al bestaan en ook de immuunomgeving kunnen herschikken, stelt de studie HSP90B1 voor als een veelbelovend doel om resistentie te overwinnen, vooral in combinatie met bestaande leverkankerbehandelingen.
Wat dit betekent voor patiënten en therapieën
Alles bij elkaar laat dit werk zien dat leverkanker geen eenduidige ziekte is maar een dynamisch ecosysteem van celtoestanden en niches die verschuiven naarmate de tumor groeit en zich verspreidt. Door specifieke kankercelpersoonlijkheden, ondersteunende cellen en ruimtelijke buurten te koppelen aan patiëntuitkomst en medicijnrespons, biedt de studie een routekaart voor preciezere behandeling: therapieën afstemmen op dominante celtoestanden, stromale knooppunten verstoren die agressief gedrag cultiveren, en gedeelde afhankelijkheden zoals HSP90B1 richten waarop veel tumor‑ en micro‑omgevingscellen vertrouwen. Hoewel verder laboratorium‑ en klinisch onderzoek nodig is, levert de atlas die dit team bouwde een gedetailleerd blauwdruk om de interne complexiteit van de tumor van een obstakel om te buigen naar een kans voor slimmere, duurzamere leverkankertherapieën.
Bronvermelding: Xia, P., Shuang, S., Fu, D. et al. Large-scale single-cell analysis and in silico perturbation reveal dynamic evolution of HCC: from initiation to therapeutic targeting. npj Precis. Onc. 10, 100 (2026). https://doi.org/10.1038/s41698-026-01307-2
Trefwoorden: hepatocellulair carcinoom, single-cell analyse, tumor micro‑omgeving, spatiële transcriptomica, HSP90B1