Clear Sky Science · nl
Vertaling van ruimtelijke transcriptomische signaturen in adenosquameuze carcinoom naar bulk prognostische biomarkers bij longadenocarcinoom: een bottom-up benadering
Verborgen waarschuwingssignalen binnen longtumoren
Longkanker blijft een van de dodelijkste vormen van kanker, deels omdat tumoren mengsels zijn van veel verschillende celtypen. Sommige van deze cellen kunnen stilletjes de ziekte aanstuwen naar een agressiever beloop of resistentie tegen behandeling, maar ze zijn te zeldzaam of te vermengd om met standaard laboratoriumtesten te worden gezien. Deze studie laat zien hoe uiterst gedetailleerde "kaarten" van genactiviteit binnen tumoren deze verborgen boosdoeners kunnen onthullen en omzetten in eenvoudige laboratoriummarkers die helpen voorspellen hoe patiënten met longkanker zullen reageren.
Nauwkeuriger kijken naar een zeldzame, gemengde tumor
De onderzoekers richtten zich op een zeldzame longkanker genaamd adenosquameus carcinoom, die twee hoofdtypen niet-kleincellige longkanker in één massa combineert: klierachtige adenocarcinoom en plattere, huidachtige squameuze carcinoom. Omdat beide componenten naast elkaar in dezelfde tumor groeien, is deze kanker een ideaal model om te bestuderen hoe tumorcellen van identiteit kunnen wisselen naarmate ze kwaadaardiger worden. Met een afbeeldingsmethode genaamd ruimtelijke transcriptomica maten de onderzoekers welke genen in duizenden individuele cellen actief waren, terwijl hun exacte positie in dunne tumorplakjes behouden bleef. Tegelijkertijd gebruikten ze standaardkleuringstesten voor twee veelgebruikte diagnostische markers, TTF‑1 (voor adenocarcinoom) en p40 (voor squameuze cellen), om hun hightech-kaarten te verankeren in de routinematige pathologie. 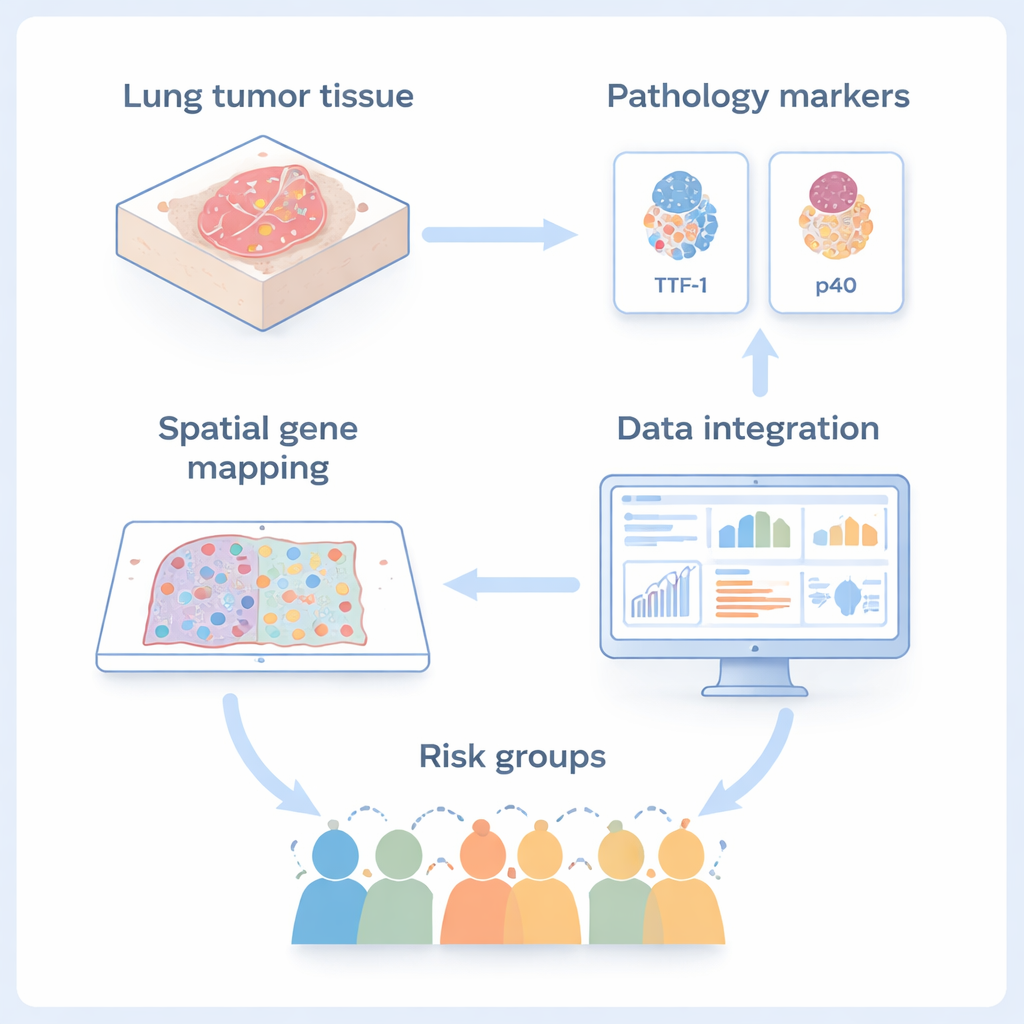
Kleurcoderen van tumorcellen om afwijkende cellen te vinden
Het simpel groeperen van cellen op basis van genpatronen was niet voldoende, omdat normale longcellen en tumorcellen soms vergelijkbaar kunnen lijken in genaflezingen. Om het beeld te verscherpen, gebruikte het team een visualisatietruc die ze RGB‑UMAP noemen. In deze aanpak wordt het algemene genactiviteitspatroon van elke cel gecomprimeerd tot drie getallen en vertaald naar een rood‑groen‑blauwe kleur. Cellen die zich vergelijkbaar gedragen verschijnen in vergelijkbare kleuren wanneer ze teruggeprojecteerd worden op de weefselafbeelding. Dit stelde de wetenschappers in staat om groepjes normale cellen te herkennen die zich tussen tumorcellen verborgen, en deze uit hun analyse te verwijderen, zodat ze echt kankercellen bestudeerden in plaats van gezonde omstanders.
Het vinden van een hybride celtoestand en een sleutelpoort voor suiker
Nadat ze normale cellen hadden weggefilterd, zochten de onderzoekers naar genen die sterk en consequent alleen in tumorcellen actief waren. Daaronder ontdekten ze een groep tumorcellen die zowel TTF‑1 als p40 negatief was maar een gemengd genpatroon vertoonde, met kenmerken van zowel adenocarcinoom als squameus carcinoom. Eén gen stak hierbij uit: SLC2A1, dat een eiwit maakt dat bekendstaat als GLUT1. GLUT1 fungeert als een poort waardoor glucose, de brandstof van de cel, uit de bloedbaan kan binnenkomen. In meerdere tumoren was SLC2A1 overvloedig aanwezig in squameuze gebieden en in de TTF‑1/p40‑negatieve zones, maar vrijwel afwezig in normaal longweefsel. Het team bevestigde dit patroon in meerdere patiëntmonsters, wat erop wijst dat hoge SLC2A1 een squameus-achtig, metabolisch actieve subpopulatie van kankercellen markeert.
Van microscopische kaarten naar patiëntuitkomsten
Om te testen of deze microscopische bevinding relevant is voor echte patiënten, gebruikten de wetenschappers grote bestaande datasets waarin bulk genactiviteit (gemiddeld over gehele tumorstalen), DNA-veranderingen en klinische uitkomsten beschikbaar waren voor honderden mensen met longadenocarcinoom. Toen ze deze patiënten indeelden op basis van SLC2A1-niveaus in hun tumoren, hadden degenen met hogere SLC2A1 meer genveranderingen die typisch zijn voor squameuze kankers, een sterkere signatuur van suiker-hongerige stofwisseling en significant slechtere overleving. Deze koppeling bleef bestaan na correctie voor factoren zoals leeftijd, stadium, rookgeschiedenis en geslacht, en werd bevestigd in een onafhankelijke openbare dataset. Ter vergelijking: in zuivere squameuze tumoren splitste SLC2A1-niveau de patiënten niet duidelijk op uitkomst, wat benadrukt dat de marker vooral informatief is binnen adenocarcinoom. 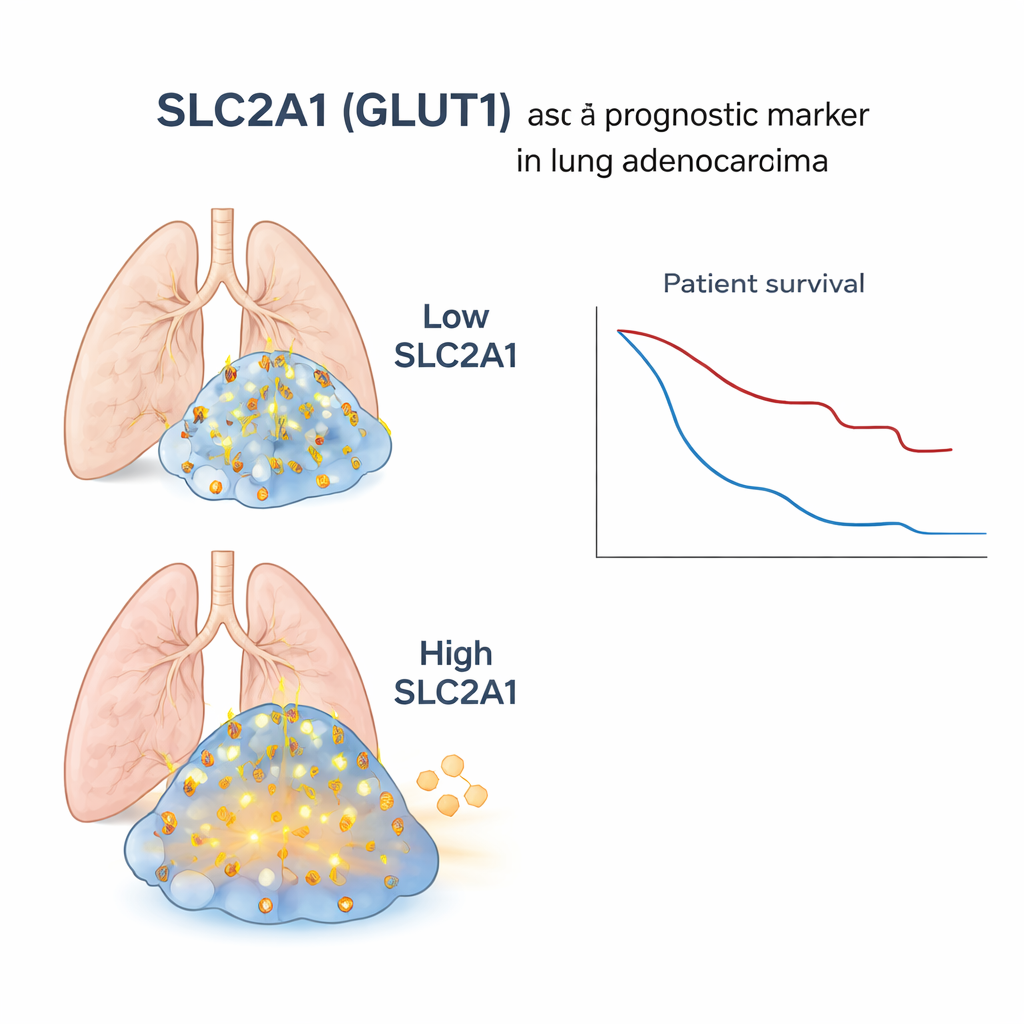
Wat dit betekent voor patiënten met longadenocarcinoom
Voor niet‑specialisten is de kernboodschap dat binnen wat onder de microscoop als één type longkanker lijkt, verborgen groepjes cellen kunnen zitten die zich meer gedragen als een ander, agressiever type. Door gebruik te maken van hoogresolutie genkaarten identificeerden de onderzoekers SLC2A1 als een eenvoudige, meetbare aanwijzing voor deze squameus‑achtige, brandstof‑hongerige cellen die in adenocarcinomen schuilgaan. Hoge niveaus van dit gen in standaard weefselmonsters wijzen op patiënten wiens tumoren waarschijnlijker agressief zullen zijn en die mogelijk intensiever gevolgd moeten worden of andere behandelstrategieën behoeven. Meer algemeen laat de studie een "bottom‑up" route zien — van individuele cellen in een weefselplaatje naar testen op gehele tumoren — die op andere kankers toepasbaar kan zijn om gevaarlijke celtoestanden te onthullen die routinemethoden momenteel missen.
Bronvermelding: Hatakeyama, K., Kawata, T., Muramatsu, K. et al. Translating spatial transcriptomic signatures in adenosquamous carcinoma into bulk prognostic biomarkers in lung adenocarcinoma: a bottom-up approach. npj Precis. Onc. 10, 77 (2026). https://doi.org/10.1038/s41698-026-01297-1
Trefwoorden: longadenocarcinoom, ruimtelijke transcriptomica, adenosquameus carcinoom, SLC2A1 GLUT1, kanker biomerkers