Clear Sky Science · nl
AI-gestuurd virtueel screeningsplatform identificeert nieuwe NSUN2-remmerkandidaten voor gerichte kankertherapie: een computationele benadering voor geneesmiddelontdekking
Nieuwe manieren om hardnekkige kankers te slim af te zijn
Veel kankers worden dodelijk, niet alleen omdat ze ontstaan, maar omdat ze leren onze beste medicijnen te ontwijken. Deze studie onderzoekt een veelbelovende nieuwe manier om een belangrijke helper van tumorgroei uit te schakelen, door kunstmatige intelligentie te gebruiken om meer dan honderd miljoen potentiële medicijnen op een computer te doorzoeken voordat er iets in een proefbuis wordt gemengd.
Een verborgen schakel in kankercellen
Diep in onze cellen werkt een enzym genaamd NSUN2 als een chemische markeerstift voor RNA, het molecuul dat helpt genen in eiwitten om te zetten. Door kleine chemische markeringen aan RNA toe te voegen, kan NSUN2 groeigerelateerde boodschappen stabieler en makkelijker leesbaar maken. Veel tumoren, waaronder long-, maag-, alvleesklier- en borstkanker, zetten de NSUN2-niveaus hoger, wat hun vermogen om te delen, uit te zaaien en resistent te worden tegen gerichte middelen vergroot. Ondanks het belang ervan bestaan er echter maar weinig kandidaat-geneesmiddelen die NSUN2 veilig kunnen dempen, vooral reversibele middelen die het enzym niet permanent beschadigen.
AI laten zoeken in een zee van moleculen
Traditionele geneesmiddelontdekking zou moeite hebben om miljoenen moleculen tegen NSUN2 in het laboratorium te testen, omdat elk experiment complexe mengsels van RNA en hulpstoffen vereist. In plaats daarvan bouwden de onderzoekers een volledig digitale pijplijn. Ze begonnen met een voorspelde driedimensionale vorm van menselijke NSUN2 gegenereerd door AlphaFold, een AI-systeem dat de structuurvoorspelling heeft getransformeerd. Om ervoor te zorgen dat dit model betrouwbaar was, alignerden ze het met een nauw verwant enzym waarvan de structuur bekend is uit röntgenstudies. De kritieke holte waar NSUN2 zijn natuurlijke hulpstof bindt bleek sterk geconserveerd te zijn, wat het team vertrouwen gaf dat virtueel dokken van potentiële geneesmiddelen in deze site zinvol zou zijn.
Van honderden miljoenen naar een handvol
Met de doelholte vastgesteld wendde het team zich tot een enorme openbare database van koopbare moleculen. Ze dokten eerst een trainingsset verbindingen in de NSUN2-holte en gebruikten de resulterende scores om een machine-learningmodel te leren welke vormen het meest veelbelovend waren. Dat model screende vervolgens snel ongeveer 350 miljoen moleculen en markeerde ruwweg 101 miljoen als waarschijnlijke “hits.” Om het veld verder te verkleinen, werden de bovenste fracties opnieuw gedokt met zorgvuldiger berekeningen, en alleen de beste 12.000 met sterke voorspelde binding werden behouden. Deze werden vervolgens door een batterij computergestuurde veiligheidstests gehaald die inschatten hoe het lichaam elk kandidaat-molecuul zou kunnen opnemen, distribueren, afbreken en verdragen. Na deze filters bleven slechts 34 moleculen over die zowel potent als geneesmiddelachtig leken.
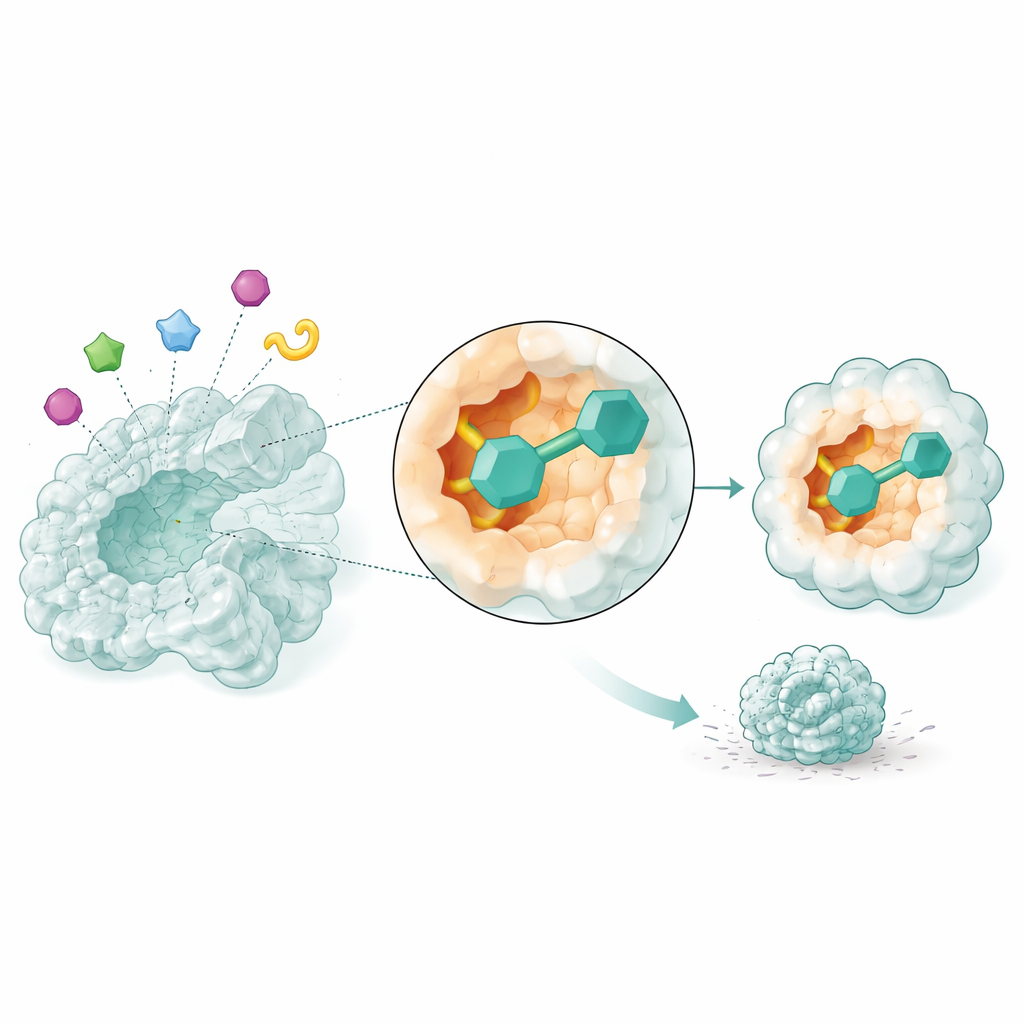
Kijkend naar kandidaat-geneesmiddelen in beweging
Statische snapshots zijn niet voldoende om te weten of een geneesmiddel zijn doel daadwerkelijk vasthoudt. De onderzoekers gebruikten daarom moleculaire dynamicasimulaties, die modelleren hoe atomen in de tijd bewegen, om de meest veelbelovende drie kandidaten gedurende 50 miljardsten van een seconde te observeren terwijl ze met NSUN2 interageerden. Twee verbindingen, alleen geïdentificeerd met hun databankcodes, vormden bijzonder stabiele complexen: de enzymstructuur bleef compact, zijn sleutelregio’s bleven stabiel in plaats van slap, en de kleine moleculen hielden een nauwe pasvorm in de holte terwijl ze blijvende contacten vormden. Deze simulaties suggereren dat de twee verbindingen NSUN2’s activiteit betrouwbaar in echte cellen zouden kunnen blokkeren.
Wat dit zou kunnen betekenen voor toekomstige behandelingen
Hoewel alle resultaten in dit werk uit berekeningen voortkomen en nog in het laboratorium bewezen moeten worden, levert de studie een korte lijst van realistische beginpunten voor nieuwe NSUN2-blokkerende geneesmiddelen. Omdat NSUN2 kankercellen helpt groeien en overlevingssignalen te stabiliseren, zouden zulke medicijnen tumoren kunnen verzwakken en mogelijk opnieuw gevoelig maken voor bestaande gerichte therapieën, met name bij longkankers die resistent zijn geworden. Even belangrijk is dat de studie een algemeen recept laat zien om AI en op fysica gebaseerde modellering te gebruiken om enorme chemische ruimtes snel en goedkoop te verkennen, en zo een krachtige route naar de volgende generatie precisiekankerbehandelingen biedt.
Bronvermelding: Yu, S., Peng, Q., Wei, W. et al. AI-driven virtual screening platform identifies novel NSUN2 inhibitor candidates for targeted cancer therapy: a computational drug discovery approach. npj Precis. Onc. 10, 98 (2026). https://doi.org/10.1038/s41698-026-01296-2
Trefwoorden: NSUN2, epitranscriptomica, AI virtuele screening, ontdekking van kankermedicijnen, RNA-methylatie