Clear Sky Science · nl
Metastatische progressie van feochromocytoom en paraganglioom verloopt via parallelle evolutie
Waarom deze zeldzame tumoren ertoe doen
Feochromocytoom en paraganglioom zijn zeldzame tumoren die ontstaan uit hormoonproducerende zenuwcellen diep in het lichaam. Ze kunnen ernstige bloeddrukpieken en andere gevaarlijke symptomen veroorzaken, vaak bij relatief jonge volwassenen. Tot een kwart van de patiënten ontwikkelt uiteindelijk uitzaaiingen naar afstandsorganen, maar er zijn weinig effectieve geneesmiddelen beschikbaar. Deze studie stelt een eenvoudige maar cruciale vraag: hoe en wanneer worden deze tumoren gemetastaseerd — en kan hun DNA nieuwe behandelingsmogelijkheden onthullen?
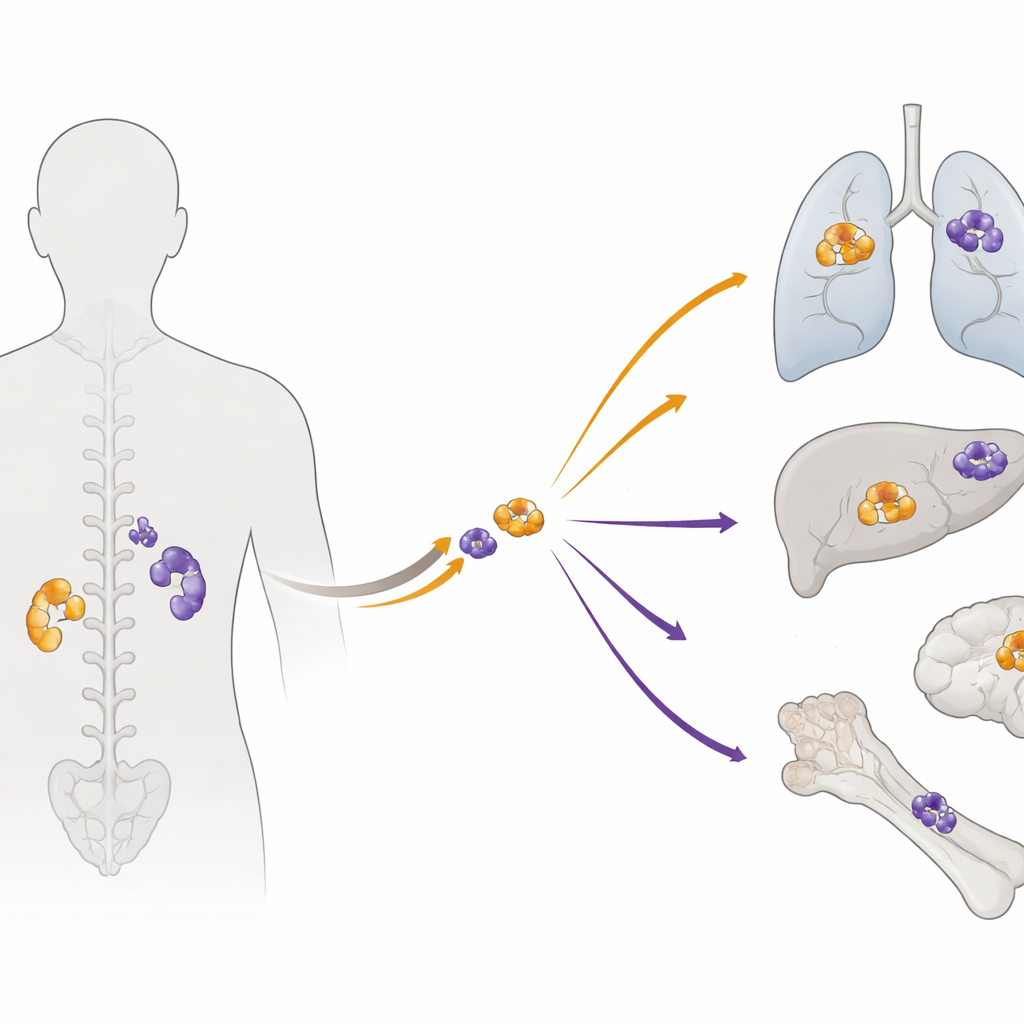
Het spoor van kanker‑DNA volgen
De onderzoekers analyseerden gepaarde tumormonsters van 27 mensen bij wie de ziekte al was uitgezaaid. Voor veel patiënten hadden ze DNA zowel van de oorspronkelijke tumor als van latere metastasen, plus normaal weefsel voor vergelijking. Met whole‑exome sequencing — een techniek die alle eiwitcoderende genen uitleest — brachten ze duizenden mutaties en grotere DNA‑winsten en -verliezen in kaart. Vervolgens pasten ze statistische hulpmiddelen toe om waarschijnlijke “driver”-veranderingen die kanker voortstuwen te onderscheiden van achtergrondruis en om de volgorde te reconstrueren waarin belangrijke genetische gebeurtenissen plaatsvonden.
Verborgen zwakke plekken in tumordefenses
Een van de opvallende patronen was de hoge frequentie van beschadigingen in genen die helpen DNA te verpakken en te repareren wanneer het breekt. Bij bijna 40% van de tumoren werden schadelijke veranderingen gevonden in chromatin‑remodelleringsgenen of genen voor DNA‑schadeherstel. Hiertoe behoorden ATRX en bekende reparatiegenen zoals BRCA1, BRCA2, ATM en ATR. Veel patiënten hadden ook erfelijke mutaties in SDHx‑genen, die al aan deze tumoren gekoppeld zijn. De combinatie van foutieve stofwisseling door SDHx en aangetast DNA‑herstel suggereert dat sommige tumoren buitengewoon kwetsbaar kunnen zijn voor middelen die zulke zwaktes uitbuiten, waaronder PARP-remmers en andere therapieën die de DNA‑herstelmachinerie aantasten.
Vroege ontsnapping en lange, stille groei
Toen het team elke primaire tumor met zijn metastasen vergeleek, vonden ze verrassend weinig overlap in de fijnmazigere mutaties. Gemiddeld was minder dan 10% van de potentieel belangrijke veranderingen gedeeld. Grondige controles bevestigden echter dat elk paar daadwerkelijk van dezelfde patiënt afkomstig was. Met behulp van “moleculaire klok”-methoden, die timing afleiden uit het aantal opgelopen mutaties, schatten de auteurs dat de stammende cellen van metastasen vaak zeer vroeg afsplitsten — ruwweg 18 jaar voordat de primaire tumor werd gediagnosticeerd. In veel gevallen vond de feitelijke uitzaaiing naar verre locaties meer dan een decennium plaats voordat artsen de oorspronkelijke massa ontdekten. Grootschalige DNA‑veranderingen, zoals wins en verliezen van hele chromosomen, deden zich meestal vroeg voor en waren gedeeld, terwijl de meeste kleinere mutaties later en onafhankelijk op iedere locatie ontstonden.
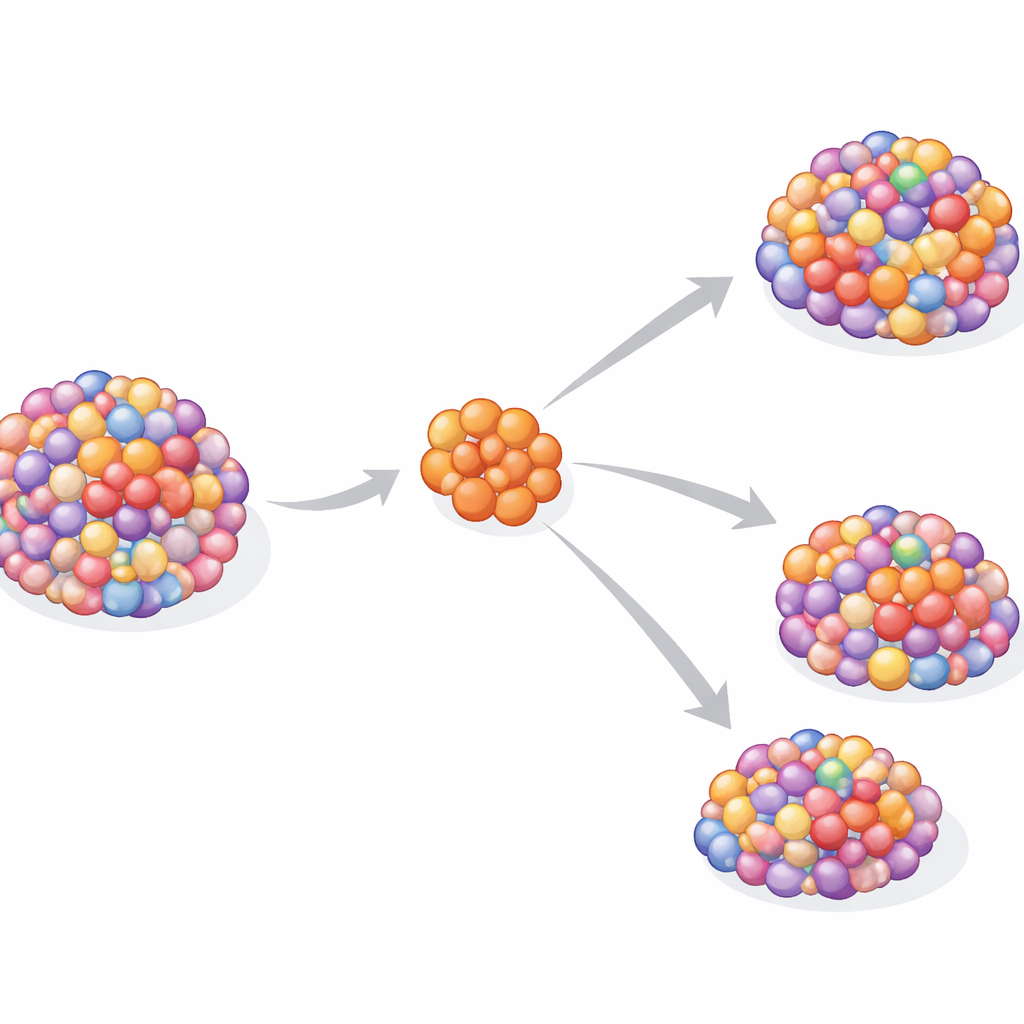
Één kloon, vele afzonderlijke reizen
Ondanks de genetische diversiteit suggereren de gegevens dat elke metastase meestal begon vanuit een enkele voorouderlijke cel en niet uit een mengsel. Dit patroon van “monoklonale zaaiing” staat in contrast met sommige andere kankers, waarbij meerdere takken van de primaire tumor gezamenlijk nieuwe locaties kunnen koloniseren. Hier lijkt een eenzame afsplitsing de vroege tumor te verlaten, zich elders in het lichaam te vestigen en vervolgens jarenlang grotendeels op zichzelf te evolueren. Het resultaat is parallelle evolutie: de primaire en metastatische tumoren delen vroege structurele DNA‑veranderingen maar wijken daarna uiteen, waarbij elk in de loop van de tijd zijn eigen unieke reeks mutaties en mogelijke gevoeligheden voor geneesmiddelen verwerft.
Wat dit betekent voor patiënten en behandeling
Voor mensen met feochromocytoom of paraganglioom schetst dit werk een somber maar informatief beeld. Metastasen zijn niet simpelweg late uitlopers van een gevorderde primaire tumor; het zijn vroege reizigers die jarenlang stil kunnen groeien voordat iemand weet dat ze bestaan. Tegelijk onthult de studie terugkerende beschadigingen in DNA‑herstel- en chromatinagerelateerde genen, wat wijst op nieuwe therapeutische invalshoeken. Samen pleiten deze bevindingen voor nauwere genetische bestudering van metastatische laesies zelf en ondersteunen ze klinische proeven met geneesmiddelen die DNA‑herstel en verwante paden targeten. Begrijpen wanneer en hoe deze tumoren zich verspreiden kan uiteindelijk leiden tot vroegere detectie en meer precieze, gepersonaliseerde behandeling voor patiënten.
Bronvermelding: Pregnall, A.M., Wubbenhorst, B., D’Andrea, K. et al. Metastatic progression of pheochromocytoma and paraganglioma occurs via parallel evolution. npj Precis. Onc. 10, 101 (2026). https://doi.org/10.1038/s41698-026-01291-7
Trefwoorden: feochromocytoom, paraganglioom, metastase, tumorevolutie, DNA-reparatie