Clear Sky Science · nl
Verlies van microRNA-29b bevordert DNMT3b-gemedieerde vermindering van STING en verzwakt radiotherapie-geïnduceerde antitumorimmuniteit bij KRAS-gemuteerde colorectale kanker
Waarom dit onderzoek ertoe doet
Voor veel mensen met rectale en colonkanker is bestraling een belangrijk onderdeel van de behandeling vóór de operatie. Toch krimpen sommige tumoren nauwelijks en keert de kanker vaak terug of geeft uitzaaiingen. Deze studie onderzoekt een veelvoorkomende genetische verandering in colorectale kanker — een KRAS-mutatie — om te verklaren waarom deze tumoren vaak resistent zijn tegen radiotherapie en nieuwe immunotherapieën, en stelt een strategie voor om het immuunsysteem van het lichaam opnieuw tegen hen in stelling te brengen.
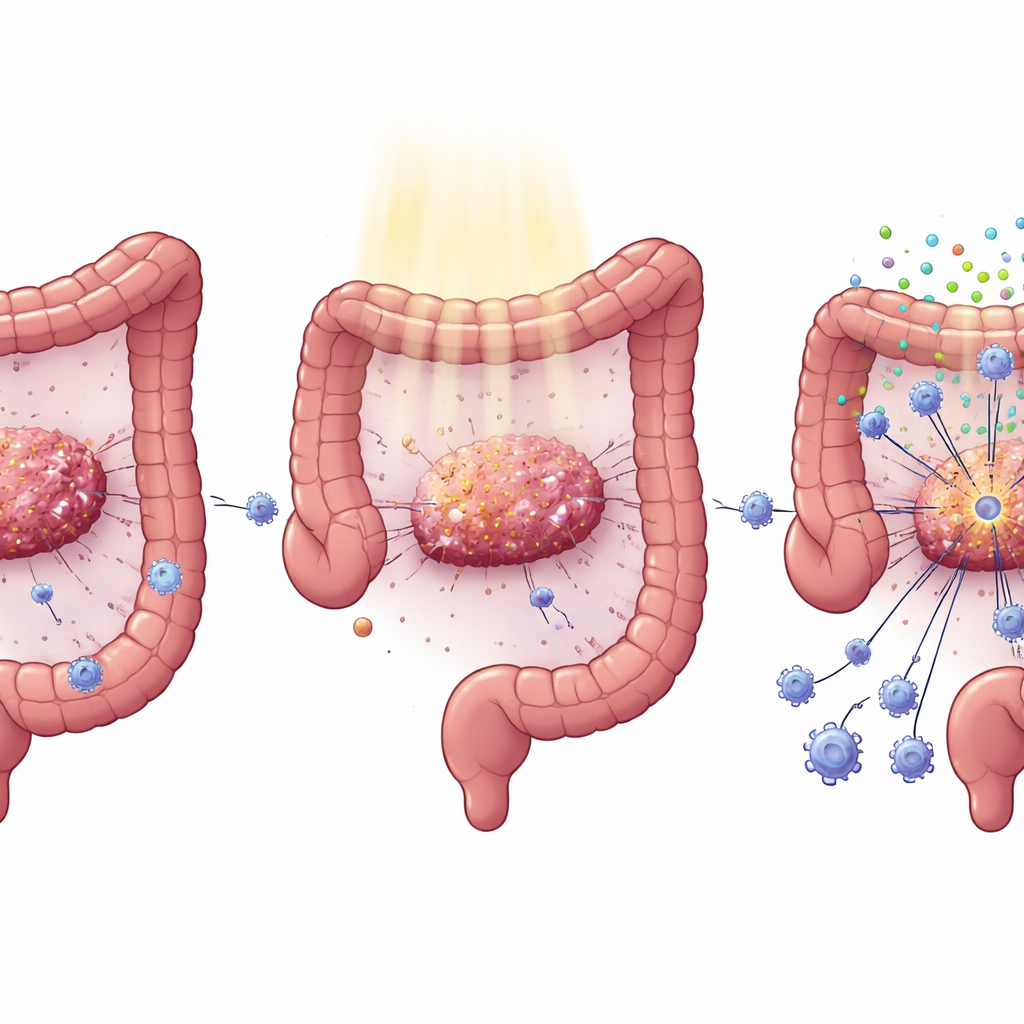
Een veelvoorkomende mutatie die tumoren verbergt voor immuunaanval
Colorectale kanker draagt vaak mutaties in het KRAS-gen, een belangrijke motor van tumorgroei en -uitzaaiing. Klinische waarnemingen toonden al aan dat KRAS-gemuteerde tumoren doorgaans slecht reageren op zowel gerichte geneesmiddelen als radiotherapie. Door grote kankerdatabases te analyseren en patiëntmonsters te bestuderen, vonden de auteurs dat tumoren met mutant KRAS minder kanker-dodende CD8-T-cellen en zwakkere activiteit van interferon-gestuurde immuursignalen vertonen. Bij patiënten die standaard chemoradiotherapie kregen vóór chirurgie van rectumkanker, vonden degenen met normale KRAS veel meer CD8-T-cellen in hun tumoren na behandeling dan patiënten met KRAS-mutaties, wat hun betere uitkomsten helpt verklaren.
Het ontbrekende alarmsysteem binnen kankercellen
Bestraling beschadigt niet alleen het tumor-DNA; het kan ook functioneren als een flare, waardoor kankercellen DNA-fragmenten vrijgeven die een intern alarmsignaal activeren dat bekend staat als cGAS–STING. Wanneer STING actief is, produceren cellen type I interferonen en andere signalen die immuuncellen aantrekken en activeren, waaronder T-cellen en dendritische cellen. De onderzoekers toonden aan dat dit alarmsysteem bij colorectale kankercellen die zodanig zijn geconstrueerd dat ze mutant KRAS dragen, is afgezwakt: na bestraling produceerden deze cellen veel minder interferon en aanverwante moleculen. Bij muismodellen herstelde het uitschakelen van KRAS in tumoren de STING-niveaus, versterkte interferonsignalen en leidde tot meer CD4- en CD8-T-cellen, minder regulatoire T-cellen en betere tumorcontrole — niet alleen in bestraalde tumoren maar ook in verre, niet-bestraalde ‘abscopale’ tumoren.
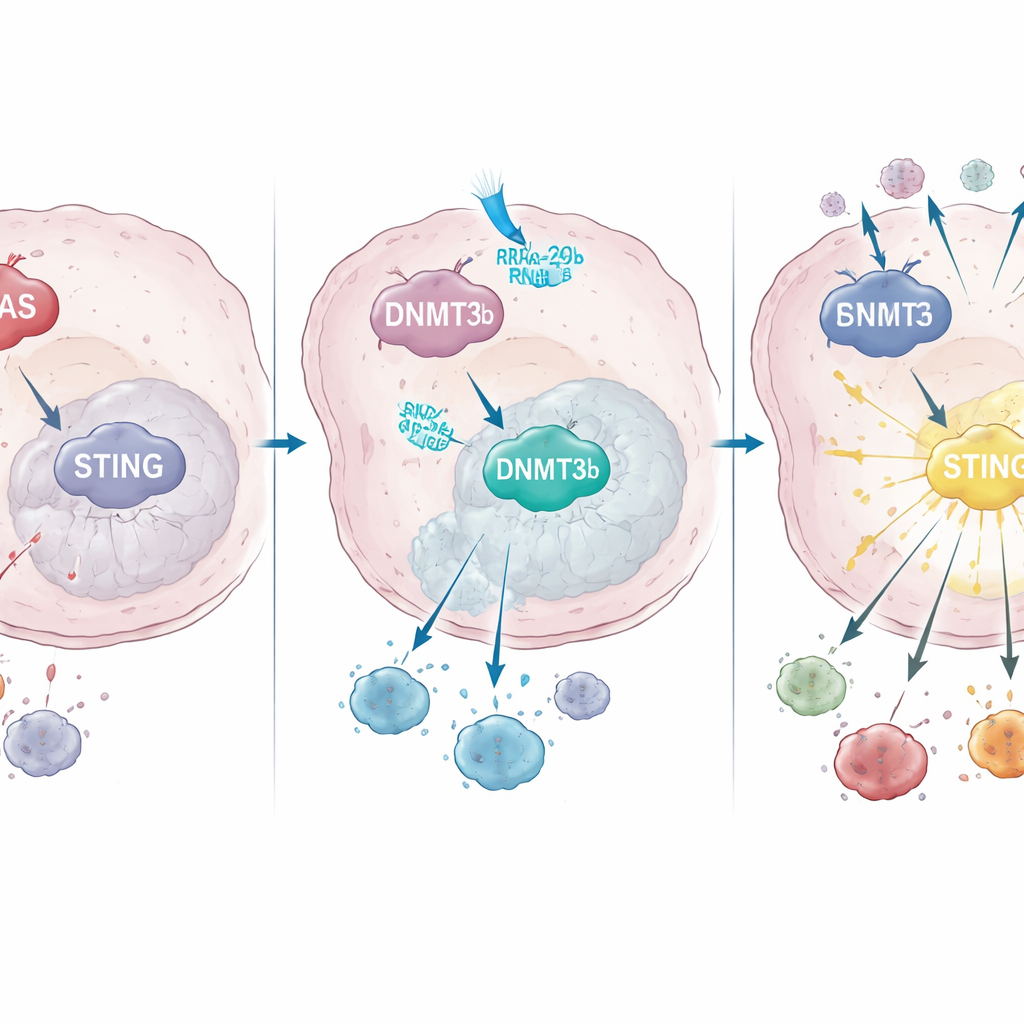
Hoe KRAS de genregulatie hervormt om STING uit te schakelen
Dieper gravend ontdekten de onderzoekers dat mutant KRAS de activiteit verhoogt van een DNA-modificerend enzym genaamd DNMT3b, dat methylgroepen aan bepaalde DNA-regio’s toevoegt en nabijgelegen genen uitschakelt. Zowel in kankercellijnen als in patiëntmonsters ging een hoog DNMT3b samen met een laag STING. Een cruciaal gedeelte van de STING-promotor — het DNA ‘aan’-schakelgebied — was sterk gemethyleerd in KRAS-gemuteerde tumoren, maar niet in tumoren met normale KRAS. Patiënten waarvan de tumoren STING na chemoradiotherapie nog konden opreguleren, vertoonden meer CD8-T-cel-infiltraat en betere overleving, wat benadrukt hoe belangrijk deze route is voor succesvolle behandeling.
Een klein RNA dat het alarm kan wekken
De auteurs onderzochten vervolgens wat DNMT3b zo overvloedig maakt in KRAS-gemuteerde kanker. Met microRNA-sequencing identificeerden ze een klein regulerend RNA, microRNA‑29b‑3p, dat normaal gesproken DNMT3b in toom houdt maar sterk wordt onderdrukt door mutant KRAS. Het herstellen van dit microRNA in in vitro gekweekte KRAS-gemuteerde cellen verlaagde DNMT3b, wekte STING opnieuw en versterkte de interferonproductie na bestraling; het blokkeren had het tegenovergestelde effect. In tumormonsters hadden KRAS-gemuteerde patiënten doorgaans lage microRNA‑29b‑3p-niveaus, hoge DNMT3b en laag STING, en patiënten met hogere microRNA‑29b‑3p leefden langer, wat deze moleculaire keten direct verbindt met klinische uitkomsten.
Een gerichte genleveringsaanpak die radiotherapie en immunotherapie versterkt
Om deze bevindingen naar een mogelijke behandeling te vertalen, ontwikkelde het team een onschadelijk virus (AAV) dat microRNA‑29b‑3p levert onder controle van een promotor die voornamelijk actief is in colorectale kankercellen. In muismodellen met KRAS‑gemuteerde colorectale tumoren zorgde toediening van deze AAV samen met lokale bestraling voor een dramatische krimp van zowel bestraalde tumoren als verre tumoren die geen bestraling ontvingen. De tumoren vertoonden minder DNMT3b, meer STING, sterkere interferonsignalen en veelvuldige infiltratie door T-cellen en andere immuuncellen. Wanneer dezelfde microRNA‑29b‑3p-behandeling werd gecombineerd met een immuuncheckpointremmer gericht op PD‑1, verbeterde de overleving verder, en dit voordeel was afhankelijk van CD8-T-cellen, wat bevestigt dat het immuunsysteem het zware werk verrichtte.
Wat dit voor patiënten zou kunnen betekenen
In eenvoudige bewoordingen laat deze studie zien hoe KRAS-gemuteerde colorectale kankers het ‘snoer doorsnijden’ naar een intern alarmsysteem dat bestraling normaal gesproken activeert, waardoor ze immuunaanvallen weten te ontwijken. Door één klein RNA, microRNA‑29b‑3p, te herstellen, konden de onderzoekers DNMT3b verlagen, STING heractiveren en immuunologisch ‘koude’ tumoren veranderen in ‘hete’ tumoren die beter reageren op zowel radiotherapie als checkpointremmers. Hoewel dit werk zich nog in de preklinische fase bevindt, wijst het op toekomstige behandelingen die bestraling combineren met tumortargeted genterapie om resistentie bij KRAS‑gemuteerde colorectale kanker te overwinnen, en zo bestaande therapieën voor veel meer patiënten effectief te maken.
Bronvermelding: Chang, HY., Chen, JY., Ke, TW. et al. Loss of MicroRNA-29b promotes DNMT3b-mediated STING downregulation to attenuate radiotherapy-induced antitumor immunity in KRAS-mutated colorectal cancer. npj Precis. Onc. 10, 93 (2026). https://doi.org/10.1038/s41698-026-01290-8
Trefwoorden: KRAS-gemuteerde colorectale kanker, radiotherapie-resistentie, STING-route, microRNA-29b, tumorimmunologie