Clear Sky Science · nl
Vergelijkende analyse van ctDNA-monitoringstrategieën bij gevorderde NSCLC met MET exon 14 skipping-mutaties behandeld met ensartinib
Waarom een bloedtest belangrijk is bij longkanker
Voor mensen met gevorderde longkanker is een van de belangrijkste vragen of een nieuw geneesmiddel daadwerkelijk werkt — en hoe snel artsen dat kunnen vaststellen. Deze studie onderzoekt een bloedgebaseerde benadering, waarbij gebruik wordt gemaakt van kleine fragmenten van tumor-DNA die in de bloedbaan circuleren, om snel te beoordelen hoe goed een gerichte therapie genaamd ensartinib patiënten helpt van wie de tumoren een specifieke genetische afwijking delen. De bevindingen suggereren dat een eenvoudige vroege bloedtest kan aangeven welke patiënten waarschijnlijk langere tijd baat hebben bij de behandeling en welke mogelijk een andere strategie nodig hebben.
De vingerafdrukken van een tumor in een buisje bloed
Kankercellen laten stukjes van hun genetisch materiaal los in het bloed, bekend als circulerend tumor-DNA. In deze proef richtten onderzoekers zich op mensen met niet-kleincellige longkanker die wordt aangedreven door een verandering in een gen genaamd MET, specifiek een defect dat bekendstaat als exon 14 skipping. Alle patiënten kregen ensartinib nadat eerdere behandelingen waren gefaald. Bloedmonsters werden vlak voor de start van het middel afgenomen en opnieuw vier weken later. Met een geavanceerde sequentietest die 229 kankergene gerelateerde genen scant, groepeerde het team de gedetecteerde afwijkingen in drie categorieën: veranderingen in MET zelf, een set goed gevestigde oncogene aandrijvers, en een brede verzamelgroep van elke detecteerbare mutatie.
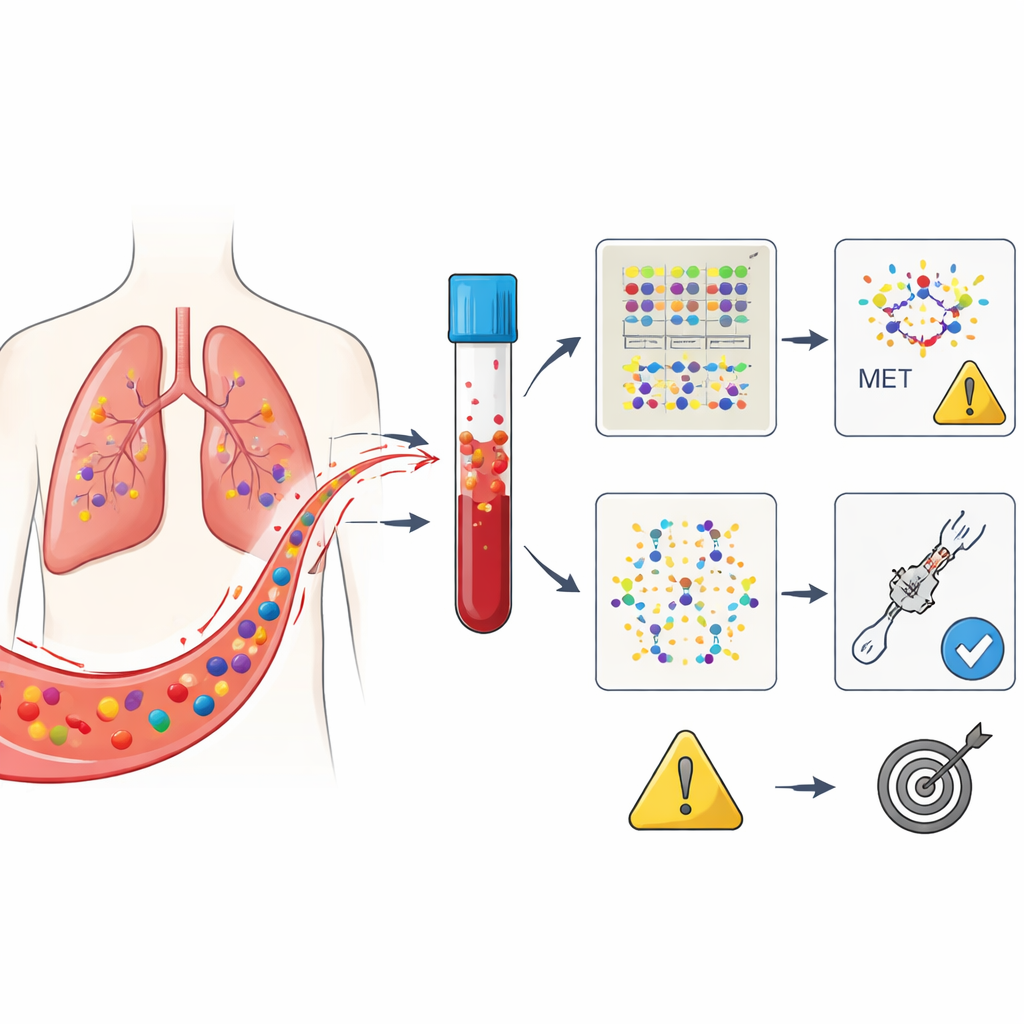
Drie manieren om hetzelfde bloedsignaal te lezen
De centrale vraag was welke van deze drie bloed"views" het beste voorspelt wie zal reageren op ensartinib en hoe lang die reactie zal duren. Bij aanvang had niet elke patiënt detecteerbaar tumor-DNA in het bloed, ook al droegen hun tumoren de MET-afwijking; dit weerspiegelt hoe ongelijk kankers DNA afgeven. Vroeg gezien voorspelde het enkel positief of negatief zijn voor tumor-DNA bij baseline de uitkomst niet sterk. Tegen de vierweekse tijdsperiode ontstond echter een duidelijk patroon: patiënten bij wie in het bloed geen MET-gerelateerde DNA-veranderingen meer werden aangetoond bleven veel langer vrij van ziekteprogressie dan degenen bij wie deze signalen aanhielden. Dit was waar, ook al konden tumormetingen op dat moment nog dubbelzinnig zijn.
Als MET-signalen vervagen, verbeteren de uitkomsten
Bij nadere beschouwing van hoe bloedresultaten in de tijd veranderden, vond het team drie trajecten. Sommige patiënten hadden nooit detecteerbaar MET-DNA in hun bloed, sommige begonnen positief en werden negatief, en anderen bleven positief of ontwikkelden nieuwe MET-veranderingen. Degenen die MET-signalen tegen week vier hadden gewist, genoten de langste periode voordat hun kanker vorderde, ongeveer negen maanden gemiddeld, en hadden het hoogste percentage meetbare tumorkrimp. Patiënten die positief bleven voor MET-DNA deden het veel slechter, met ziekteprogressie in net iets meer dan twee maanden gemiddeld. Het monitoren van de bredere sets mutaties leverde ook nuttige informatie op, maar was minder precies omdat veel laag-niveau of niet-gerelateerde veranderingen het beeld konden vertroebelen.
Balanceren tussen eenvoud en dieper inzicht
Alleen MET-gerelateerd DNA als leidraad gebruiken bood het scherpste en eenvoudigste beeld van of ensartinib hielp. Deze gefocuste benadering had een hoge specificiteit, wat betekent dat wanneer MET-signalen verdwenen, de kans groot was dat de patiënt het goed zou doen. Dat maakt het aantrekkelijk als praktisch hulpmiddel: enkelfunctie-tests zijn goedkoper, sneller en gemakkelijker te interpreteren dan grote genpanelen. Tegelijkertijd had het scannen van meer genen nog steeds waarde, omdat het nieuwe mutaties kon onthullen die konden verklaren waarom een tumor later niet meer reageerde en kon wijzen op toekomstige behandelingsopties. De studie suggereert dat het combineren van een smalle, MET-centrale blik voor vroege behandelbeslissingen met een bredere blik voor het volgen van resistentie het beste van beide benaderingen kan bieden.
Wat dit betekent voor patiënten
Voor leken is de kernboodschap dat een bloedtest die slechts een maand na de start van ensartinib wordt afgenomen al een aanwijzing kan geven over de langetermijnopbrengst van het middel. Als MET-gerelateerd tumor-DNA uit de bloedbaan verdwijnt, zijn de kansen op een betekenisvolle en blijvende respons groot; als het aanhoudt, moeten artsen mogelijk nauwkeuriger volgen of andere opties overwegen. Hoewel dit een relatief kleine, single-arm studie was die bevestiging in grotere groepen behoeft, versterkt het het idee dat "liquide biopsies" kunnen fungeren als een vroeg rapportcijfer voor gerichte behandelingen. In de toekomst zou dergelijke monitoring de zorg kunnen personaliseren, patiënten kunnen behoeden voor het blijven gebruiken van ineffectieve middelen en hen sneller kunnen leiden naar therapieën die wel werken.
Bronvermelding: Zhou, M., Zhu, Y., Sun, X. et al. Comparative analysis of ctDNA monitoring strategies in advanced NSCLC with MET exon 14 skipping mutations treated with ensartinib. npj Precis. Onc. 10, 110 (2026). https://doi.org/10.1038/s41698-026-01284-6
Trefwoorden: circulerend tumor-DNA, MET exon 14 skipping, ensartinib, niet-kleincellige longkanker, liquide biopsie monitoring