Clear Sky Science · nl
Een interpreteerbaar deep-learningmodel voor het voorspellen van moleculaire subtypes van endometriumcarcinoom op H&E‑gekleurde preparaten
Waarom dit van belang is voor de gezondheid van vrouwen
Endometriumcarcinoom, dat ontstaat in het slijmvlies van de baarmoeder, is een van de meest voorkomende kankers bij vrouwen en het sterftecijfer stijgt wereldwijd. Artsen weten inmiddels dat deze kanker meerdere moleculaire “varianten” kent die verschillend reageren op operatie, bestraling, chemotherapie en nieuwere immuuntherapieën. Tegenwoordig vereist het bepalen van die moleculaire subtypes meestal dure en tijdrovende gentests die veel ziekenhuizen niet gemakkelijk kunnen aanbieden. Deze studie onderzoekt of een zorgvuldig ontworpen kunstmatige intelligentie (AI)-systeem routinematige pathologiepreparaten—de roze‑ en paarse weefselbeelden die al van elke patiënt worden gemaakt—kan uitlezen en nauwkeurig deze moleculaire subtypes kan afleiden, waardoor precieze zorg mogelijk breder beschikbaar zou kunnen worden.
Een nadere blik op tumordiversiteit
Niet alle endometriumtumoren gedragen zich hetzelfde. Sommige groeien langzaam en blijven in de baarmoeder beperkt; andere verspreiden zich vroeg en zijn moeilijker te behandelen. Moderne richtlijnen verdelen deze tumoren in vier moleculaire subtypes op basis van DNA‑veranderingen en hoe de cellen DNA‑schade herstellen. Deze categorieën helpen bij het voorspellen van de prognose en bij beslissingen zoals hoe ingrijpend de operatie moet zijn en of een patiënt mogelijk baat heeft bij immunotherapie. De benodigde genetische tests en speciale kleuringen zijn echter duur, vergen deskundige interpretatie en zijn vaak niet beschikbaar in kleinere of middelenarme ziekenhuizen. Pathologen vermoeden al lang dat veel van deze moleculaire verschillen visuele aanwijzingen achterlaten in de manier waarop cellen en ondersteunend weefsel er onder de microscoop uitzien—maar die aanwijzingen kunnen te subtiel en complex zijn voor het menselijke oog om consistent te beoordelen.
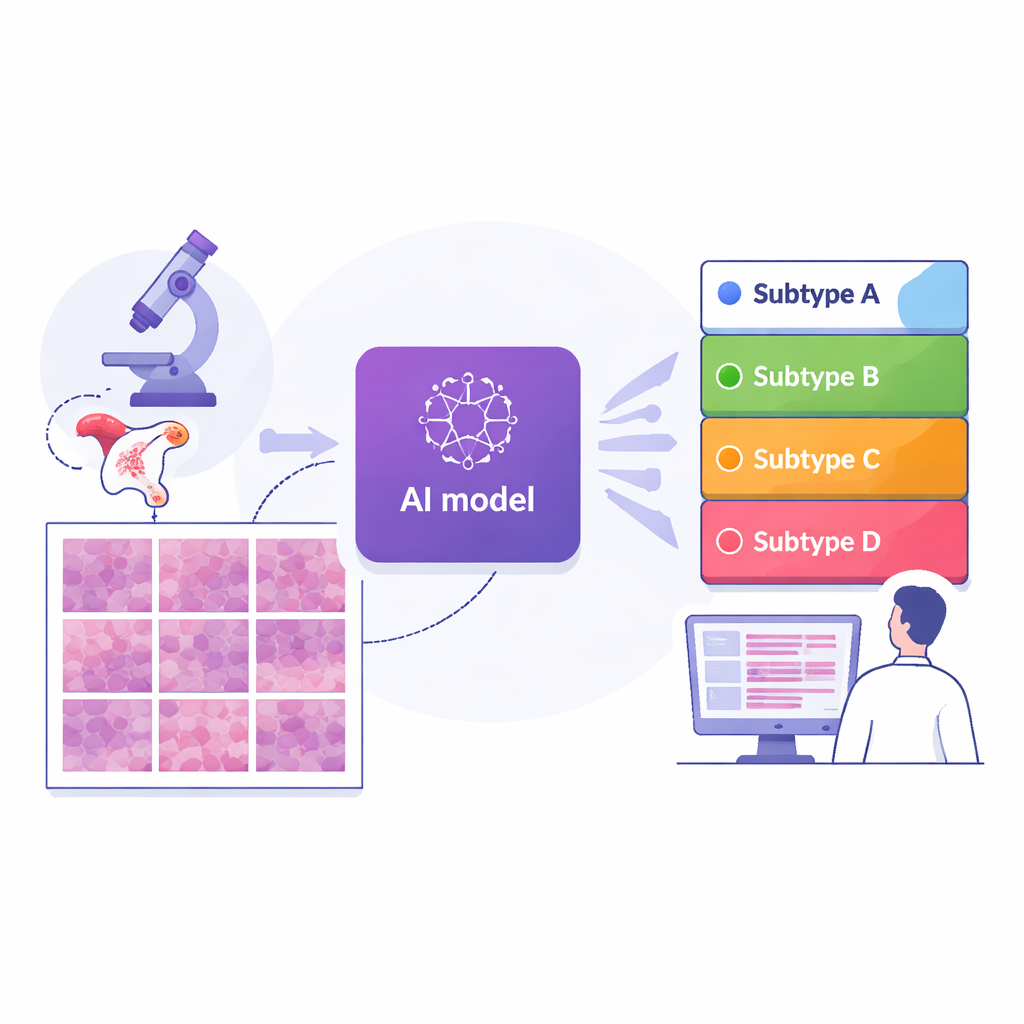
Computers leren pathologiepreparaten lezen
De onderzoekers verzamelden digitale beelden van 364 preparaten van 324 vrouwen behandeld in een groot kankercentrum in Shanghai, plus twee onafhankelijke vergelijkingsgroepen: 296 preparaten uit een internationaal openbaar dataset en 36 van een ander ziekenhuis in Suzhou. Voor elk geval was al vastgesteld tot welk van de vier moleculaire subtypes het behoorde met behulp van geavanceerde genetische testen. Het team verdeelde vervolgens elke whole‑slide‑afbeelding in duizenden kleine tegels en trainde een deep‑learningmodel—een type AI dat gebruikt wordt bij beeldherkenning—om elke tegel te bekijken en de waarschijnlijkheid te schatten dat deze tot elk subtype behoort. Door tegelvoorspellingen te middelen over een heel preparaat produceerde het systeem een enkele subtypevoorspelling per patiënt, wat overeenkomt met hoe artsen over de tumor als geheel denken.
Hoe goed het systeem presteerde
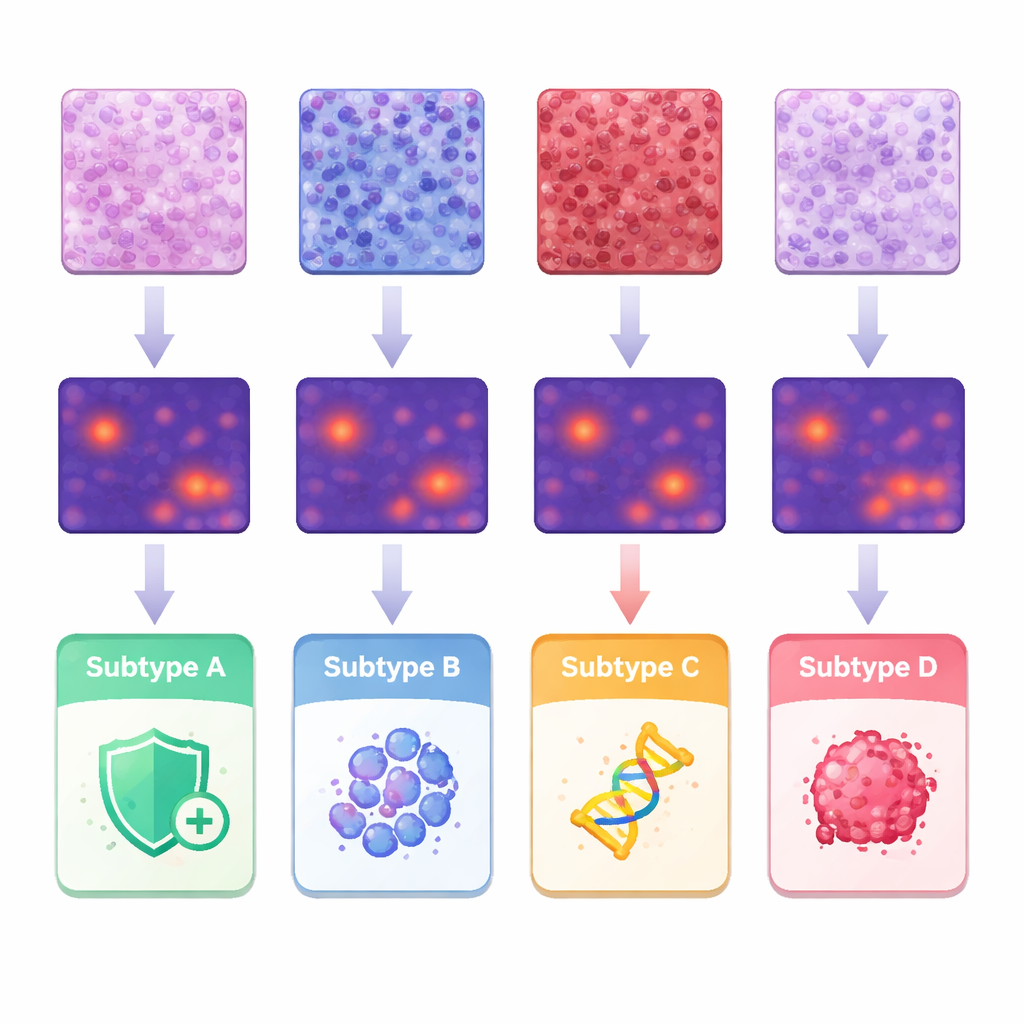
In de hoofdgroep uit Shanghai bereikte de AI een hoog nauwkeurigheidsniveau: de algemene score voor het onderscheiden van de vier subtypes (gemeten met een standaardstatistiek die loopt van 0,5 bij willekeurig raden tot 1,0 voor perfecte scheiding) was ongeveer 0,87. De prestaties bleven sterk—rond 0,84—toen het systeem werd getest op de twee externe groepen afkomstig van verschillende ziekenhuizen en slide‑scanners, wat suggereert dat de methode redelijk robuust is. Vergeleken met verschillende toonaangevende AI‑strategieën die complexere aandacht- of pooling‑mechanismen gebruiken, presteerde dit end‑to‑endmodel, gebouwd op een moderne beeldanalyse‑backbone, over het algemeen beter. Belangrijk is dat de auteurs het systeem interpreteerbaar hebben gemaakt: ze gebruikten visualisatietools om precies te markeren welke regio’s van elke tegel de AI voor zijn beslissingen gebruikte.
Wat de AI “zag” in het tumormicro‑milieu
Om te begrijpen welke kenmerken de voorspellingen aandreven, koppelde het team de AI‑heatmaps aan klassieke pathologieobservaties en aan gedetailleerde metingen van individuele celvormen en -ordening. Tumoren van één subtype lieten een dichte infiltratie van immuuncellen in het ondersteunend weefsel zien, terwijl een ander subtype de neiging had meer compact opeengepakte structurele cellen te hebben. Een derde groep vertoonde meer massieve plakken van sterk afwijkende tumorcellen, en het subtype dat geassocieerd is met agressief gedrag vertoonde papillaire, vingerachtige structuren en zeer onregelmatige kernen. Door ongeveer 245 miljoen cellen te segmenteren en te analyseren kwantificeerden de onderzoekers verschillen in celgrootte, variatie en onderlinge afstand, en toonden aan hoe bepaalde combinaties overeenkwamen met specifieke subtypes. Deze bevindingen ondersteunen het idee dat moleculaire verschillen een herkenbare afdruk op de weefselarchitectuur achterlaten die machines systematisch kunnen detecteren.
Van proof of concept naar klinische ondersteuning
Dit werk is niet bedoeld als vervanging van genetische testen; in plaats daarvan stelt het een "H&E‑first" triagetool voor dat de standaardkleuring gebruikt die al voor elke biopsie is voorbereid. In de praktijk zou een door AI gegenereerde waarschijnlijkheidskaart voor subtypes pathologen kunnen helpen beslissen welke bevestigende testen eerst te bestellen, beperkt weefsel prioriteren voor de meest informatieve assays en het nemen van behandelbeslissingen versnellen, vooral in ziekenhuizen waar volledige moleculaire profilering moeilijk te verkrijgen is. De studie benadrukt ook huidige beperkingen, zoals zwakkere prestaties voor het zeldzaamste subtype en de noodzaak van grotere, meer diverse datasets voordat implementatie mogelijk is. Toch biedt het een overtuigende demonstratie dat routinemicroscoopbeelden genoeg verborgen informatie bevatten zodat AI complexe moleculaire labels kan benaderen, en opent het een weg naar meer rechtvaardige, datagedreven zorg voor vrouwen met endometriumcarcinoom.
Bronvermelding: Guo, Q., Cui, H., Zhang, Y. et al. An interpretable deep learning model for predicting endometrial cancer molecular subtypes from H&E-stained slides. npj Precis. Onc. 10, 71 (2026). https://doi.org/10.1038/s41698-026-01280-w
Trefwoorden: endometriumcarcinoom, digitale pathologie, deep learning, moleculaire subtypes, precisie‑oncologie