Clear Sky Science · nl
Een geïntegreerde single-cell longkankeratlas onthult verschillende fibroblastfenotypes tussen adenocarcinom en plaveiselcelcarcinomen
Waarom de buurt rond een tumor ertoe doet
Longkanker bestaat niet alleen uit kankercellen. Het is meer als een drukke stad waar kankercellen naast bloedvaten, immuuncellen en ondersteunende cellen leven. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote implicaties: bouwen de twee belangrijke vormen van niet‑kleincellige longkanker—adenocarcinoom en plaveiselcelcarcinoom—verschillende “buurten” in de long, en kunnen die verschillen helpen verklaren waarom patiënten het beter of slechter doen? Met krachtige single‑cell technieken om DNA‑activiteit te lezen, brengen de onderzoekers honderden duizenden individuele cellen in kaart om te laten zien hoe één belangrijke groep ondersteunende cellen, fibroblasten, zich heel verschillend gedraagt in deze twee kankersoorten.
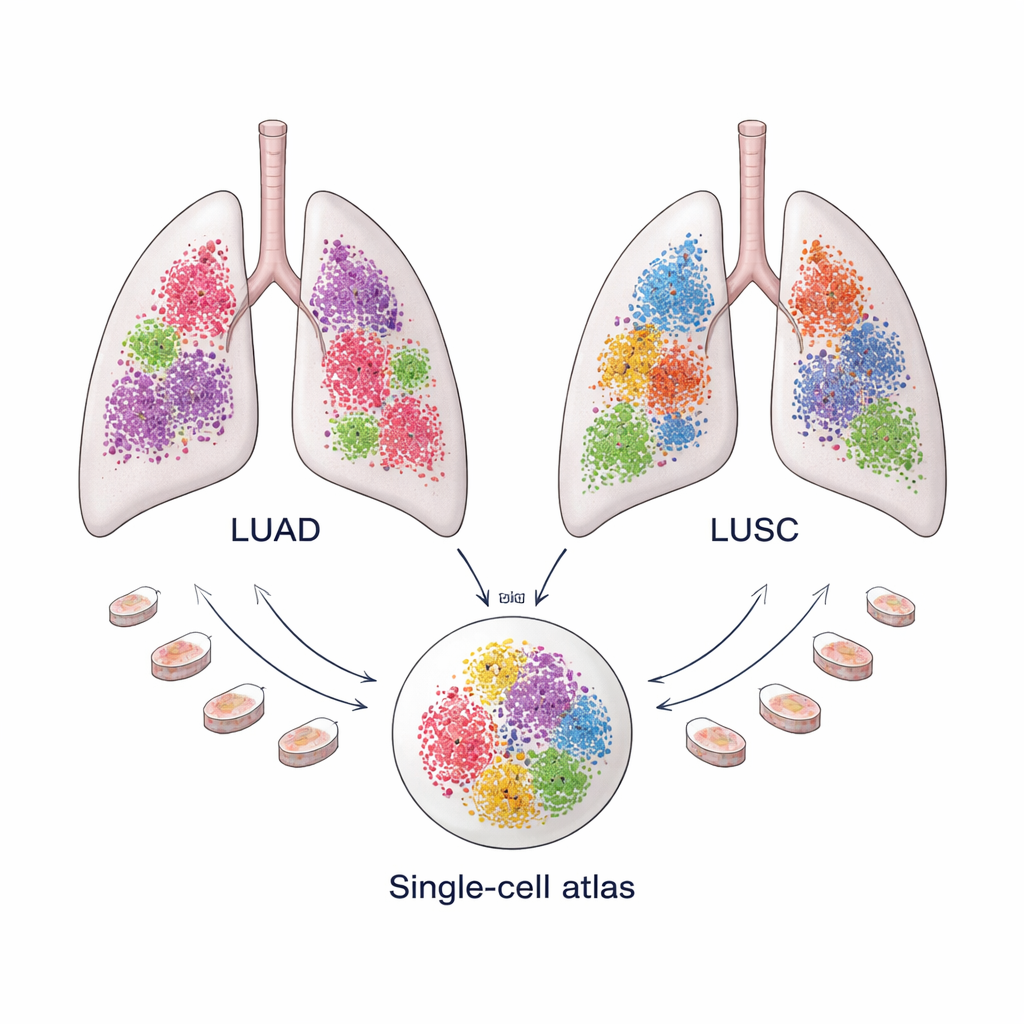
Twee veelvoorkomende longkankers, twee verschillende ecosystemen
Niet‑kleincellige longkanker vormt ongeveer 85 procent van de longkankers en wordt gedomineerd door twee types: longadenocarcinoom (LUAD), dat vaak in de buitenste delen van de long ontstaat, en longplaveiselcelcarcinoom (LUSC), dat vaker centraal voorkomt. Hoewel beide tegenwoordig onder hetzelfde brede label behandeld worden, reageren ze verschillend op therapie en hebben ze uiteenlopende langetermijnuitkomsten. Steeds meer bewijs suggereert dat deze verschillen niet alleen door de kankercellen zelf komen, maar ook door de tumor‑micro‑omgeving—de mix van immuuncellen, bloedvaten en structurele cellen die de tumor omringen en ermee interageren.
Het bouwen van een single‑cell longkankeratlas
Om deze microomgevingen gedetailleerd te begrijpen, stelde het team een grote “atlas” samen van single‑cell RNA‑sequencingdata: 366.652 cellen uit 175 LUAD‑monsters en 125.238 cellen uit 74 LUSC‑monsters, afkomstig uit tien publieke datasets. Het genexpressiepatroon van elke cel diende als een vingerafdruk waarmee de onderzoekers cellen konden indelen in hoofdgroepen zoals immuuncellen, bloedvatcellen, kankercellen en structurele of “stroma”cellen. Geavanceerde computationele methodes verwijderden technische ruis en brachten de monsters op één lijn zodat cellen van verschillende patiënten direct vergeleken konden worden. Deze schaal is cruciaal omdat sommige celtypen—vooral fibroblasten—zeldzaam zijn en in één enkele studie moeilijk in voldoende aantallen te isoleren zijn.
Fibroblasten: vormgevers van het tumorlanschap
Fibroblasten zijn ondersteunende cellen die bindweefsel bouwen en remodeleren. In tumoren worden ze kanker‑geassocieerde fibroblasten (CAF’s) genoemd, die afhankelijk van hun toestand de tumorgroei kunnen remmen of bevorderen. Door te focussen op meer dan 8.700 fibroblasten identificeerden de auteurs vijf belangrijke CAF‑subtypen: myofibroblastische CAF’s (mCAFs), inflammatoire CAF’s (iCAFs), vaatgerelateerde CAF’s (vCAFs), delende CAF’s (cCAFs) en antigeen presenterende CAF’s (apCAFs). De balans tussen deze subtypen verschilde opvallend tussen LUAD en LUSC. LUAD‑tumoren hadden relatief meer iCAFs, die hoge niveaus van ontstekingsmoleculen afscheiden, terwijl LUSC‑tumoren rijker waren aan mCAFs, die stijf, vezelig weefsel produceren en helpen het fysieke geraamte van de tumor te vormen.
Kankercellen leren fibroblasten hun rol
Om te testen of de kankercellen zelf fibroblasten instrueren hun identiteit aan te nemen, kweekten de onderzoekers normale longfibroblasten in kweekschalen naast ofwel LUAD‑ ofwel LUSC‑cellijnen. Wanneer fibroblasten werden blootgesteld aan LUAD‑cellen, zetten ze genen aan die typerend zijn voor iCAFs, waaronder bekende ontstekingssignalen zoals IL‑6 en bepaalde chemokines. In combinatie met LUSC‑cellen schakelden dezelfde fibroblasten in plaats daarvan mCAF‑genen in die betrokken zijn bij spierachtige contractie en collageenproductie. Analyses van cel‑tot‑celcommunicatie suggereerden dat LUAD‑cellen cytokines zoals IL‑1, LIF en OSM gebruiken om de inflammatoire iCAF‑toestand te stimuleren, terwijl LUSC‑cellen meer leunen op mechanische signalen en niet‑canonieke WNT‑signalering om fibroblasten richting het matrixbouwende mCAF‑type te duwen.
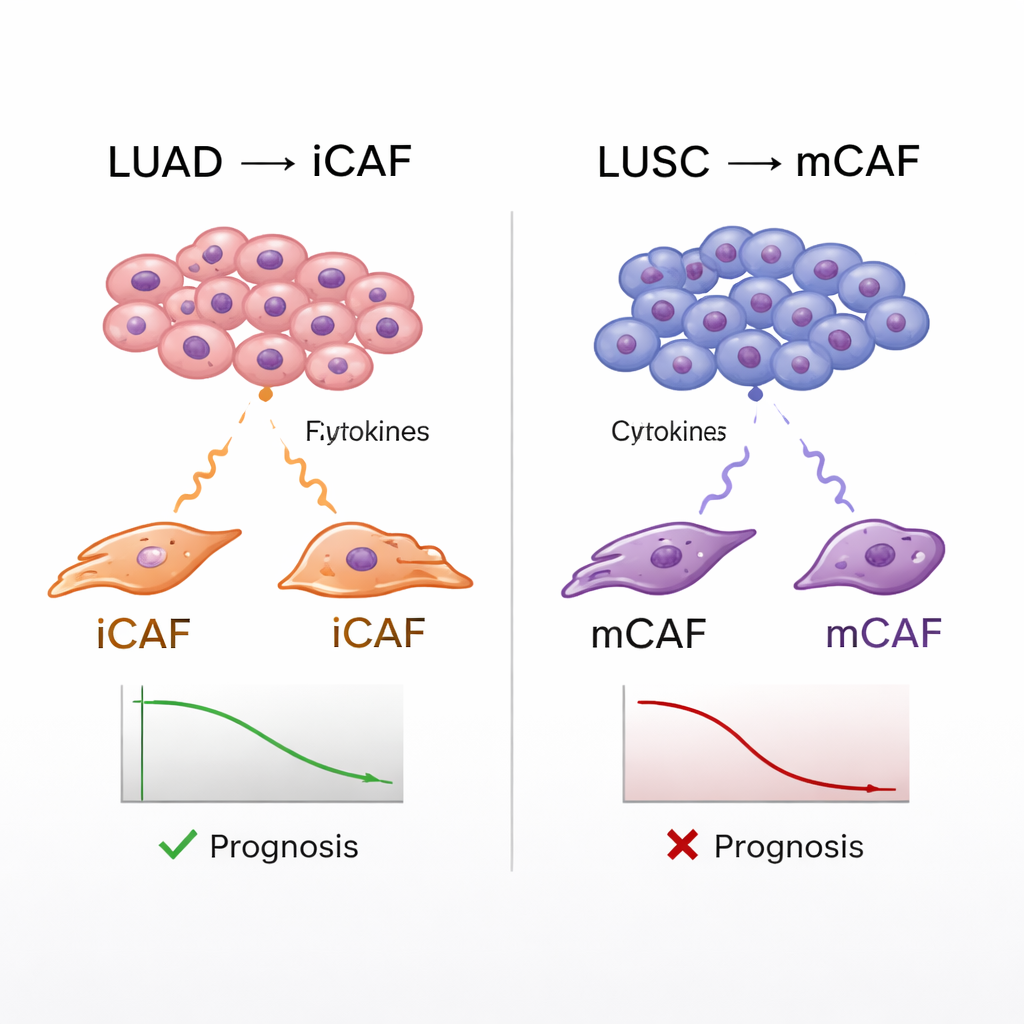
Het koppelen van fibroblasttypen aan patiëntuitkomsten
De atlas stelde het team ook in staat CAF‑subtypen te koppelen aan gegevens van echte patiënten. Met grote kankerdatabanken schatten ze hoe sterk elk patiëntentumor genhandtekeningen voor de verschillende fibroblasttypen tot expressie bracht en vergeleken deze scores met overleving. In zowel LUAD als LUSC waren tumoren verrijkt in mCAFs geassocieerd met slechtere uitkomsten, wat overeenkomt met het idee dat een dichte, vezelige capsule rond tumoren de kankerprogressie kan ondersteunen en immuunaanvallen kan blokkeren. iCAFs toonden echter een dubbel gezicht: in LUSC voorspelden hoge iCAF‑signaturen ook een slechtere overleving, terwijl ze in LUAD juist met betere uitkomsten geassocieerd waren. Verdere analyses suggereerden dat iCAFs in LUSC neutrofielen aantrekken—immuuncellen die in deze context ogenschijnlijk remmend werken op behulpzame T‑cellen—waardoor een extra vijandige omgeving voor effectieve immuunreacties ontstaat.
Wat dit betekent voor toekomstige zorg bij longkanker
Voor niet‑specialisten is de kernboodschap dat niet alle ondersteunende cellen in longtumoren hetzelfde zijn, en dat hetzelfde fibroblastsubtype tegenovergestelde betekenissen kan hebben afhankelijk van de tumorcontext. LUAD en LUSC verschillen niet alleen in het DNA van hun kankercellen; ze bouwen verschillende microscopische ecosystemen die bepalen hoe tumoren groeien en hoe patiënten het doen. Door deze ecosystemen cel voor cel in kaart te brengen, identificeert deze studie specifieke fibroblastpopulaties die als prognostische markers of als doelwitten voor toekomstige therapieën kunnen dienen—waardoor behandelingen idealiter afgestemd kunnen worden op niet alleen het type kanker maar ook op de samenstelling van de cellen die de tumor omringen en ondersteunen.
Bronvermelding: Hirano, Y., Suzuki, H., Nakayama, J. et al. An integrated single-cell lung cancer atlas reveals distinct fibroblast phenotypes between adenocarcinoma and squamous cell carcinomas. npj Precis. Onc. 10, 72 (2026). https://doi.org/10.1038/s41698-026-01279-3
Trefwoorden: longkanker, tumormicro‑omgeving, fibroblasten, single-cell RNA-sequencing, kankerprognose