Clear Sky Science · nl
TheraMind: een multi-LLM-ensemble voor het versnellen van drug repurposing bij longkanker via case report-mining
Waarom dit belangrijk is voor patiënten en artsen
Voor mensen met vergevorderde longkanker is tijd kostbaar en raken behandelingsopties vaak snel uitgeput. Het ontwikkelen van volledig nieuwe geneesmiddelen kan meer dan tien jaar duren, maar verspreide aanwijzingen over nuttige therapieën kunnen al verborgen liggen in gepubliceerde patiëntverhalen, zogenoemde case reports. Dit artikel introduceert TheraMind, een kunstmatig-intelligentiesysteem dat duizenden van deze rapporten doorzoekt om bestaande medicijnen te vinden die mogelijk veilig hergebruikt kunnen worden om mensen met slecht behandelbare longkanker te helpen.
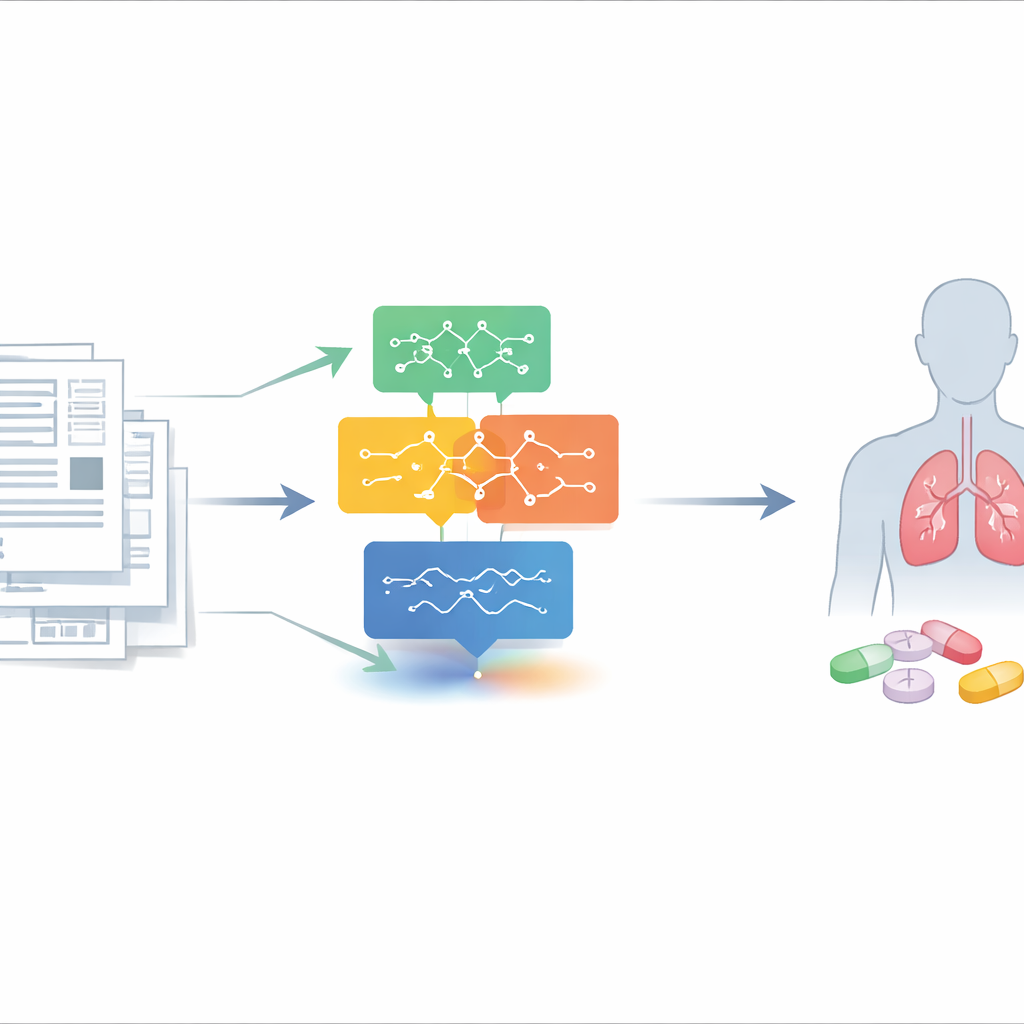
De uitdaging van nieuwe toepassingen voor oude medicijnen
Niet-kleincellige longkanker is de dodelijkste kanker ter wereld, met overlevingscijfers die zeer laag blijven zodra de ziekte is uitgezaaid. Nieuwe geneesmiddelen ontdekken en testen vanaf nul is traag, duur en riskant. Daarentegen zijn "herbestemde" medicijnen al goedgekeurd voor andere aandoeningen, dus hun veiligheid is veel beter bekend. Oncologen zijn geïnteresseerd in zulke middelen, vooral voor patiënten die alle standaardbehandelingen hebben doorlopen, maar zij hebben echte klinische bewijzen nodig dat een middel daadwerkelijk iemand met longkanker heeft geholpen — niet alleen veelbelovende laboratoriumgegevens. Deze klinische aanwijzingen verschijnen vaak in individuele case reports die diep in de medische literatuur begraven liggen en die met de hand moeilijk en tijdrovend te vinden zijn.
Een digitale lezer voor duizenden patiëntverhalen
De onderzoekers bouwden TheraMind als een onvermoeibare, zorgvuldige lezer van case reports. Uitgaande van 18 medicijnkandidaten die werden voorgesteld door eerdere genomische en laboratoriumstudies, haalde het systeem automatisch 10.023 case reports uit PubMed, de grootste medische artikeldatabase. Vervolgens voerde het de tekst van elk rapport in bij drie afzonderlijke taalmodellen — verschillende AI-"lezers" getraind om medisch schrijven te begrijpen. Voor elk rapport beantwoordden deze modellen dezelfde vier eenvoudige vragen: Wordt de patiënt beschreven als iemand met niet-kleincellige longkanker? Werd het bestudeerde medicijn specifiek gegeven om die aandoening te behandelen? Werd de behandeling voortijdig gestopt? En had de patiënt een goed klinisch resultaat?
Hoe het AI-team tot een gezamenlijke beslissing komt
Zodra TheraMind elk rapport omzet in een set ja-of-nee-antwoorden, komen er meerdere lagen van besluitvorming in werking. Een methode gebruikt een handmatig ontworpen beslisboom die vereist dat alle vier de voorwaarden worden vervuld voordat een casus relevant wordt genoemd voor drug repurposing. Een andere methode laat één model het bewijs flexibeler wegen, door zowel de ja-of-nee-antwoorden als de korte verklaringen die het genereerde mee te nemen. De krachtigste methode combineert drie afzonderlijke classifiers, elk gebaseerd op een ander model, en accepteert een rapport alleen wanneer ten minste twee van de drie instemmen dat het relevant is. Deze "meerderheidsstem"-aanpak helpt individuele fouten te neutraliseren, vergelijkbaar met het vragen van meerdere onafhankelijke artsen om hetzelfde dossier te beoordelen.
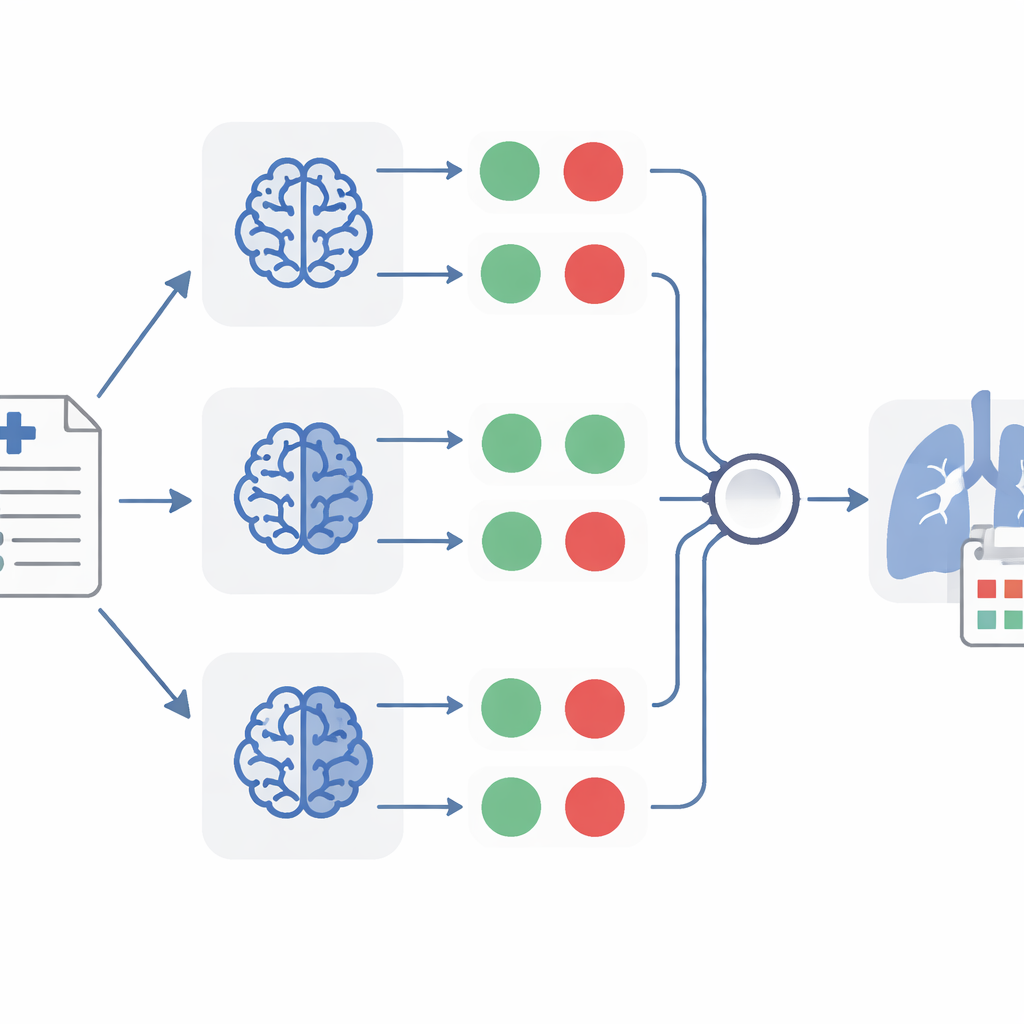
Wat TheraMind ontdekte in longkankerrapporten
Toegepast op de grote verzameling case reports markeerde TheraMind 26 rapporten als sterke ondersteuning voor het gebruik van tien verschillende geneesmiddelen bij niet-kleincellige longkanker. De ensemblemethode behaalde een recall van ongeveer 92 procent, wat betekent dat het vrijwel alle werkelijk relevante rapporten vastlegde, terwijl het een zeer hoge specificiteit van 99,7 procent behield, zodat maar weinig irrelevante rapporten doorsijpelen. Voor elk geselecteerd rapport extraheerde het systeem ook belangrijke patiëntgegevens — zoals leeftijd, geslacht, medische voorgeschiedenis, aandoening en het vermoedelijke medicijn — in een consistent gegevensformaat, en genereerde het een korte, eenvoudige samenvatting van de casus. Menselijke beoordelaars met achtergronden in biologie en computerwetenschappen controleerden deze uitkomsten en bevestigden dat één van de modellen bijzonder nauwkeurige en volledige extracties leverde.
Verder dan longkanker en richting de kliniek
Om de flexibiliteit van het systeem te testen, richtte het team TheraMind ook op borstkanker en meerdere kandidaatmedicijnen die eerder door hun eigen onderzoek waren geïdentificeerd. In die context rapporteerde het systeem geen overeenkomende case reports, een nauwkeurige weergave van het huidige wetenschappelijke register in plaats van het verzinnen van bewijs. De auteurs bepleiten dat dit soort gestructureerde, transparante pijplijn — die regelgebaseerde logica combineert met meerdere AI-lezers — kan helpen de kloof te dichten tussen laboratoriumontdekkingen en behandelingen die klaar zijn voor klinische proeven. Ze benadrukken zowel de belofte van het toepassen van vergelijkbare methoden op andere kankersoorten als de noodzaak om patiëntprivacy zorgvuldig te behandelen als toekomstige versies rechtstreeks op elektronische medische dossiers aansluiten.
Wat dit betekent voor toekomstige behandelingen
Eenvoudig gezegd verandert TheraMind verspreide, ongestructureerde patiëntverhalen in georganiseerde bewijzen waar artsen en onderzoekers iets mee kunnen. Door snel rapporten aan het licht te brengen waarin bestaande medicijnen mensen met longkanker lijken te helpen, kan het aangeven welke herbestemde middelen nader onderzoek in klinische trials verdienen. Hoewel het medische oordeelsvorming niet vervangt, biedt deze multi-model AI-lezer een manier om bergen medisch tekst te zeven en een korte, betrouwbare lijst van veelbelovende opties te leveren voor patiënten die dringend nieuwe keuzes nodig hebben.
Bronvermelding: More, V., Lu, L., Ding, Z. et al. TheraMind: a multi-LLM ensemble for accelerating drug repurposing in lung cancer via case report mining. npj Precis. Onc. 10, 95 (2026). https://doi.org/10.1038/s41698-025-01265-1
Trefwoorden: drug repurposing, longkanker, case reports, grote taalmodellen, klinische evidentie-mining