Clear Sky Science · nl
Neoadjuvante sintilimab, albuminegebonden paclitaxel en carboplatine voor lokaal gevorderd, reseceerbaar plaveiselcelcarcinoom van de slokdarm: klinische studie en mechanistische verkenning
Het tij keren tegen een dodelijke keel‑/slokdarmkanker
Slokdarmkanker behoort tot de dodelijkste kankers wereldwijd en wordt vaak pas ontdekt als de ziekte al diep in de borstkas is gevorderd. Veel patiënten komen nog in aanmerking voor chirurgie, maar zelfs met de beste beschikbare chemotherapie en bestraling blijft het risico op terugkeer hoog. Deze studie onderzoekt een nieuwe manier om de eigen afweer van het lichaam vóór de operatie te versterken en kijkt onder de microscoop hoe tumoren en hun omliggende cellen daarop reageren. De bevindingen wijzen op effectievere behandelopties en op een pad naar werkelijk gepersonaliseerde zorg.
Een nieuw driestrengsplan vóór de operatie
De onderzoekers namen 24 mensen in China op in de studie met een veelvoorkomende en agressieve vorm van slokdarmkanker, het plaveiselcelcarcinoom. Allen hadden tumoren die gevorderd maar nog wel chirurgisch verwijderbaar waren. Voorafgaand aan de operatie kreeg elke patiënt drie cycli van een combinatiebehandeling: sintilimab, een immuun‑activerend antilichaam dat T‑cellen helpt kankercellen te herkennen; plus twee standaard chemotherapiemiddelen, albuminegebonden paclitaxel en carboplatine. Na deze neoadjuvante fase ondergingen de patiënten een operatie om de slokdarmtumor te verwijderen, en de meesten zetten sintilimab daarna voort.
Krachtiger tumorkrimp en bemoedigende overleving
Toen chirurgen en pathologen de verwijderde tumoren onderzochten, bleek dat deze voor‑operatieve behandeling bij veel patiënten tot sterke krimp had geleid. Ongeveer 42% toonde wat artsen een majeure pathologische respons noemen, wat betekent dat slechts een klein gedeelte van de levende kankercellen overbleef. Bij één op de drie patiënten werden in het hoofdgebied van de tumor helemaal geen detecteerbare kankercellen meer gevonden. Ook op scans en tijdens klinische follow‑up waren de resultaten veelbelovend: drie jaar na behandeling was ruwweg driekwart van de patiënten vrij van recidief en bijna vier op de vijf nog in leven. Belangrijk is dat de bijwerkingen van dit geïntensiveerde schema beheersbaar waren, zonder behandelinggerelateerde sterfgevallen en met veilige en haalbare chirurgische verwijdering.
Hoe de buurt van de tumor de respons bepaalt
Niet iedere patiënt profiteerde evenveel, dus het team vroeg zich af waarom dat zo was. Ze richtten zich op de tumormicro‑omgeving — de complexe buurt van kankercellen, immuuncellen en signaalmoleculen. Met gerichte eiwitmetingen op zorgvuldig gedisseceerde tumormonsters vergeleken ze patiënten die goed reageerden met degenen die dat niet deden. Voorafgaand aan de behandeling vonden ze 14 eiwitten die verschilden tussen de twee groepen. Eén oppervlakte-eiwit, CD44, stak er uit: tumoren met hogere CD44‑niveaus bleken geneigd beter te reageren op de sintilimab‑gebaseerde therapie. Na behandeling waren veel eiwitten betrokken bij immuunactiviteit en DNA‑herstel verminderd bij responders, wat suggereert dat de combinatiebehandeling succesvol de ondersteunende systemen van de kanker verstoorde en het lokale immuunlandschap hervormde.
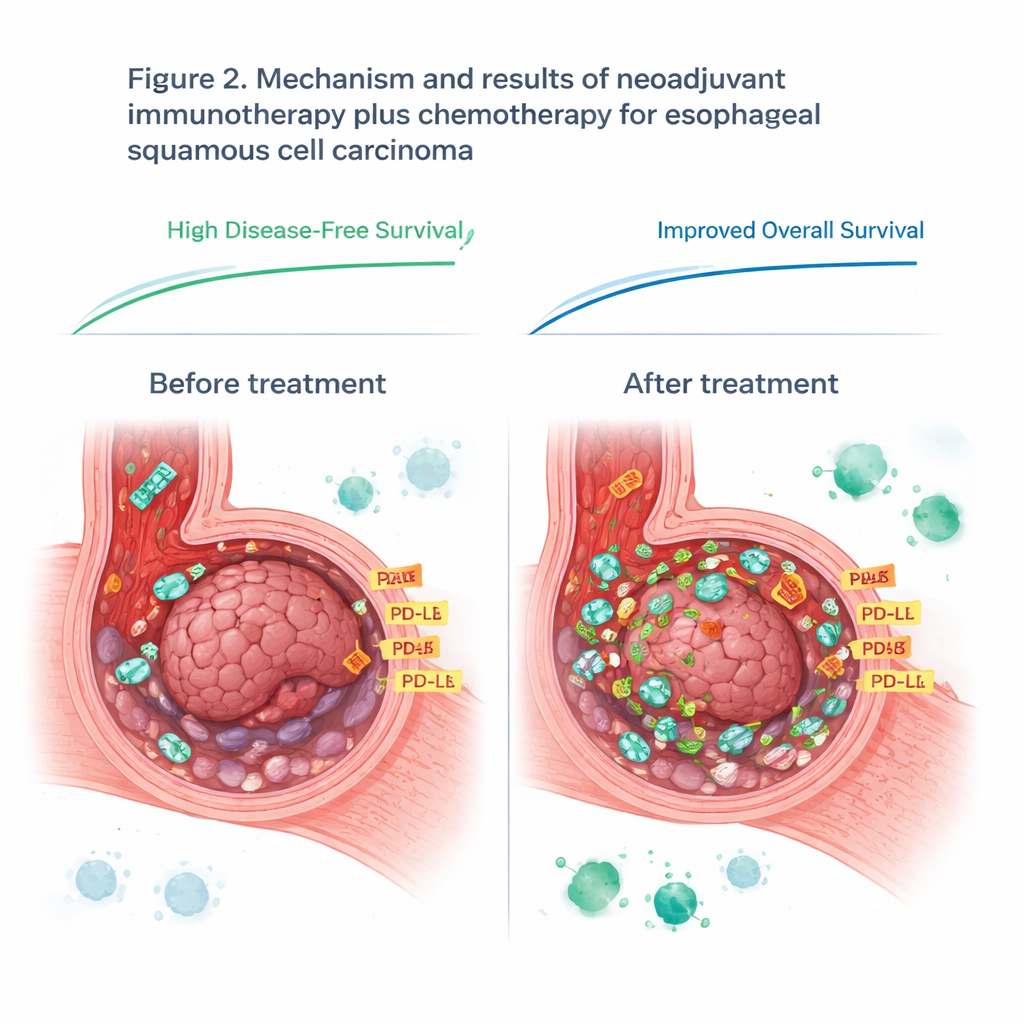
Een heroverweging van een populair immuunmarker
De studie bekeek ook PD‑L1, een eiwit dat vaak als kompas wordt gebruikt om te bepalen wie baat kan hebben bij immuuncheckpoint‑remmers. Voorafgaand aan de behandeling voorspelden PD‑L1‑niveaus in de tumormonsters niet wie het goed zou doen, wat de huidige praktijk bij dit type kanker ter discussie stelt. Tijdens de behandeling stegen PD‑L1‑waarden echter bij alle patiënten, waarschijnlijk doordat het geactiveerde immuunsysteem de tumor overspoelde met inflammatoire signalen. Na therapie bleken hogere PD‑L1‑niveaus in het overgebleven tumorweefsel sterker gerelateerd aan hoe goed de immunotherapie werkte. Dit suggereert dat timing ertoe doet: één enkele meting van PD‑L1 vóór behandeling kan cruciale veranderingen missen die zich voordoen zodra het immuunsysteem wordt geactiveerd.
Wat dit betekent voor patiënten en de toekomst
Voor mensen die een operatie ondergaan voor gevorderde slokdarmkanker bevat deze studie twee hoopgevende boodschappen. Ten eerste lijkt het combineren van sintilimab met chemotherapie vóór de operatie tumoren dieper te laten krimpen en mogelijk de kans op langdurige overleving te vergroten, zonder gevaarlijk extra bijwerkingen. Ten tweede laat het werk zien dat de tumor en de micro‑omgeving niet vastliggen, maar door behandeling worden hervormd op manieren die via eiwitten als PD‑L1 en CD44 kunnen worden gevolgd. In de toekomst zouden zulke moleculaire vingerafdrukken artsen kunnen helpen therapieën in real time te selecteren en aan te passen, waardoor meer ‘koude’ tumoren die het immuunsysteem negeren, kunnen worden omgevormd tot ‘hete’ tumoren die een krachtige, duurzame immuunaanval uitnodigen.
Bronvermelding: Wu, H., Jiang, Q., Li, X. et al. Neoadjuvant sintilimab, albumin-bound paclitaxel, and carboplatin for locally advanced, resectable esophageal squamous cell carcinoma: clinical study and mechanistic exploration. npj Precis. Onc. 10, 82 (2026). https://doi.org/10.1038/s41698-025-01248-2
Trefwoorden: slokdarmkanker, immunotherapie, neoadjuvante therapie, PD-1-remmers, tumormicro-omgeving