Clear Sky Science · nl
Algoritme-gestuurde geïndividualiseerde therapieontwerpen verbeteren de overleving in een muismodel van triple-negatieve borstkanker
Waarom slimmer chemotherapiegeven ertoe doet
Chemotherapie redt levens, maar wordt nog vaak op een „one-size-fits-all”-manier toegediend: mensen met een vergelijkbare kanker krijgen vaak dezelfde medicatiedosis op hetzelfde schema. Dat kan voor sommigen zware bijwerkingen betekenen en voor anderen onvoldoende voordeel opleveren. De hier beschreven studie stelt een eenvoudige maar krachtige vraag: wat als we computersystemen konden gebruiken om chemotherapie in real time voor elk individu af te stemmen, zoals een thermostaat de verwarming in een huis regelt? Met behulp van een geavanceerd muismodel van een agressieve borstkanker tonen de onderzoekers aan dat zulke op maat gemaakte dosering de overleving kan verlengen en de ontwikkeling van medicijnresistentie kan beperken.
Het probleem van routinematige kankermedicijnschema’s
Vandaag de dag krijgen veel patiënten de hoogst verdragen dosis chemotherapie, gegeven met vaste tussenpozen. Dit zogenaamde maximum tolerated dose-protocol houdt geen rekening met hoe snel een specifiek gezwel groeit, hoe het lichaam van een patiënt het medicijn verwerkt of hoe dat gezwel in de loop van de tijd reageert. Als gevolg daarvan kunnen tumoren aanvankelijk krimpen maar later terugkomen als meer medicijnresistente varianten, terwijl patiënten de last van sterke bijwerkingen dragen. Eerdere pogingen om dit te verbeteren, zoals „metronomische” chemotherapie met kleinere, frequentere doses, hebben gemengde resultaten opgeleverd in klinische proeven en hebben niet duidelijk gemaakt hoe je het beste doses en timing kiest. Er is een duidelijke behoefte aan een meer rationele, geïndividualiseerde manier om chemotherapie in te plannen.
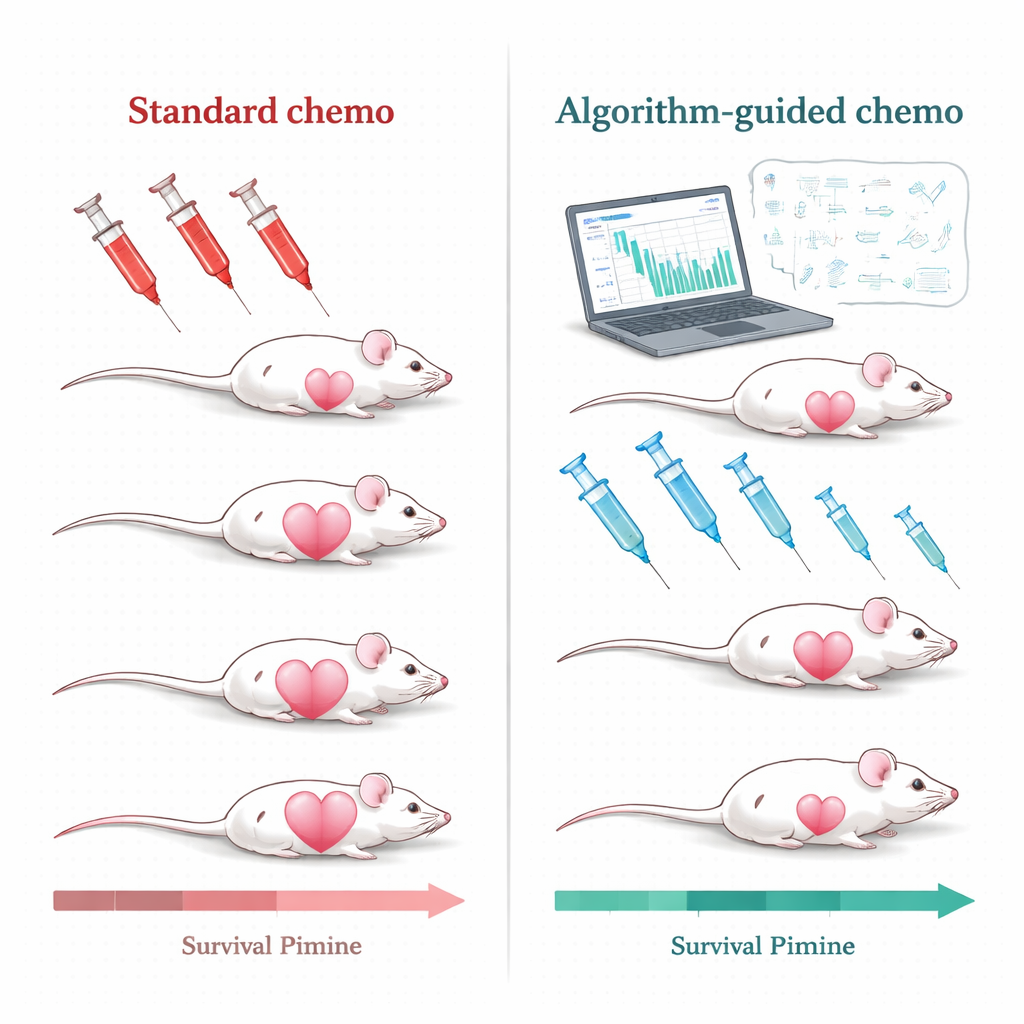
Algoritmen gebruiken om de behandeling aan te passen
Het onderzoeksteam pakte deze uitdaging aan bij muizen met triple-negatieve borsttumoren, een vorm van borstkanker die bij mensen bijzonder moeilijk te behandelen is en nog vrijwel volledig afhankelijk is van chemotherapie. De muizen werden behandeld met een veelgebruikte formulering, pegyleerde liposomale doxorubicine. In plaats van herhaaldelijk hoge doses toe te dienen alleen wanneer tumoren teruggroeiden tot een bepaalde omvang, bouwden de wetenschappers wiskundige modellen die beschrijven hoe de tumor groeit, afsterft onder behandeling en hoe het medicijn door de bloedbaan beweegt. Ze voerden aan die modellen eenvoudige, klinisch realistische metingen toe: herhaalde tumoromvangmetingen en bloedspiegels van het medicijn. Uit deze invoer genereerde een computeralgoritme gepersonaliseerde behandelplannen voor elke muis.
Twee manieren waarop de computer kan helpen
De studie testte twee varianten van algoritme-ondersteund therapieontwerp. In de ene benadering, PDPK genoemd, gebruikte de computer vroege gegevens om een 30-daags schema te ontwerpen van relatief kleine, herhaalde doses die bedoeld waren de medicijnspiegel in het bloed constant maar laag te houden — hoog genoeg om de tumor te beheersen, maar laag genoeg om toxiciteit te beperken. In de tweede benadering, model predictive control, werkte het algoritme het plan elke dag bij op basis van de meest recente tumormeting en paste de dosisgroottes aan om de tumor gestaag naar beneden te duwen. Beide methoden rustten op hetzelfde basisidee: gebruik een realistische „digitale tweeling” van de tumordragende muis om vele mogelijke doseringspatronen vooruit te simuleren en de patronen te kiezen die het meest kansrijk zijn binnen veiligheidsbeperkingen.
Langere overleving en minder medicijnresistentie
Toen het team deze algoritme-gestuurde regimens vergeleek met het standaard hoogdosisprotocol dat op tumorgroei reageert, waren de verschillen opvallend. Onder conventionele therapie krompen tumoren vaak aanvankelijk sterk maar kwamen uiteindelijk terug, en herhaalde grote doses bevorderden het ontstaan van medicijnresistente ziekte. In tegenstelling daarmee hielden de meeste algoritme-ontworpen behandelingen tumoren veel strakker onder controle, verlengden ze de tijd tot terugval en voorkwamen ze in veel gevallen duidelijke tekenen van resistentie gedurende de studieperiode. Over tientallen muizen leefden zowel de PDPK- als de model predictive control-groepen aanzienlijk langer dan dieren op het standaardschema, waarbij verschillende algoritmegebaseerde strategieën sterke, statistisch significante overlevingsvoordelen lieten zien.
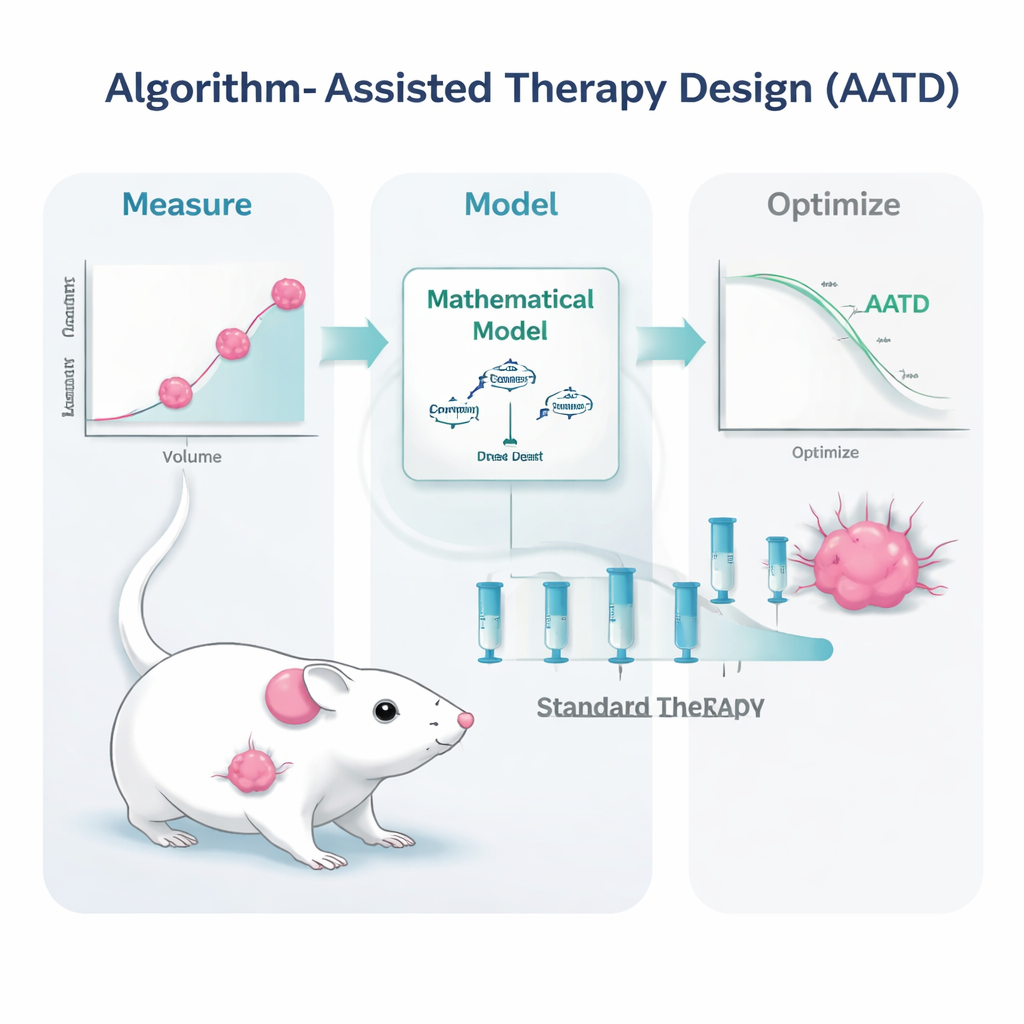
Wat dit voor toekomstige patiënten kan betekenen
Hoewel dit werk in muizen is uitgevoerd, zijn de belangrijkste ingrediënten — het meten van tumoromvang, het monitoren van medicijnspiegels in het bloed en het draaien van computermodellen — al mogelijk bij menselijke patiënten met moderne beeldvorming en laboratoriumhulpmiddelen. De studie suggereert dat artsen in plaats van te vragen: „Wat is de standaarddosis?”, op den duur kunnen vragen: „Gezien het gedrag van deze patiëntens eigen tumor en de manier waarop het medicijn wordt verwerkt, welke dosis en timing werkt nu het beste?” Praktische obstakels blijven, zoals de noodzaak van frequentere metingen en de logistiek van flexibele dosering, maar de boodschap is duidelijk: chemotherapie hoeft niet bot en uniform te zijn. Met behulp van algoritmen kan het een preciezer, aanpasbaar instrument worden dat patiënten een betere kans biedt op langdurige controle van agressieve kankers.
Bronvermelding: Gombos, B., Léner, V., Drexler, D.A. et al. Algorithm-assisted individualized therapy design improves survival in a mouse model of triple-negative breast cancer. npj Precis. Onc. 10, 84 (2026). https://doi.org/10.1038/s41698-025-01245-5
Trefwoorden: gepersonaliseerde chemotherapie, triple-negatieve borstkanker, algoritme-gestuurde therapie, wiskundige tumormodellering, doxorubicine dosering