Clear Sky Science · nl
Ruimtelijke transcriptomica onthult moleculaire heterogeniteit en subtypspecifieke therapeutische doelen bij kleincellig longkanker
Waarom deze longkankerstudie ertoe doet
Kleincellig longkanker behoort tot de dodelijkste kankersoorten, treft vooral mensen met een rookgeschiedenis en keert vaak snel terug na chemotherapie. Artsen weten dat niet alle kleincellige longkankers zich hetzelfde gedragen, maar ze misten hulpmiddelen om te zien hoe verschillende kankerceltypes en immuuncellen binnen elke tumor zijn gerangschikt. In deze studie is een nieuwe technologie gebruikt die genactiviteit leest op duizenden kleine plekken verspreid over een tumorplaat, en zo een “moleculaire kaart” van elk monster creëert. Door dit te combineren met aangepaste computeranalyse ontdekten de onderzoekers verborgen patronen die kunnen wijzen op meer precieze, subtypspecifieke behandelingen.
Tumoren in hun context in kaart brengen
Het team analyseerde tumormonsters van 21 patiënten met kleincellig longkanker in een beperkt stadium die een operatie ondergingen voordat ze medicijnen kregen. In plaats van het weefsel te vermalen en daarmee alle ruimtelijke informatie te verliezen, pasten ze ruimtelijke transcriptomica toe: een techniek die meet welke genen op veel gedefinieerde plekken in een weefselsectie zijn aangezet. Elke plek bevindt zich in zijn oorspronkelijke positie, waardoor de onderzoekers genactiviteit kunnen koppelen aan waar kankercellen, normale cellen en immuuncellen zich fysiek bevinden. Ze voegden twee belangrijke hulpmiddelen toe: een nieuwe “Edgeindex”-score om te kwantificeren hoe diep tumorcellen in aangrenzend weefsel infiltreren, en een artificieel neuraal netwerk—een vorm van machine learning—om automatisch aan te geven welke plekken tumor bevatten en welke niet.
Verschillende kankertypes binnen één ziekte
Kleincellig longkanker is geen eenduidige ziekte maar omvat minstens vier belangrijke moleculaire subtypen, vaak aangeduid als ASCL1, NEUROD1, POU2F3 en YAP1, naar sleutelregelgenen die ze definiëren. Met hun ruimtelijke kaarten konden de onderzoekers zien waar elk subtype binnen tumoren domineerde en hoe hun biologie verschilde. De veelvoorkomende ASCL1- en NEUROD1-vormen waren sterk gekoppeld aan celdelingsprogramma’s, in lijn met hun reputatie als sterk prolifererende tumoren. Daarentegen waren POU2F3-regio’s gelinkt aan immuun-gerelateerde routes, terwijl YAP1-gebieden signalen vertoonden die samenhangen met stofwisseling en weefselherschikking—kenmerken die mogelijk verband houden met uitzaaiing en therapieresistentie. Omdat deze patronen ruimtelijk worden opgelost, kan de methode het werkelijke “driver”-subtype binnen een gemengde tumor identificeren, iets wat bulktesten vaak missen.
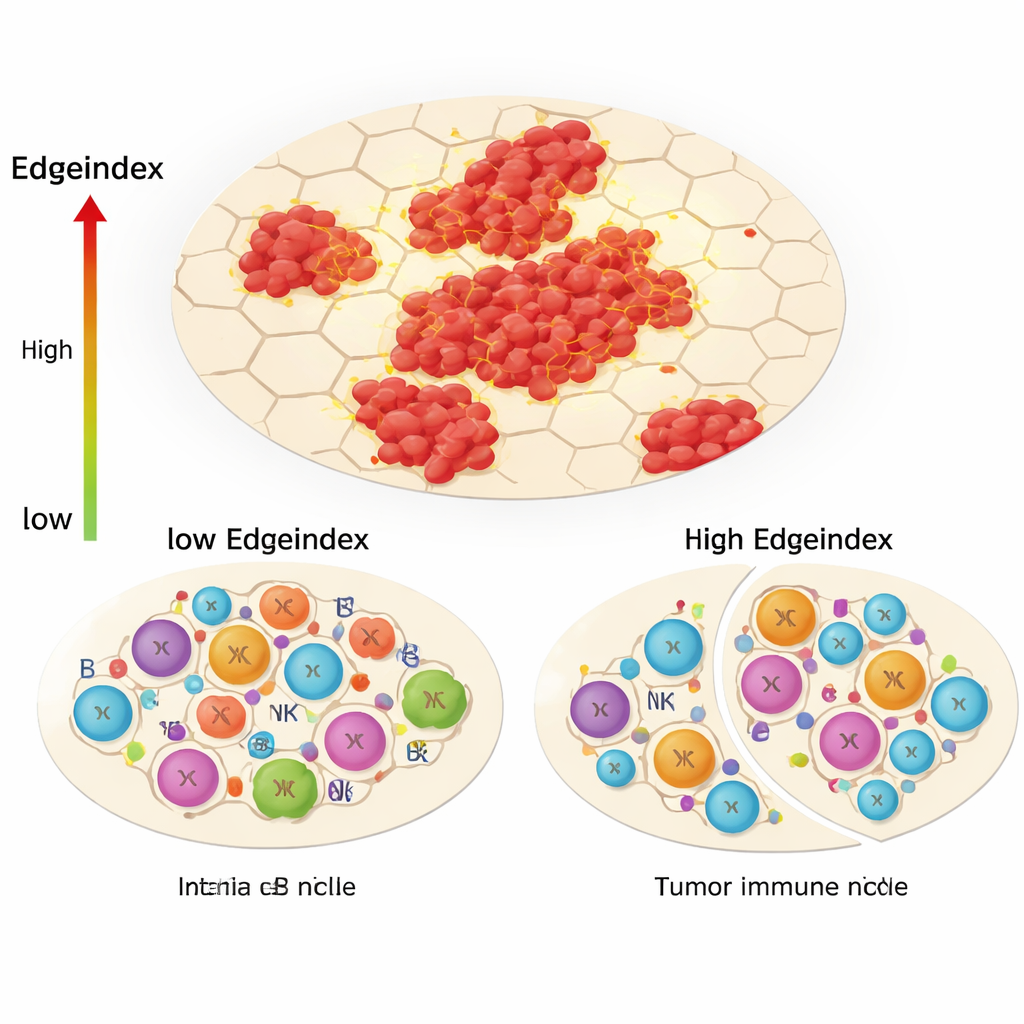
De indringende rand en de immuunverschuiving
Een van de centrale innovaties van de studie, de Edgeindex, vangt in welke mate tumorcellen zich vermengen met omliggend niet-tumorweefsel. Lage scores duiden op compacte, goed begrensde tumoren, terwijl hoge scores wijzen op verspreide eilandjes en rafelige, invasieve grenzen. Tumoren met een hoge Edgeindex waren verrijkt voor genprogramma’s die betrekking hebben op de extracellulaire matrix, metastase en celdood. Ze vertoonden ook een opvallend veranderd immuunlandschap: minder helper-T-cellen en andere adaptieve immuuncellen, maar meer aangeboren cellen zoals bepaalde natuurlijke killer-cellen en monocyten. De auteurs interpreteren dit als een “immunologisch nicheherschikking”, waarbij de tumor gerichte, precieze immuunresponsen verdringt en een minder effectieve, vooral aangeboren verdediging overlaat die de kanker niet volledig onder controle kan houden.
Verborgen diversiteit in en rond tumoren
Buiten subtype- en invasiepatronen onthulden de ruimtelijke gegevens dat zowel de kankercelpopulaties als hun omliggende micro-omgevingen intern divers waren. Door plekken binnen elke tumor te clusteren, telde het team hoeveel verschillende genexpressiebuurten er bestonden in de kankergedeeltes en in het nabijgelegen niet-tumorweefsel. Een hogere diversiteit binnenin de tumor was gekoppeld aan immuun-gerelateerde routes, terwijl bepaalde patronen in het omliggende weefsel gelinkt waren aan celdelingsactiviteit en genetische regulatie. De onderzoekers onderzochten ook hoe sterk verschillende regio’s “communiceerden” via bekende signaalmoleculen. Tumoren met intensere communicatie tussen regio’s neigden naar sterkere immuun-gerelateerde signalen, wat het idee bevestigt dat immuunactiviteit en tumorgroei ruimtelijk nauw met elkaar verweven zijn.
Het volgen van tumorontwikkeling in de tijd
Om te benaderen hoe tumorcellen veranderen naarmate de ziekte vordert, voerde het team een “pseudotijd”-analyse uit die cellen ordent langs een ontwikkelingspad op basis van hun genactiviteit. In de verschillende monsters identificeerden ze herhaaldelijk één gen, UCHL1, als centraal in deze trajecten. Hoge UCHL1-niveaus vielen samen met sterke celdelingsactiviteit in tumorpunten, terwijl lagere niveaus samenhingen met immuun- en celdoodroutes. Aangezien UCHL1 een neuronachtig eiwit is dat eerder in verband is gebracht met agressieve longkankers, versterken deze bevindingen het idee dat het een nuttig geneesmiddeldoel kan zijn, met name voor de neuro-endocriene-achtige cellen die kleincellig longkanker aandrijven.
Wat dit betekent voor patiënten
In eenvoudige bewoordingen zet deze studie platte microscoopglaasjes van kleincellig longkanker om in rijke, gelaagde kaarten die laten zien waar verschillende kankersubtypen zich bevinden, hoe agressief ze infiltreren, hoe ze met hun omgeving communiceren en hoe het immuunsysteem reageert of faalt. De nieuwe Edgeindex-score en de kaartbenadering benadrukken welke tumoren bijzonder infiltratief zijn en welke immuuncellen aan de rand aanwezig of afwezig zijn. Door deze ruimtelijke patronen te koppelen aan subtypspecifieke kwetsbaarheden—zoals geneesmiddelen die DLL3, BCL-2, AURKA, IGF-1R/PARP of immuuncheckpoints richten—brengt het werk het veld dichter bij het matchen van elke patiënt met een op maat gemaakte behandelingsstrategie. Hoewel deze hulpmiddelen nog in grotere studies getest moeten worden, bieden ze een blauwdruk voor preciezere en mogelijk effectievere therapieën bij een kankertype dat dringend betere opties nodig heeft.
Bronvermelding: Xie, T., Tang, L., Fan, G. et al. Spatial transcriptomics reveals molecular heterogeneity and subtype-specific therapeutic targets in small cell lung cancer. npj Precis. Onc. 10, 81 (2026). https://doi.org/10.1038/s41698-025-01243-7
Trefwoorden: kleincellig longkanker, ruimtelijke transcriptomica, tumorheterogeniteit, tumor-immuunmicro-omgeving, precisie-oncologie