Clear Sky Science · nl
Computationele pathologiekenmerken van immuunarchitectuur voorspellen klinisch relevante uitkomsten bij kleincellig longkanker (SCLC)
Waarom de lijfwachtcellen ertoe doen bij longkanker
Kleincellig longkanker is een van de meest agressieve vormen van longkanker: het verspreidt zich vaak snel en keert na behandeling terug. Artsen kunnen tumoren onder de microscoop zien, maar de fijnmazige patronen waarin kankercellen en immuuncellen naast elkaar liggen zijn te complex om met het blote oog te beoordelen. Deze studie introduceert een computergebaseerde methode genaamd PhenopyCell die die verborgen patronen uit routinebiopten leest en gebruikt om te voorspellen hoe lang patiënten naar verwachting zullen leven en hoe goed ze mogelijk op chemotherapie reageren. Voor patiënten en families kan zulke informatie in de toekomst helpen om behandelingen op maat te maken in plaats van te vertrouwen op een one-size-fits-all aanpak.
Dieper kijken naar een dodelijke longkanker
Kleincellig longkanker is goed voor ongeveer 15% van de longkankers, maar veroorzaakt een groot deel van de sterfte omdat het snel groeit en uitzaait. Meestal wordt het ingedeeld in “gelimiteerde” ziekte, die binnen één bestralingsterrein past, en “extensieve” ziekte, die zich verder heeft verspreid. De standaard eerstelijnsbehandeling is krachtige chemotherapie op basis van platinum, soms gecombineerd met immunotherapie. Veel tumoren lijken aanvankelijk te smelten, maar de kanker keert vaak binnen een jaar terug en minder dan één op de tien patiënten overleeft op lange termijn. Huidige tests op basis van tumorgrootte, uitzaaiingen en basale microscopische kenmerken verklaren niet waarom sommige patiënten beter reageren op dezelfde medicijnen dan anderen.
Computers leren tumornuurtjes lezen
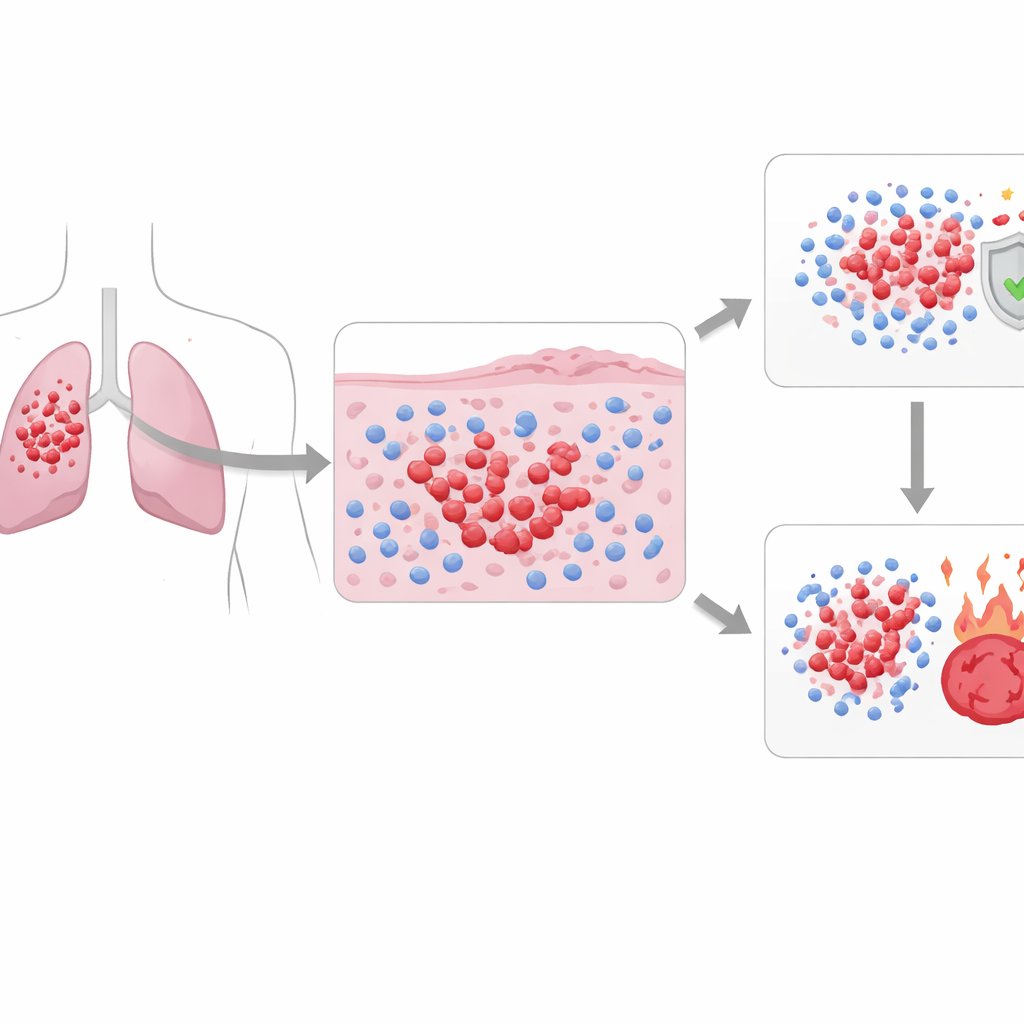
De onderzoekers bouwden PhenopyCell om standaard gekleurde weefselsnedes om te zetten in een gedetailleerde kaart van cel-“buurten”. Met bestaande deep-learningtools leerden ze eerst een computer individuele tumorcellen en immuuncellen te vinden en te markeren op digitale afbeeldingen van biopten van 281 patiënten behandeld in drie Amerikaanse centra. Vervolgens verdeelden ze elke snede in tumor-, nabijgelegen weefsel- en verre niet-tumorregio’s en berekenden ze meer dan honderd numerieke kenmerken. Deze kenmerken beschrijven bijvoorbeeld hoe dicht immuuncellen rond tumorklauwen liggen, hoe ver immuuncellen van kankercellen verwijderd zijn, hoe divers de mix van cellen is en hoe regelmatig cellen over de snede zijn geordend.
Verborgen patronen gekoppeld aan overleving en medicijnrespons
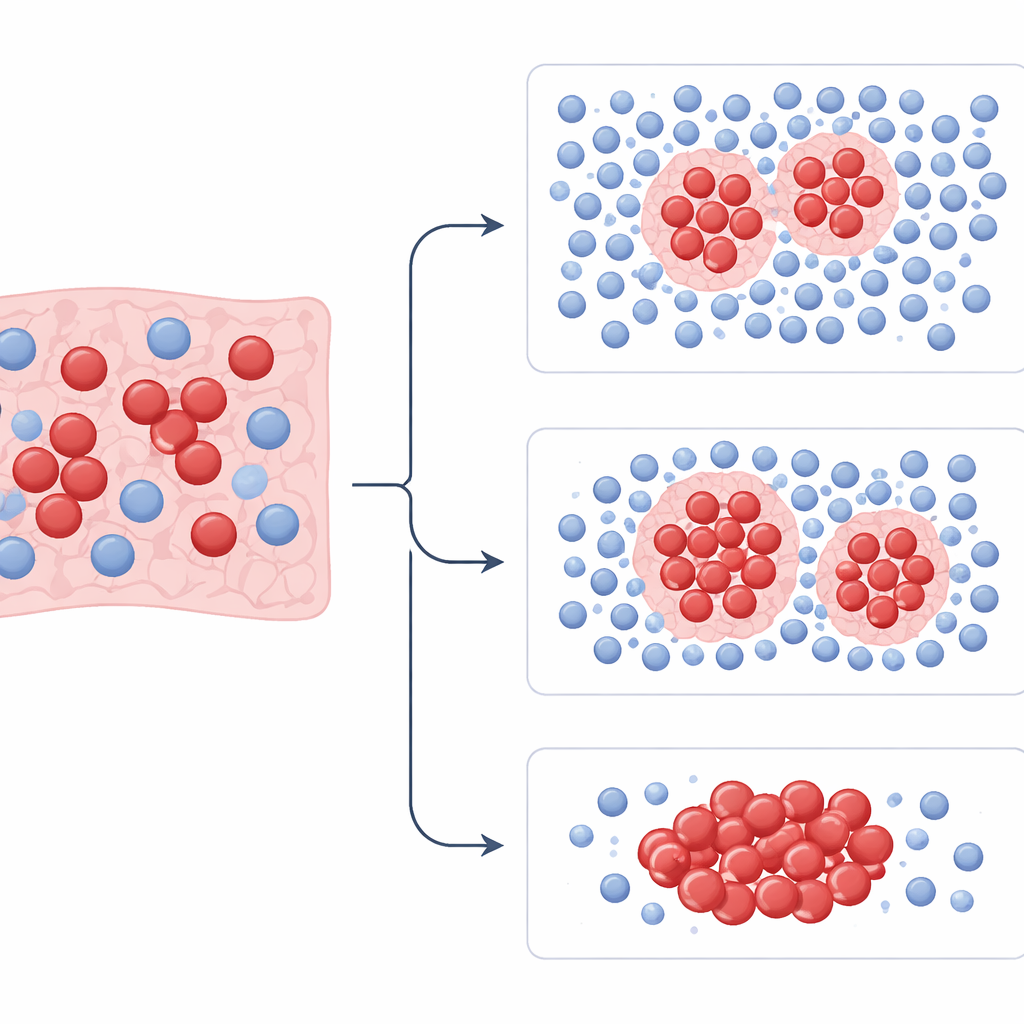
Met deze metingen trainde het team modellen om patiënten in hogere- en lagere-risicogroepen te scheiden en om te voorspellen wie op platinumchemotherapie zou reageren. Ze trainden de modellen op de gevallen van één ziekenhuis en testten ze daarna op patiënten uit de andere twee ziekenhuizen. In alle datasets waren de door PhenopyCell vastgelegde patronen sterk gerelateerd aan de totale overleving en aan de vraag of chemotherapie werkte. Patiënten waarvan de tumoren veel georganiseerde pockets van immuuncellen zagen die tumorklauwen strak omringen, leefden doorgaans langer. Patiënten met verspreide of schaarse immuuncellen en sterk ongelijk verdeelde tumorcellen hadden vaker een agressievere aandoening en slechte uitkomsten. Deze verbanden bleven bestaan na correctie voor leeftijd, geslacht en andere klinische factoren, en ze werden gezien zowel in gelimiteerde als in extensieve stadia van de ziekte.
Voorbij zwarte dozen en routinematige microscoopcontroles
De studie vergeleek PhenopyCell ook met nieuwere “foundation” kunstmatige-intelligentie-modellen en met traditionele maatstaven voor immuuncellen, de zogenaamde tumorinfiltrerende lymfocyten. Sommige grote deep-learningmodellen bereikten hoge nauwkeurigheid in de oorspronkelijke trainingsgroep maar presteerden inconsistent wanneer ze op externe patiënten werden getest, wat vragen oproept over stabiliteit. Eenvoudige telmethoden voor immuuncellen, zowel door de computer geschat als door een patholoog beoordeeld, voorspelden de overleving ook niet betrouwbaar. Daarentegen bood PhenopyCell’s focus op de ruimtelijke ordening van immuun- en tumorcellen — niet alleen op hun aantal — meer betrouwbare en makkelijker te interpreteren signalen. De kenmerken die het gebruikt zijn direct te relateren aan biologische concepten zoals immuuxclusie, gebieden van afgestorven weefsel en variërende tumorvormen.
Wat dit voor patiënten zou kunnen betekenen
Voor niet-specialisten is de kernboodschap dat de “architectuur” van een tumor — hoe kankercellen en de lijfverdedigers het strijdveld innemen — belangrijke aanwijzingen bevat over hoe de ziekte zich zal gedragen en hoe ze op behandeling zal reageren. PhenopyCell laat zien dat deze aanwijzingen uit precies dezelfde routinebiopsies gehaald kunnen worden die al in de standaardzorg worden genomen, zonder extra ingrepen. Hoewel de studie retrospectief is en grotendeels gebaseerd op patiënten die alleen chemotherapie kregen, suggereert ze dat toekomstige hulpmiddelen artsen kunnen helpen bepalen welke patiënten het hoogst risico lopen, wie baat kan hebben bij agressievere of nieuwe therapieën en wie onnodige bijwerkingen zou kunnen vermijden. Grotere, prospectieve studies, vooral bij patiënten die moderne immunotherapieën krijgen, zijn nodig voordat zo’n systeem dagelijkse beslissingen kan sturen, maar dit werk effent een duidelijke weg naar meer gepersonaliseerde zorg bij kleincellig longkanker.
Bronvermelding: Barrera, C., Jain, P., Corredor, G. et al. Computational pathology features of immune architecture predict clinically relevant outcomes in small-cell lung cancer (SCLC). npj Precis. Onc. 10, 119 (2026). https://doi.org/10.1038/s41698-025-01225-9
Trefwoorden: kleincellig longkanker, computationele pathologie, tumormicro-omgeving, immuuncelarchitectuur, voorspelling van behandelingsrespons