Clear Sky Science · nl
Het ontcijferen van hersenmetastasen bij epitheliale eierstokkanker: multimodale analyse en potentiële biomarkers
Waarom dit onderzoek ertoe doet
Eierstokkanker is al een gevaarlijke ziekte, maar bij een klein aantal vrouwen verschijnt ze later op een veel kwetsbaardere locatie: de hersenen. Deze hersenmetastasen zijn zeldzaam maar vaak dodelijk, en artsen hebben nog weinig manieren om te voorspellen wie risico loopt of wat de beste behandeling is. Deze studie volgt die reis van bekken naar hersenen op moleculair niveau, met moderne DNA- en RNA-instrumenten om te begrijpen hoe eierstokkankercellen zich aanpassen aan de hersenen en om vroege waarschuwingssignalen te identificeren die ooit kunnen helpen bij meer gerichte zorg.
Van een veelvoorkomende kanker naar een zeldzame hersendreiging
Epitheliale eierstokkanker is de dodelijkste gynaecologische kanker in ontwikkelde landen. De meeste patiënten reageren aanvankelijk op chirurgie en chemotherapie, maar ongeveer 80 procent ziet de ziekte uiteindelijk terugkeren en resistent worden tegen medicijnen. Recidieven blijven meestal binnen de buik; slechts een klein deel van de vrouwen ontwikkelt afstandsspreiding, bijvoorbeeld naar de hersenen. Naarmate behandelingen verbeteren en vrouwen langer leven, is er meer tijd voor losgeraakte kankercellen om de hersenen te zaaien, en artsen zien deze metastasen steeds vaker. Zodra hersenmetastasen optreden, daalt de gebruikelijke overleving tot onder een jaar, wat het belang van inzicht in hoe en waarom dit gebeurt onderstreept.
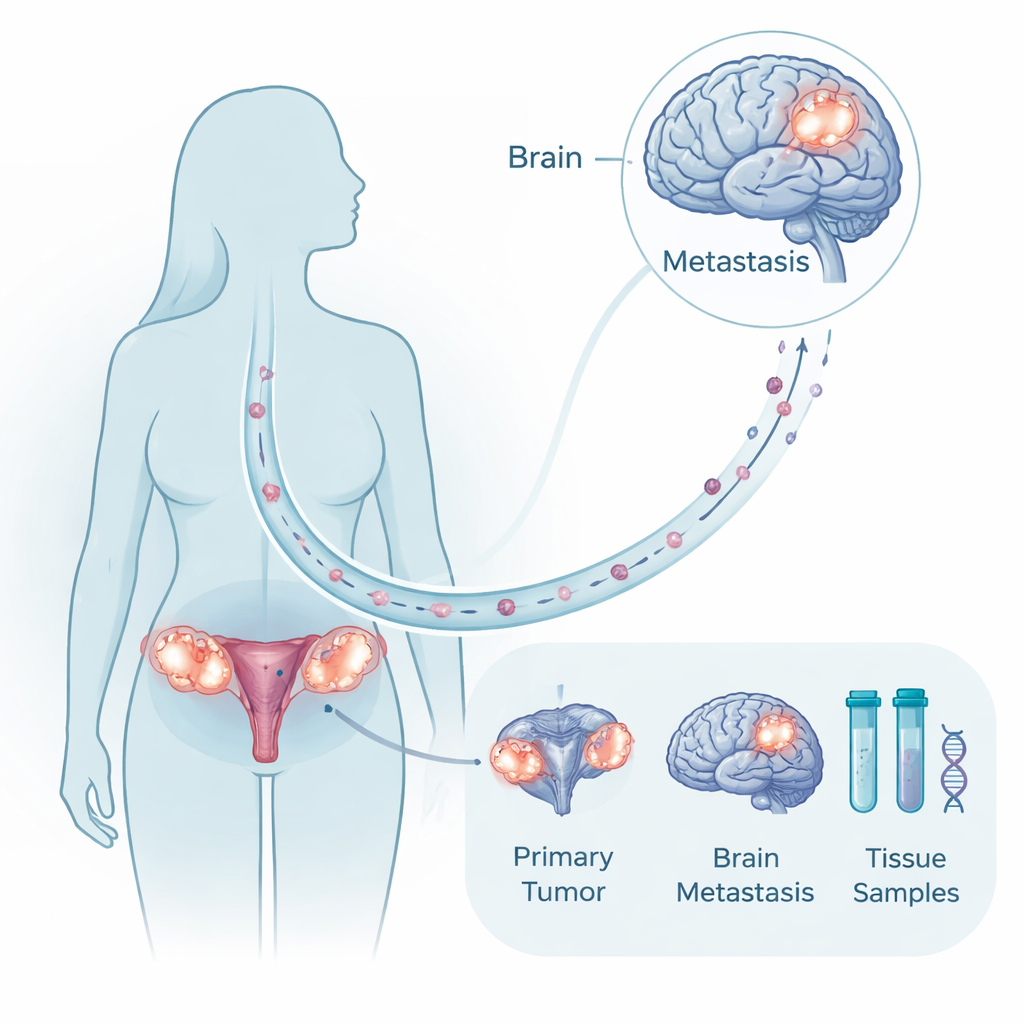
Een zeldzame maar waardevolle weefselsverzameling
Aangezien hersenchirurgie voor veel patiënten niet mogelijk of niet passend is, is het ongewoon om tumormonsters te hebben van zowel de oorspronkelijke eierstokmassa als de overeenkomende hersenlaesie bij dezelfde vrouw. De onderzoekers verzamelden precies dit soort gepaarde materiaal van tien patiënten die over twee decennia werden behandeld, samen met vergelijkingsmonsters van gezond hersen- en eierstokweefsel en van andere, niet-hersen metastasen. Ze onderzochten tumor-DNA op mutaties en grote chromosomale veranderingen, en ze analyseerden RNA om te zien welke genen aan- of uitgezet waren. Deze multimodale aanpak stelde hen in staat te onderzoeken of hersentumoren volledig nieuwe aftakkingen zijn of nauwe verwanten van de primaire tumor, en welke moleculaire programma’s veranderen wanneer cellen zich in de hersenen vestigen.
Genetische stabiliteit, maar nieuw gedrag
De DNA-analyse toonde aan dat de oorspronkelijke eierstoktumoren en hun overeenkomstige hersenmetastasen opmerkelijk vergelijkbaar waren. Beide droegen veel van dezelfde kankerveroorzakende mutaties, vooral in een gen genaamd TP53, en deelden een algemene “monoclonale” oorsprong, wat betekent dat de hersenlaesies leken voort te komen uit dezelfde voorouderlijke kankercel. Grote DNA-toevoegsels en -verliezen kwamen iets vaker voor in hersenlaesies, maar waren niet dominant. Dit suggereert dat het niet de verwerving van een volledig nieuwe set mutaties is die de verspreiding naar de hersenen mogelijk maakt. In plaats daarvan lijkt de kritische verschuiving plaats te vinden op het niveau van genactiviteit: welke instructies uit het DNA worden afgelezen en door de kankercellen gebruikt terwijl ze zich aanpassen aan de unieke omgeving van de hersenen.
Hoe eierstoktumoren leren te overleven in de hersenen
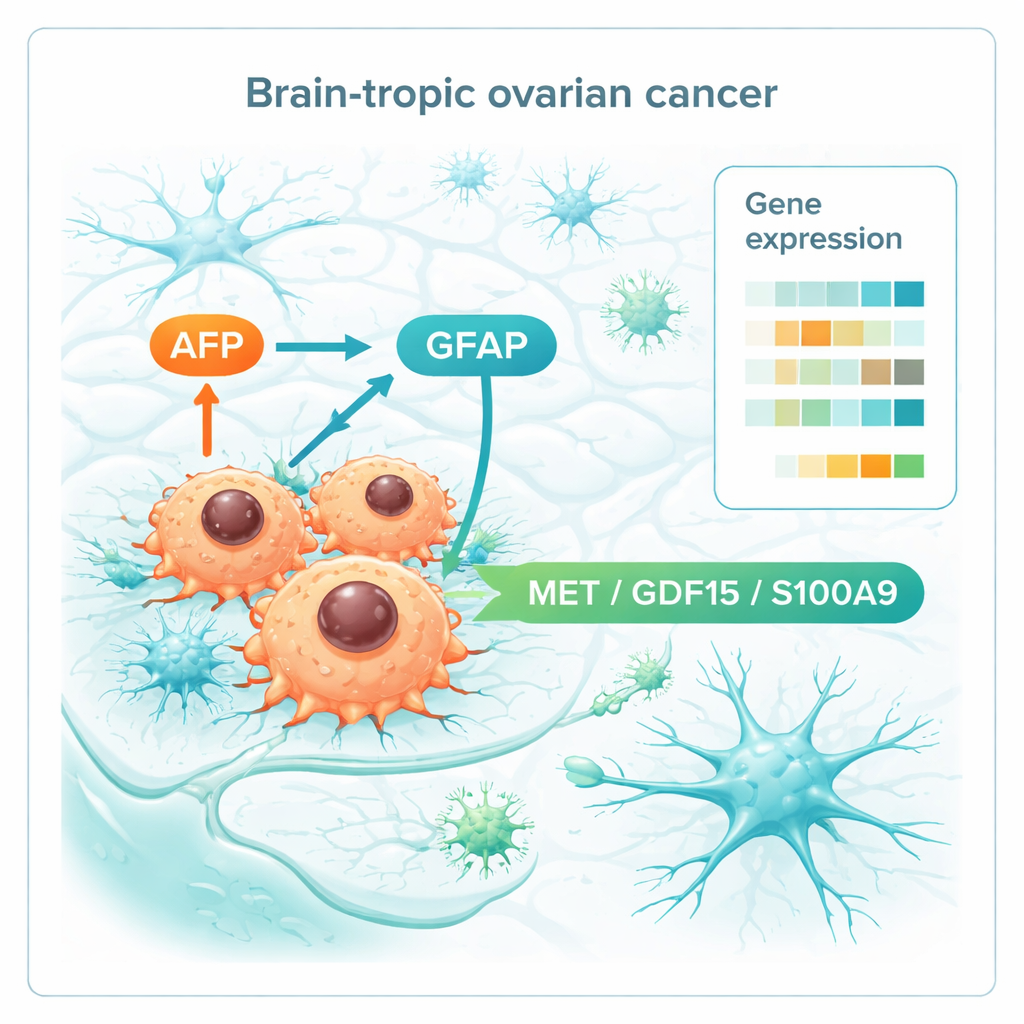
Toen het team de genactiviteit over alle weefsels vergeleek, kwam een duidelijk hersenmetastatisch profiel naar voren. Hersenklaesies toonden tekenen van agressieve groei, met activatie van celdelingsprogramma’s gedreven door bekende kankeregulatoren zoals MYC en E2F. Ze wijzigden ook de eiwitten die het weefselraamwerk vormen en herstructureren, wat cellen helpt het hersenweefsel binnen te dringen en zich te verankeren. Opvallend was dat sommige genen die aan zenuw- en gliacellen zijn gekoppeld werden geactiveerd, wat suggereert dat eierstokkankercellen gedeeltelijk hersencellen nabootsen om erin te passen. Onder de meest opvallende bevonden zich AFP, meestal actief in de foetus en bepaalde tumoren, en GFAP, een kenmerkend eiwit van steuncellen in de hersenen. De auteurs identificeerden ook een klein aantal genen dat al verhoogd was in de primaire eierstoktumoren van vrouwen die later hersenmetastasen ontwikkelden, maar niet in langdurige overlevers zonder hersenbetrokkenheid. Dit “premetastatische” patroon omvatte immuunmodulatie, communicatie met zenuwachtige signalen en veranderingen in de stofwisseling.
Vroege waarschuwingssignalen en moleculaire wisselwerking
Dieper gravend richtten de onderzoekers zich op moleculen die aan het celoppervlak zitten of worden uitgescheiden, omdat dit uitstekende kandidaten zijn voor bloedtesten of geneesmiddendoelwitten. Zij brachten drie spelers in kaart — MET, GDF15 en S100A9 — die consequent hoger waren zowel in primaire tumoren die naar de hersenen zouden uitzaaien als in de hersenmetastasen zelf. Deze moleculen zijn betrokken bij celmigratie, stress- en voedingssensatie, en het vormen van de immuunomgeving, wat suggereert dat ze eierstokkankercellen helpen met de hersenen te communiceren en het weefsel in hun voordeel te herschikken. Samen met AFP en GFAP vormen zij een korte lijst met potentiële biomarkers die ooit hoogrisicopatiënten kunnen aanwijzen of kunnen wijzen op geneesmiddelen die tumor–hersencommunicatie onderbreken.
Wat dit betekent voor patiënten
Voorlopig zal dit werk de behandeling niet onmiddellijk veranderen, en de auteurs geven toe dat hun patiëntengroep klein is. Toch toont de studie aan dat hersenmetastatische eierstokkankers veel van hun oorspronkelijke genetische samenstelling behouden terwijl ze herbedraden hoe hun genen worden gebruikt, en benadrukt daarmee nieuwe manieren om problemen vroeg te signaleren. Als vervolgonderzoek bevestigt dat markers zoals AFP, GFAP, MET, GDF15 en S100A9 betrouwbaar een neiging tot uitzaaiing naar de hersenen aangeven, kunnen artsen bepaalde patiënten nauwkeuriger volgen, behandelkeuzes aanpassen of geneesmiddelen testen die deze paden blokkeren. In wezen begint de studie een angstaanjagende late complicatie om te zetten in een proces dat gemeten, begrepen en uiteindelijk onderschept kan worden.
Bronvermelding: Trozzi, R., Salvi, M., Karimi, M. et al. Deciphering brain metastasis in epithelial ovarian cancer: multimodal analysis and potential biomarkers. npj Precis. Onc. 10, 83 (2026). https://doi.org/10.1038/s41698-025-01206-y
Trefwoorden: eierstokkanker, hersenmetastasen, biomarkers, genexpressie, precisie-oncologie