Clear Sky Science · nl
Gerichte immunotherapieën en nanogeneeskunde voor eierstokkanker: de weg vooruit
Waarom dit belangrijk is voor de gezondheid van vrouwen
Eierstokkanker behoort tot de dodelijkste vormen van kanker bij vrouwen, grotendeels omdat de ziekte meestal laat wordt ontdekt en behandeld met harde, niet-specifieke medicijnen. Dit overzichtsartikel onderzoekt hoe een nieuwe generatie immuun-gebaseerde behandelingen en piepkleine magnetische deeltjes, zogenaamde magnetische nanodeeltjes, de zorg voor eierstokkanker kunnen transformeren—nauwkeuriger, persoonlijker en uiteindelijk effectiever, met minder bijwerkingen.
De uitdaging van het opsporen en behandelen van eierstokkanker
Eierstokkanker groeit vaak stil. Vroege symptomen zijn vaag—opgeblazen gevoel, lichte buikklachten—en standaardbeeldvorming zoals echo’s, CT en MRI kan kleine of vroegtijdige tumoren die diep in de buik verborgen liggen missen. Tegen de tijd dat veel patiënten worden gediagnosticeerd, heeft de ziekte zich al in de buikholte verspreid, wat chirurgie bemoeilijkt en het risico op terugkeer vergroot. Chemotherapie en gerichte middelen kunnen helpen, maar ze beschadigen ook gezond weefsel en tumoren leren vaak hun effecten te ontwijken. Deze beperkingen hebben onderzoekers ertoe aangezet slimmere manieren te zoeken om eierstokkankercellen zowel op te sporen als aan te vallen.
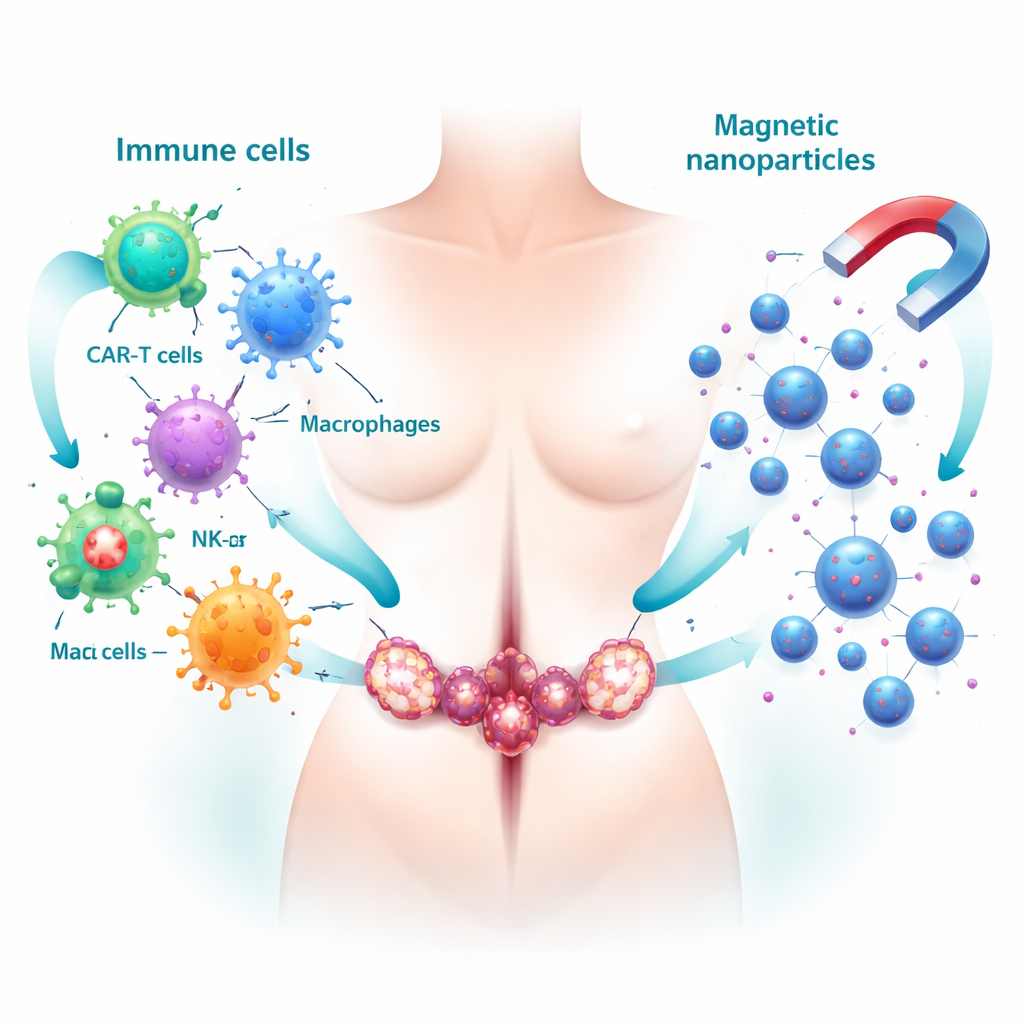
Het immuunsysteem leren tumoren op te sporen
Eén belangrijke strategie is het benutten van de eigen afweer van het lichaam. Speciaal ontworpen T-cellen, bekend als CAR-T-cellen, worden in het laboratorium zo aangepast dat ze merkers herkennen die vooral op eierstokkankercellen voorkomen. Terug in de patiënt kunnen ze die cellen gericht opzoeken en doden. Natural killer (NK)-cellen vormen een andere verdedigingslinie; ze kunnen worden uitgebreid of genetisch getuned om eierstoktumoren beter te herkennen en werken zelfs krachtiger in combinatie met gerichte antilichamen of checkpoint-remmers die de “remmen” op de immuunrespons wegnemen. Tegelijk belicht het artikel ook de keerzijde van het tumormilieu: tumor-geassocieerde macrofagen, een type immuuncel dat vaak wordt geherprogrammeerd om de tumor te beschermen in plaats van te bestrijden. Het omkeren of heropvoeden van deze cellen tot tumorbestrijders blijkt een veelbelovende manier om immunotherapie effectiever te maken.
Magnetische nanodeeltjes als slimme kankerhulpmiddelen
De tweede pijler van het overzicht is nanogeneeskunde, met name magnetische nanodeeltjes op basis van ijzerhoudende materialen. Omdat ze reageren op magneten en duidelijk zichtbaar zijn op MRI-scans, kunnen ze fungeren als piepkleine, bestuurbare instrumenten in het lichaam. Door hun oppervlak te coaten met moleculen die eierstokkankermarkers herkennen, kunnen deze deeltjes tumoren opsporen en chemotherapie rechtstreeks daarheen brengen, waardoor de medicijnconcentratie in de tumor sterk stijgt terwijl gezonde organen worden gespaard. Onder een wisselend magnetisch veld kunnen dezelfde deeltjes een tumor veilig verhitten tot ongeveer 42–45 °C—heet genoeg om kankercellen te verzwakken of te doden en ze gevoeliger te maken voor standaardmiddelen, maar niet zo heet dat het omliggend gezond weefsel ernstig schaadt.
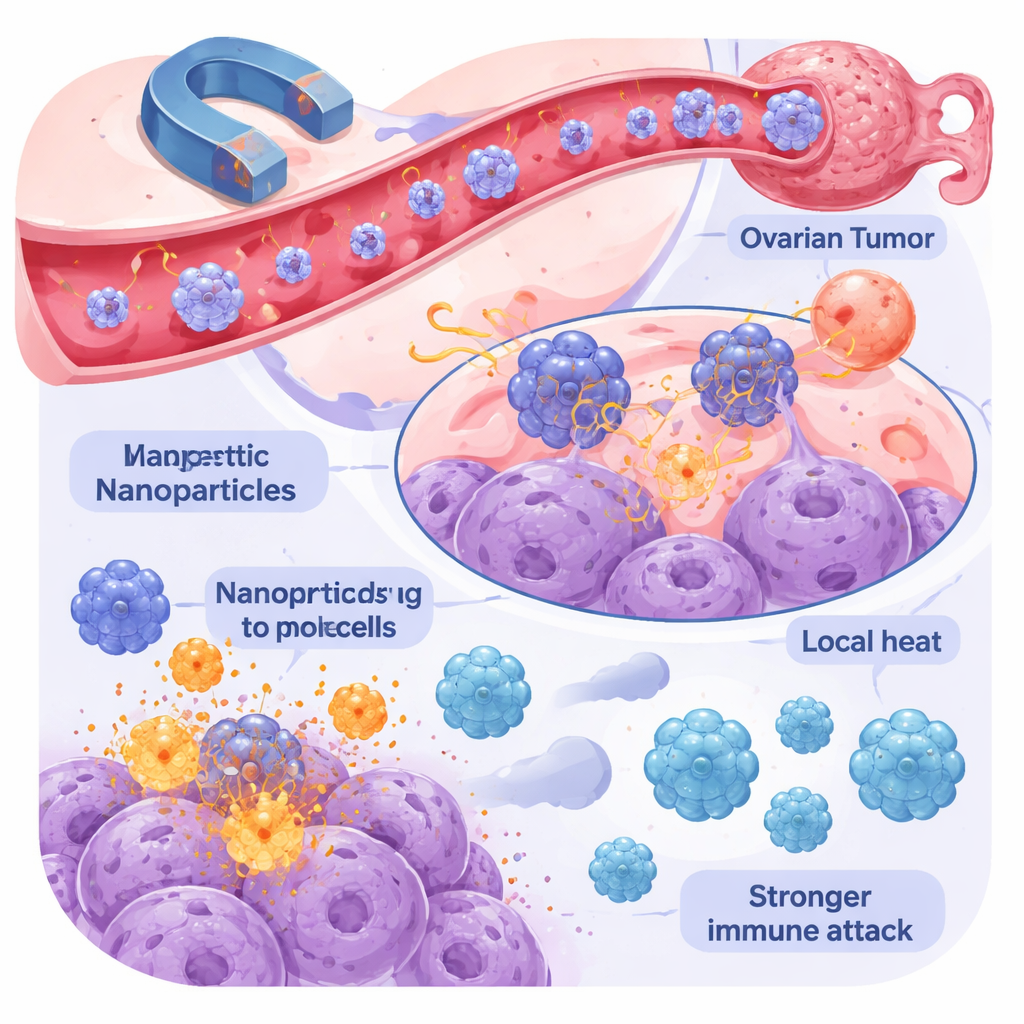
Combineren van warmte, medicijnen en immuniteit
De echte opwinding ontstaat door immunotherapie te combineren met magnetische nanogeneeskunde. Wanneer magnetische nanodeeltjes medicijnen afleveren, warmte genereren of helpen tumoren te vernietigen, sterven kankercellen op een manier die “gevaarssignalen” en tumorfragmenten in de lokale omgeving vrijkomen, waardoor de tumor als het ware verandert in zijn eigen vaccin. Dit kan T-cellen en NK-cellen aantrekken en activeren, waardoor checkpointremmers en CAR-gebaseerde therapieën effectiever worden. Onderzoekers gebruiken nanodeeltjes ook om immuunstimulerende moleculen en antilichamen rechtstreeks in de tumor te vervoeren, waardoor hun lokale concentratie stijgt en systemische bijwerkingen afnemen. Vroege dierstudies tonen scherpere tumorkrimp, minder terugkeer en sterkere infiltratie door immuuncellen wanneer deze benaderingen worden gecombineerd.
Obstakels, veiligheid en de weg voorwaarts
Ondanks deze vooruitgang blijven er uitdagingen. Eierstoktumoren zijn ongelijk verdeeld en verspreid in de buik, wat een gelijkmatige verdeling van nanodeeltjes bemoeilijkt, en niet-afbreekbare deeltjes kunnen zich ophopen in organen zoals de lever als ze niet zorgvuldig worden ontworpen. Dicht littekenachtig weefsel rond tumoren kan diepe penetratie blokkeren. Het artikel bespreekt technische oplossingen—zoals biologisch afbreekbare coatings, camouflage met ‘eigen’ celmembranen en enzymen die tumorbarrières verzachten—die veiligheid, targeting en klaring verbeteren. Het benadrukt ook het belang van behandeling op maat van ieders genetica en immuunprofiel en het gebruik van geavanceerde beeldvorming om te volgen waar nanodeeltjes naartoe gaan en hoe goed ze werken.
Wat dit voor patiënten zou kunnen betekenen
Praktisch gezien wijst het in dit overzicht beschreven werk op een toekomst waarin eierstokkanker eerder wordt gevonden en zachter maar krachtiger wordt behandeld. Magnetische nanodeeltjes zouden medicijnen en warmte precies daarheen kunnen geleiden waar ze nodig zijn, terwijl immuun-gebaseerde therapieën zorgen voor een aanhoudende, lichaamsbrede aanval op eventuele resterende kankercellen. Als komende klinische onderzoeken de veelbelovende resultaten uit laboratorium- en dierstudies bevestigen, kunnen vrouwen met eierstokkanker profiteren van behandelingen die gerichter, persoonlijker en veel minder belastend zijn dan de huidige standaardtherapieën.
Bronvermelding: Li, Y., Dou, J., Fu, Y. et al. Targeted immunotherapies and nanomedicines for ovarian cancer: the way forward. npj Precis. Onc. 10, 80 (2026). https://doi.org/10.1038/s41698-025-01204-0
Trefwoorden: eierstokkanker, immunotherapie, nanogeneeskunde, magnetische nanodeeltjes, gerichte medicijnafgifte