Clear Sky Science · nl
Methoden voor gerandomiseerde, geblindeerde, gecontroleerde evaluatie van veronderstelde ziekte-interventies in multilab, preklinische beoordelingsnetwerken
Waarom dit ertoe doet voor dagelijkse gezondheid
Veel veelbelovende medische behandelingen lijken krachtig in dierstudies maar falen vervolgens in grote, dure klinische onderzoeken. Dit artikel laat concreet zien hoe wetenschappers die vroege dierproeven kunnen herontwerpen zodat de uitkomsten betrouwbaarder zijn en beter voorspellen wat bij echte patiënten zal gebeuren—met beroerte als testcase. 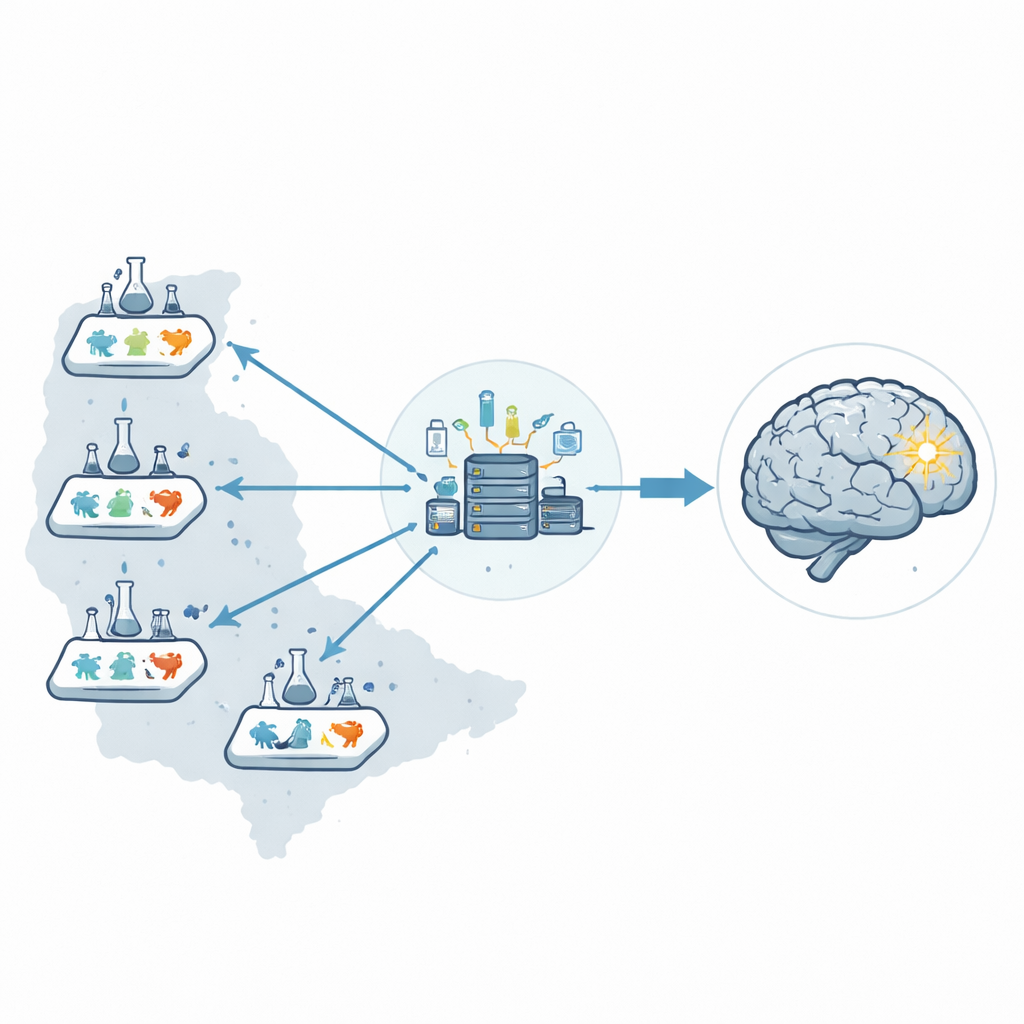
Een netwerk opbouwen in plaats van één laboratorium
In plaats van te vertrouwen op één laboratorium richtten de onderzoekers een preklinisch netwerk van zes laboratoria op in de Verenigde Staten, het Stroke Preclinical Assessment Network. Een centraal coördinatiecentrum beheerde de gehele operatie: het verzenden van gecodeerde medicijnvials, het willekeurig toewijzen van behandelingen, het ontvangen van alle gegevens en het uitvoeren van de statistiek. Door die rollen te scheiden van de mensen die de operatie uitvoerden of uitkomsten beoordeelden, verminderden ze de kans dat menselijke verwachtingen de resultaten subtiel zouden beïnvloeden.
Eerlijkheid en verbergen in de praktijk brengen
Om de regels van een goed klinisch onderzoek te imiteren, werd elk dier bij binnenkomst in een laboratorium geregistreerd, gemarkeerd en gevolgd. Behandelingen waren verborgen in identieke vials zodat chirurgen niet konden zien of het om echte middelen of placebo’s ging tijdens het opwekken van de beroerte en het toedienen van therapie. Een gestructureerd randomisatieplan zorgde dat mannelijke en vrouwelijke dieren, verschillende beroertemodellen en alle zes locaties gelijkmatig bijdroegen aan elke behandelgroep. Zelfs als een dier stierf of een procedure mislukte, bleef het in het dossier staan zodat verliezen niet stilletjes konden worden genegeerd, wat helpt verborgen vertekeningen te voorkomen.
Behandelingen testen in realistische beroertemodellen
Het netwerk gebruikte vijf verschillende knaagdiermodellen die samen belangrijke aspecten van menselijke beroerte omvatten, waaronder leeftijd, hoge bloeddruk en door dieet veroorzaakte obesitas. Beroerte werd op dezelfde manier op alle locaties opgewekt door kort een grote hersenslagader af te sluiten en vervolgens de bloedstroom te herstellen—vergelijkbaar met moderne trombectomieprocedures bij mensen. Dieren ontvingen een van zes kandidaat-beschermende behandelingen of een overeenkomende controle. Het team volgde hen vervolgens met eenvoudige bewegingsproeven, zoals hoe ze een hoek omdraaiden of over een raster liepen, en met hersenscans om de grootte van het letsel gedurende 30 dagen te meten.
Geblindeerde scorering, gedeelde data en slimme statistiek
Om oordelen onbevooroordeeld te houden, werden gedragstests op video opgenomen en geüpload naar een centraal archief. Deze video’s, ontdaan van identificerende informatie, werden naar getrainde beoordelaars in andere laboratoria gestuurd, die ze beoordeelden zonder te weten welke behandeling het dier had gekregen of waar het was getest. MRI-beelden werden door een geautomatiseerde analysemethode geleid die de hersenen en het letselgebied met minimale menselijke tussenkomst segmenteerde. Alle resultaten gingen naar een multi-arm, multi-stage statistisch ontwerp waarmee meerdere behandelingen parallel getest konden worden: zwakke of duidelijk ineffectieve kandidaten konden vroegtijdig worden gestopt, terwijl veelbelovende kandidaten doorgingen naar latere fasen. 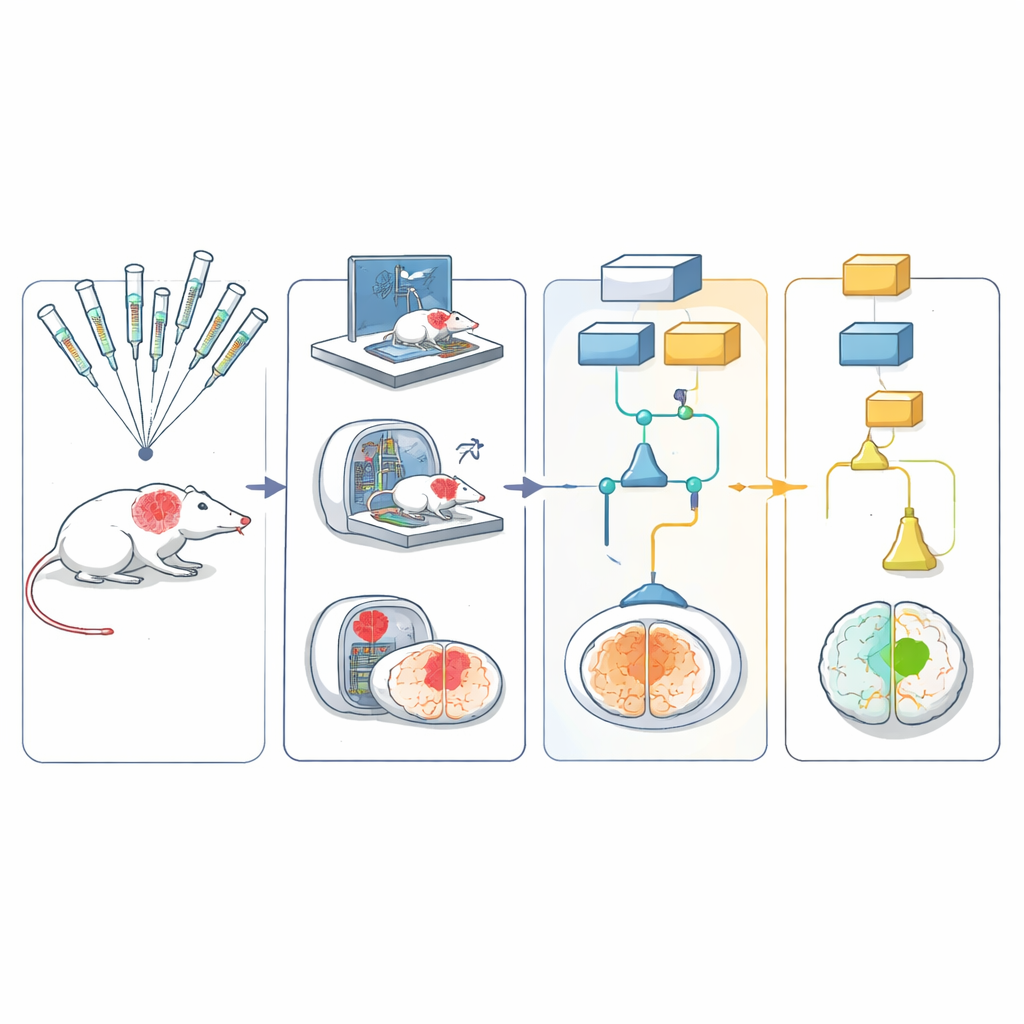
Wat de resultaten lieten zien over beroerdetherapieën
Over vier fasen en 2.615 dieren bleek het systeem werkbaar, zelfs tijdens de verstoringen door de COVID-19-pandemie. De methoden hielden behandelgroepen consequent in balans, minimaliseerden doseringsfouten en toonden verbetering van de datakwaliteit naarmate locaties de leercurve doorliepen. Uiteindelijk werden vijf van de zes behandelingen uitgesloten, terwijl één—urinezuur, een vrije-radicalenvanger—aan de vooraf vastgestelde grens voor voordeel voldeed. Tegelijkertijd onthulde het werk beperkingen van sommige populaire modellen, zoals zeer hoge sterftecijfers bij oude muizen, wat suggereert dat ze mogelijk onpraktisch of niet realistisch zijn voor toekomstige studies.
Groot plaatje: een sjabloon voor betrouwbaardere preklinische wetenschap
Voor een niet-specialistische lezer is de kernboodschap dat hoe we behandelingen bij dieren testen net zo belangrijk is als wat we testen. Door de waarborgen van moderne klinische onderzoeken—randomisatie, blindering, volledige verantwoording van elk subject en zorgvuldige statistiek—naar dieronderzoek over te nemen, laat dit netwerk zien dat vroege studies zowel strenger als efficiënter kunnen zijn. De gedetailleerde handleiding die zij bieden kan worden aangepast aan andere ziekten en biedt een route naar labbevindingen die bestand zijn tegen replicatie en artsen, patiënten en financiers meer vertrouwen geven dat een therapie echt kans maakt in de kliniek.
Bronvermelding: Lamb, J., Nagarkatti, K., Diniz, M.A. et al. Methods for randomized, blinded, controlled evaluation of putative disease interventions in multilaboratory, preclinical assessment networks. Lab Anim 55, 74–82 (2026). https://doi.org/10.1038/s41684-026-01683-z
Trefwoorden: beroerte, preklinische proeven, diermodellen, onderzoekszorgvuldigheid, multicenterstudies