Clear Sky Science · nl
PiggyBac-gemedieerde transgenese en CRISPR–Cas9-knockout in de grote wasmot, Galleria mellonella
Een kleine rups met grote medische potentie
Stel je voor dat je nieuwe antibiotica test of gevaarlijke infecties bestudeert zonder muizen of andere zoogdieren te gebruiken. De larven van de grote wasmot, Galleria mellonella, doen zich steeds vaker voor als een goedkope, ethisch aantrekkelijkere vervanger voor zulke experimenten. Deze studie laat zien hoe wetenschappers een belangrijke stap vooruit hebben gezet door deze rupsen dezelfde genetische gereedschappen te geven die fruitvliegen en zebravissen zo krachtig maakten voor biomedisch onderzoek.
Waarom deze insect van belang is voor de menselijke gezondheid
Galleria mellonella-larven bootsen verrassend goed na hoe menselijke lichamen reageren op ziekteverwekkers. Ze kunnen worden gehouden bij 37 °C—onze lichaamstemperatuur—en zijn vatbaar voor een breed scala aan medisch relevante bacteriën en schimmels. Wanneer ze ziek worden, verkleuren ze door een proces dat melanisatie heet, wat onderzoekers een zichtbare indicator van gezondheid geeft. Omdat het ongewervelden zijn, vallen ze buiten veel van de wettelijke en ethische drempels die gelden voor gewervelde dieren, en ze zijn goedkoop in grote aantallen te kweken. De larven blijken zelfs in staat om gangbare kunststoffen af te breken, wat ook mogelijkheden in milieugerelateerd onderzoek suggereert.
Het ontbrekende genetische gereedschapskistje
Ondanks deze voordelen ontbraken bij de wasmotlarven de verfijnde genetische methoden die beschikbaar zijn in klassieke laboratoriumdieren. In het afgelopen decennium hebben verschillende teams het genoom van de mot ontrafeld en zijn actieve genen en eiwitten in kaart gebracht, maar onderzoekers konden nog niet eenvoudig genen aan- of uitzetten of nuttige markers toevoegen. Dat gebrek beperkte wat met het model kon worden gedaan—bijvoorbeeld het maken van dieren die oplichten bij infectie, of het verwijderen van specifieke genen om te testen hoe die immuunsystemen beïnvloeden. Het huidige artikel pakt dit probleem direct aan door twee krachtige gen-bewerkingssystemen, bekend als PiggyBac en CRISPR–Cas9, aan te passen voor gebruik in Galleria mellonella.
Rupsen bouwen die oplichten
Het team onderzocht eerst het tijdsverloop van vroege embryo-ontwikkeling bij de mot en vond een periode van ongeveer zes uur nadat de eieren gelegd zijn waarin alle delende kernen nog een gemeenschappelijk interieur delen. Door in deze periode DNA in te brengen, kan nieuw genetisch materiaal in alle latere weefsels terechtkomen, inclusief toekomstige sperma en eieren. Met dit venster als uitgangspunt introduceerden de onderzoekers DNA-constructen op basis van het PiggyBac-transposon, een "knip-en-plak"-element dat grote stukken DNA in het genoom invoegt. Na het testen van verschillende helperplasmiden identificeerden ze een versie met een hyperactief PiggyBac-enzym die met succes transgene lijnen produceerde. Deze larven brachten groene en rode fluorescerende eiwitten tot expressie in uiteenlopende lichaamsweefsels, en DNA-analyse toonde aan dat de genetische cassette in een onschadelijk stuk tussen natuurlijke genen was terechtgekomen.
Cellen volgen en genen uitzetten
Vervolgens maakten de auteurs meer gespecialiseerde rapportagelijnen. Eén construct labelde een structureel eiwit genaamd tubuline met groen fluorescerend eiwit om het interne skelet van de cel te benadrukken, terwijl een ander een rood merker fuseerde met een histoneiwit dat DNA in de kern wikkelt. Deze lijnen lichtten op in kenmerkende patronen in darm, vetlichaam, zijdegklieren en andere weefsels, waardoor onderzoekers celstructuren in levende of gefixeerde larven konden visualiseren. Om verder te gaan dan het toevoegen van genen en ze daadwerkelijk uit te schakelen, schakelde het team CRISPR–Cas9 in. Ze injecteerden vooraf samengestelde CRISPR-eiwit–RNA-complexen gericht op de groene fluorescerende marker in embryo’s die de rapportagecassette al droegen. Veel nakomelingen vertoonden een gedeeltelijk of volledig verlies van het groene signaal terwijl de rode oogfluorescentie bleef, en DNA-sequenering bevestigde kleine inserties en deleties op de bedoelde CRISPR-knipplaats.
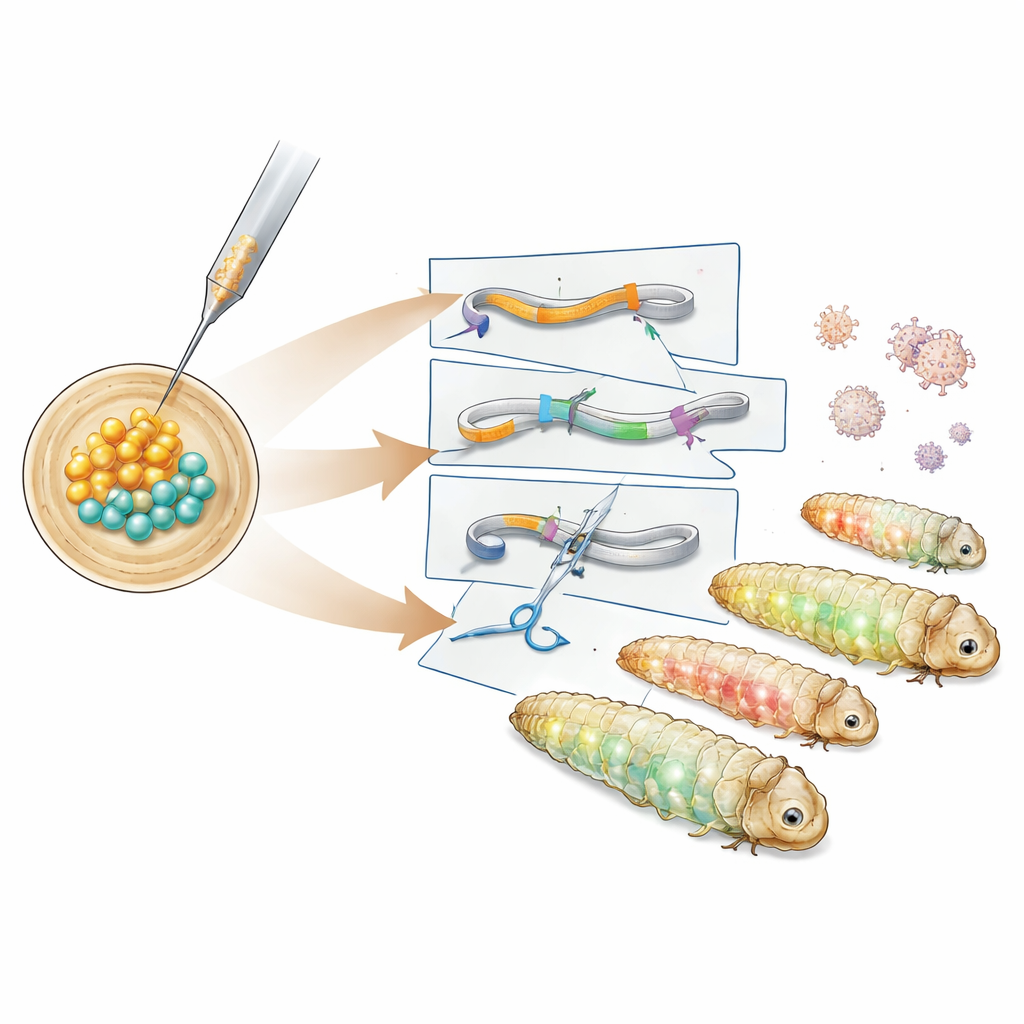
Van technische vooruitgang naar praktische impact
Hoewel de efficiëntie van zowel PiggyBac als CRISPR in deze motten nog bescheiden is vergeleken met sommige andere insecten, schetsen de auteurs duidelijke wegen voor verbetering door het afstemmen van promotoren, enzymvarianten en injectiestrategieën. Zelfs in de huidige vorm is de gereedschapskist krachtig genoeg om stabiele lijnen te genereren die belangrijke celcomponenten visualiseren of gerichte genknockouts dragen. Voor niet-specialisten is het grote plaatje dat Galleria mellonella nu bijna even flexibel kan worden gemanipuleerd als beter bekende laboratoriumdieren. Dat betekent dat onderzoekers rupsen kunnen maken die over infectie rapporteren, aspecten van menselijke ziekten modelleren of nieuwe geneesmiddelen testen op manieren die sneller, goedkoper en diervriendelijker zijn, en mogelijk de afhankelijkheid van zoogdierenmodellen in de infectiebiologie en aanverwante vakgebieden verkleinen.
Bronvermelding: Pearce, J.C., Campbell, J.S., Prior, J.L. et al. PiggyBac-mediated transgenesis and CRISPR–Cas9 knockout in the greater wax moth, Galleria mellonella. Lab Anim 55, 95–102 (2026). https://doi.org/10.1038/s41684-025-01665-7
Trefwoorden: Galleria mellonella, invertebraat infectiemodel, genetische engineering, PiggyBac-transgenese, CRISPR-knockouts