Clear Sky Science · nl
Richten op kanker‑uitgedrukt EGFR met een gehumaniseerde monoklonale antilichamen
De verborgen vlaggen van kanker vinden
Kankergeneesmiddelen hebben vaak moeite een evenwicht te vinden tussen het aanvallen van tumorcellen en het sparen van gezond weefsel. Dit artikel beschrijft een nieuw in het laboratorium ontworpen antilichaam, A10 geheten, dat kankercellen die een specifieke vorm van een groeireceptor dragen kan onderscheiden van normale cellen. Door zich te richten op een structuur die vooral zichtbaar wordt wanneer deze receptor gewijzigd is of in hoge aantallen op tumorcellen voorkomt, opent A10 de deur naar therapieën die zowel krachtig als selectiever zijn dan veel huidige opties.
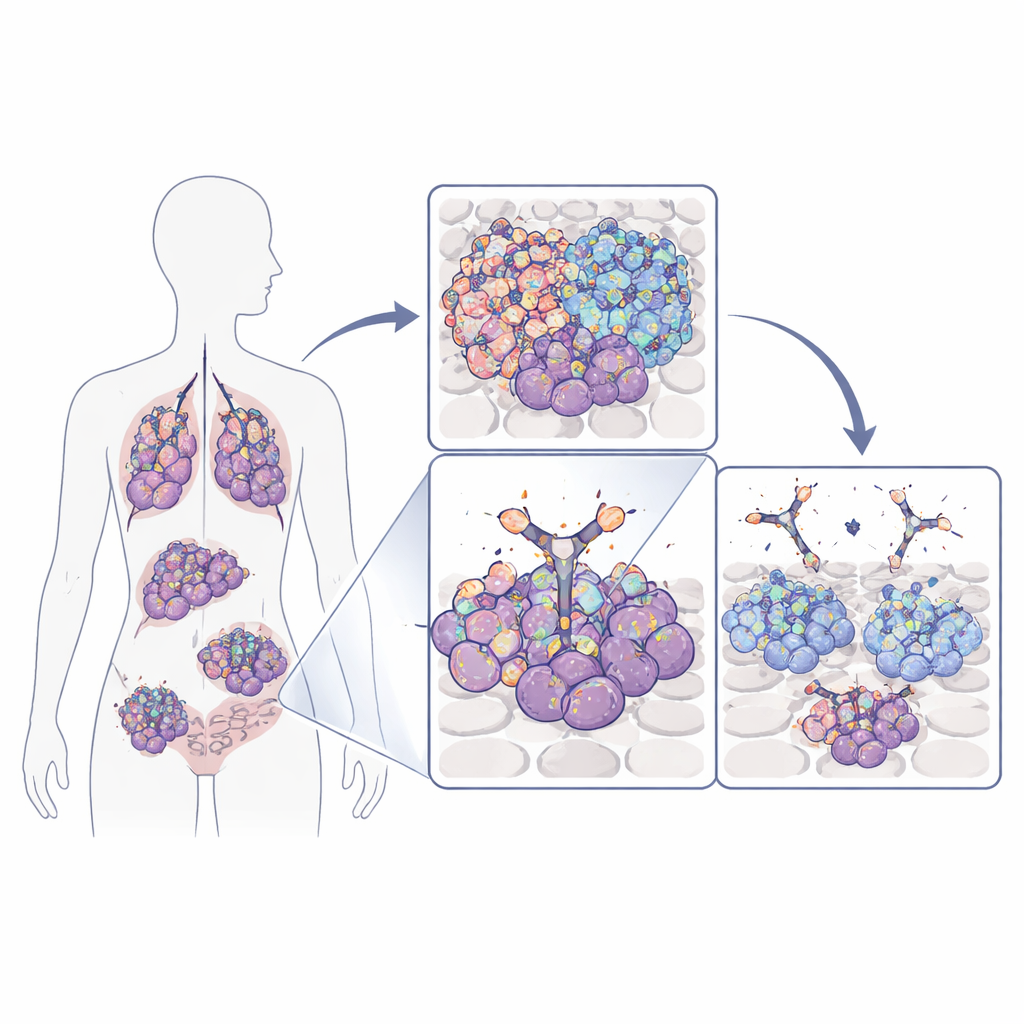
Waarom deze groeischakelaar ertoe doet
Veel tumoren, waaronder agressieve hersen-, long-, borst‑ en colorectale kankers, zijn afhankelijk van een eiwit op het celoppervlak genaamd epidermale groeifactorreceptor (EGFR) om te groeien en te overleven. Tumorcellen kunnen dit receptor verhogen door het gen te amplificeren, het te muteren of een verkorte, altijd‑actieve vorm te produceren die bekendstaat als EGFRvIII. Standaardmiddelen die EGFR blokkeren treffen vaak zowel kankercellen als normaal weefsel, omdat ze delen van de receptor herkennen die overal aanwezig zijn. Het team achter deze studie richtte zich in plaats daarvan op een kleine lus van EGFR die vooral op kankercellen duidelijk zichtbaar wordt—ofwel omdat EGFR in abnormaal hoge aantallen aanwezig is, of omdat de receptor in EGFRvIII is ingekort. Die lus werkt als een kankerspecifieke “vlag” die in principe veel veiliger kan worden aangegrepen.
Een muisantilichaam omzetten in een geneesmiddel voor mensen
De onderzoekers hadden eerder een muisantilichaam ontdekt, 40H3, dat deze blootliggende lus op kanker‑uitgedrukt EGFR herkende. Muisantilichamen kunnen echter immuunreacties veroorzaken bij herhaalde toediening aan patiënten. Om dit te voorkomen gebruikten de onderzoekers eiwit‑engineeringsmethoden om de kernbindende segmenten van 40H3 op menselijke antilichaam‑kaders over te brengen, waarmee veertien “gehumaniseerde” kandidaten werden gemaakt plus een chimeer referentiemolecuul. Toen ze deze varianten testten op kankercellen die veel EGFR produceren, binden drie versies bijzonder goed, en één—A10—stak er als sterkste binder uit terwijl het normale cellen met bescheiden EGFR‑niveaus negeerde. Over een breed paneel van tumorcellen met verschillende EGFR‑mutaties en kopieaantallen toonde A10 consequent hogere binding dan het oorspronkelijke muisantilichaam en behield het een sterke voorkeur voor kwaadaardige cellen.
Zien hoe het antilichaam zijn doel grijpt
Om te begrijpen waarom A10 zo selectief is, bepaalde het team een hoge‑resolutie 3D‑structuur van het actieve deel van het antilichaam gebonden aan de EGFR‑lus. De lus vouwt zich tot een strakke haarspeld die door een disulfidebrug wordt gestabiliseerd, en A10 omklemt deze vorm in een groef gevormd tussen zijn twee armen, met veel geladen contactpunten die het op zijn plaats vergrendelen. Vergelijking van deze structuur met bekende vormen van het volledige EGFR‑molecuul leverde een belangrijke inzicht op: in zowel de inactieve "aangebonden" als de actieve dimer‑vorm van normaal EGFR is de lus grotendeels verborgen of deels afgeschermd door aangrenzende domeinen. Dit betekent dat A10 niet gemakkelijk toegang heeft tot zijn bindingsplaats op typische, matig tot uitgedrukte receptoren. In tegenstelling daarmee ontbreekt in de kankerspecifieke variant EGFRvIII het voorste deel van de receptor, waardoor de lus sterk blootligt en toegankelijk is. De gegevens suggereren dat A10 vooral EGFR herkent tijdens bepaalde overgangsvormen en in overbevolkte of ingekorte vormen die bij voorkeur op tumorcellen voorkomen.
Het antilichaam bewapenen om tumorcellen te doden
Het herkennen van een tumor‑specifieke vlag is op zichzelf nuttig, maar de onderzoekers gingen verder door A10 om te zetten in een antilichaam‑geneesmiddelconjugaat (ADC). Ze hechtten chemisch een krachtig cel‑dodend middel, monomethyl auristatin E (MMAE), aan A10 met behulp van een linker die binnen cellen kan worden geknipt. Dit A10‑MMAE ADC bond aan kankercellen net zo goed als het onverzegelde antilichaam. In laboratoriumtesten over veel cellijnen was het ADC het meest effectief tegen tumoren met zeer hoge EGFR‑niveaus of EGFRvIII, waar A10 overvloedige bindingsplaatsen had. In deze cellen waren minuscule hoeveelheden van het conjugaat voldoende om celdood te veroorzaken. Tumorlijnen met minder A10‑doelen of een aangeboren resistentie tegen MMAE werden minder beïnvloed, en normale fibroblastcellen met wild‑type EGFR bleven ongedeerd ondanks hun gevoeligheid voor vrij MMAE. De resultaten tonen aan dat de combinatie van selectieve binding en intracellulaire vrijgave van het middel de toxiciteit scherp op kankercellen kan richten.
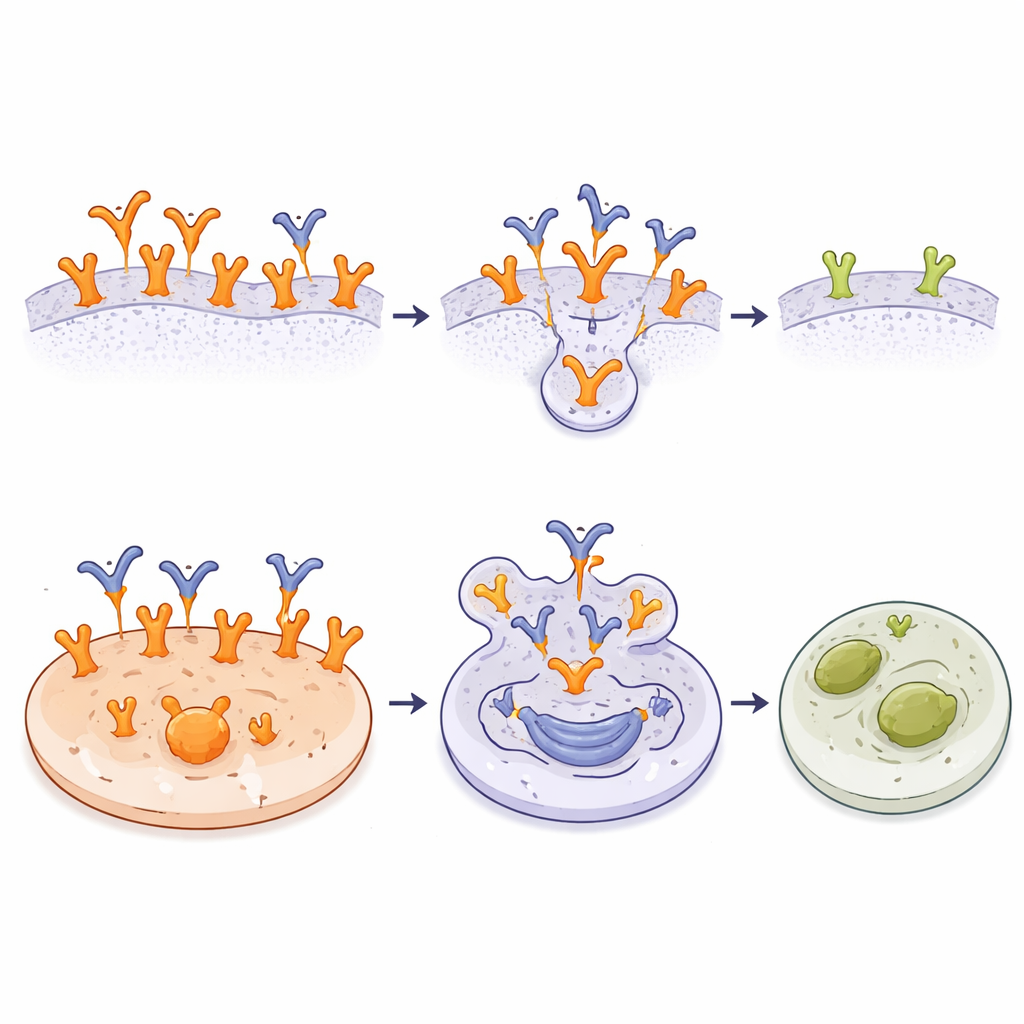
Wat dit kan betekenen voor de toekomstige kankerzorg
In eenvoudige bewoordingen laat dit werk zien dat het mogelijk is een antilichaam te bouwen dat EGFR alleen “ziet” wanneer het eruitziet en zich gedraagt als een kanker‑gedreven receptor, terwijl het grotendeels de alledaagse vorm op gezond weefsel negeert. Door precies in kaart te brengen hoe A10 een verborgen lus op EGFR vastgrijpt en aan te tonen dat een op A10 gebaseerd geneesmiddelconjugaat receptorrijke tumorcellen efficiënt kan doden en normale cellen kan sparen, biedt de studie een sterke basis voor de ontwikkeling van veiligere, sterk gerichte therapieën. Als deze bevindingen naar patiënten vertalen, zouden toekomstige behandelingen gebaseerd op A10 krachtige geneesmiddelen direct kunnen afleveren aan EGFR‑afhankelijke kankers terwijl de rest van het lichaam grotendeels ongemoeid blijft.
Bronvermelding: Costa, T.G.F., Sarnovsky, R., Zhan, J. et al. Targeting cancer expressed EGFR with a humanized monoclonal antibody. Sci Rep 16, 10814 (2026). https://doi.org/10.1038/s41598-026-46245-y
Trefwoorden: EGFR, antilichaam‑geneesmiddelconjugaat, gerichte kankertherapie, glioblastoom, EGFRvIII