Clear Sky Science · nl
Structurele en mechanistische inzichten in α2β1- en α5β1-integrinegerichte targeting door bio-engineerde extracellulaire vesikels afkomstig van longkankercellen
De verborgen boodschappers van kanker
Longkanker wordt vaak pas laat ontdekt, wanneer behandelingsopties beperkt zijn. Een veelbelovende benadering is geneesmiddelen precies aan kankercellen afleveren, zodat gezond weefsel gespaard blijft. Deze studie onderzoekt een klein natuurlijk transportsysteem — extracellulaire vesikels, of EV’s — dat kankercellen al gebruiken om signalen te versturen. Door deze vesikels te herzien met een korte targettag laten de onderzoekers zien hoe ze zich kunnen vasthechten aan specifieke aanhechtingsplaatsen op tumorcellen, wat de basis legt voor preciezere en minder toxische kankertherapieën.
Natuurlijke pakketjes veranderen in slimme koeriers
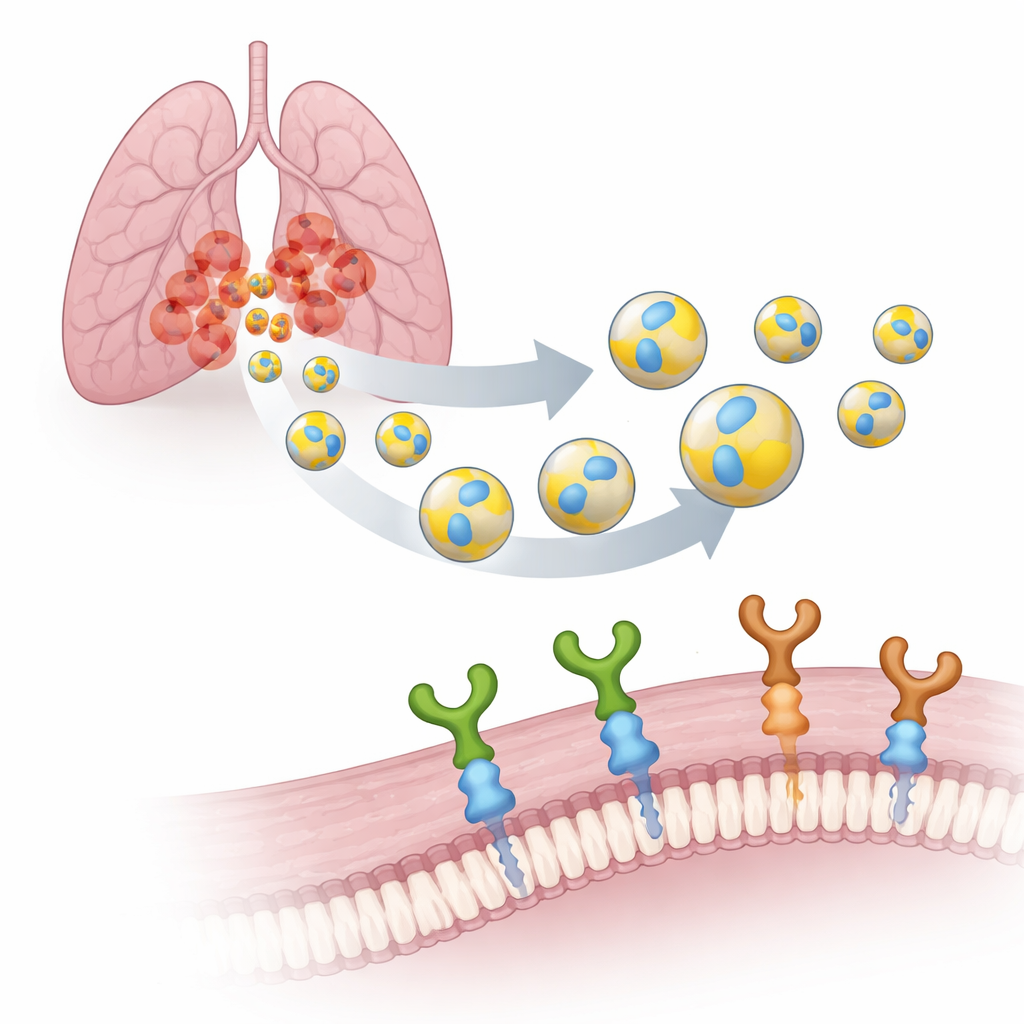
Elke cel in ons lichaam geeft EV’s af: nanoschaal belletjes omgeven door een membraan, een beetje zoals microscopische zeepbellen. Omdat ze door onze eigen cellen worden gemaakt, zijn EV’s biologisch afbreekbaar, passeren ze biologische barrières gemakkelijk en roepen ze minder snel bijwerkingen op dan synthetische dragers. Het team richtte zich op EV’s geproduceerd door menselijke longkankercellen (A549) en voorzag hun oppervlak van een kleine tag van zeven bouwstenen, PTHTRWA. Eerdere experimenten toonden aan dat deze tag EV’s doet aangroeien naar longkankercellen in muizen, veel sterker bindt aan tumorcellen dan aan normale longcellen en daarnaast slechts weinig toxisch is.
De juiste aanlegplaatsen op tumorcellen vinden
Om van deze getagde vesikels echt gerichte hulpmiddelen te maken, moesten de onderzoekers identificeren welke “poorten” op kankercellen ze herkennen. Ze onderzochten twee verwante receptoroppervlakken, α2β1- en α5β1-integrines. Dit zijn moleculaire grijphaken die cellen helpen zich aan hun omgeving te hechten en signalen naar binnen te sturen. In longtumoren wordt α5β1 sterk gekoppeld aan agressief gedrag, uitzaaiing en slechte overleving, terwijl α2β1 in verband is gebracht met chemoresistentie. Met een gevoelige techniek, surface plasmon resonance, vergeleek het team hoe sterk PTHTRWA-gedecoreerde EV’s aan beide integrines binden. Ze vonden dat vesikels zonder tag nauwelijks interactie vertoonden, terwijl getagde EV’s onder bijna fysiologische condities hechte, stabiele complexen met beide receptoren vormden.
Inzoomen op de moleculaire omhelzing
Om atomair te begrijpen wat er gebeurt wanneer de tag de integrines ontmoet, schakelden de onderzoekers computsimulaties in. Ze bouwden driedimensionale modellen van de tag gebonden aan sleutelregio’s van de integrines en lieten deze systemen honderden nanoseconden in virtueel water evolueren. De berekeningen toonden aan dat PTHTRWA nauw in een ondiepe groef op de α2β1-receptor past en een netwerk van waterstofbruggen en hydrofobe contacten vormt dat het complex stabiliseert. Cruciaal was dat de binding een meer “open” vorm van de receptor bevoordeelde — de hoge-affiniteit, signaalgereed vorm — boven de “gesloten” rusttoestand. Toen ze licht gewijzigde versies van de tag testten, zagen ze dat kleine chemische aanpassingen aan één uiteinde subtiel kunnen veranderen hoe het peptide in de groef ligt en hoe sterk het de voorkeur geeft aan de ene integrine boven de andere.
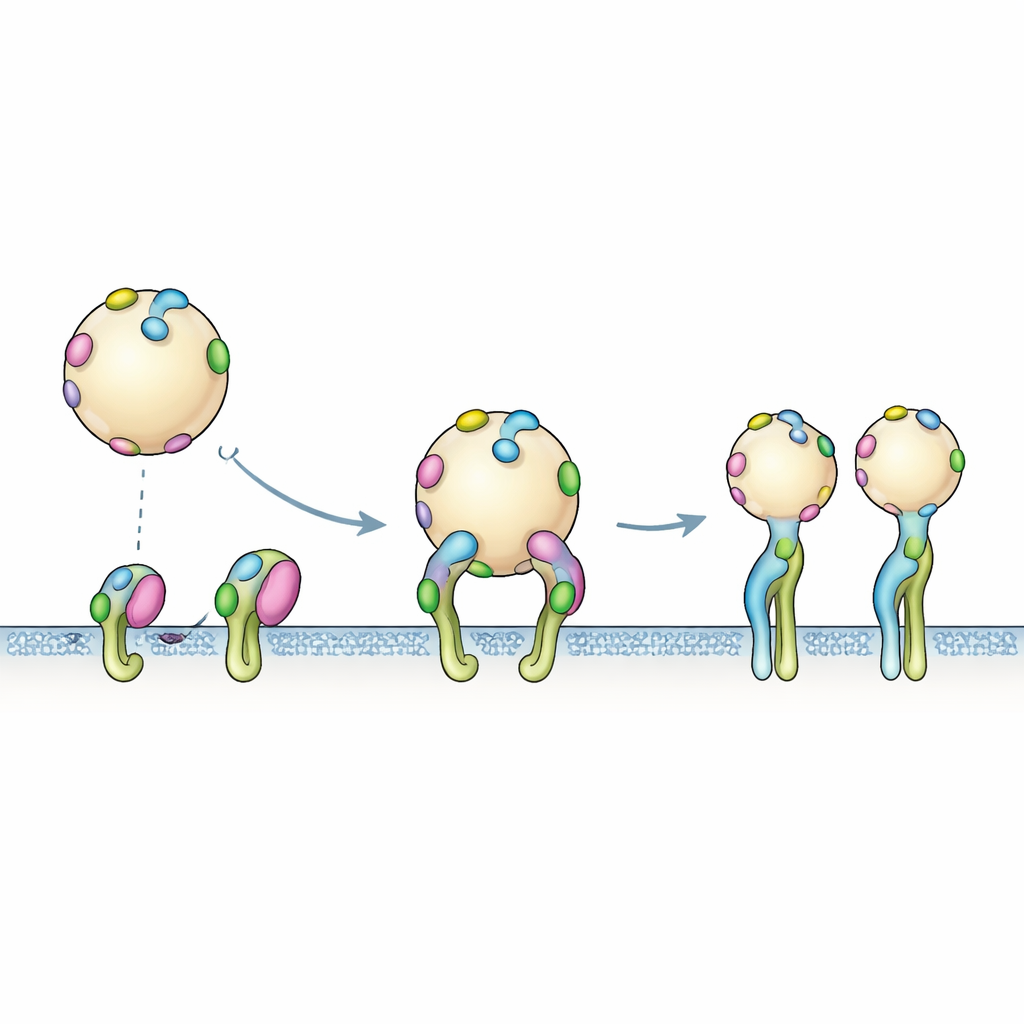
Van enkele tags naar multivalente grijpers
Computermodellen vangen telkens één tag die één receptor raakt, maar het echte EV-oppervlak zit vol met veel kopieën van PTHTRWA. De bindingsexperimenten weerspiegelen deze multivalente realiteit: zodra een getagde vesikel een gebied met integrines nadert, kunnen meerdere tags gelijktijdig binden. De sensorgegevens pasten het beste bij een twee-stappenproces. Eerst dockt de vesikel kort via snelle, reversibele ontmoetingen. Vervolgens treedt een trager herschikking op waarbij de integrines in hun open vorm verschuiven en de algehele greep verstevigt. Deze cooperatieve, veelhandige klem verklaart waarom de schijnbare bindingssterkte van hele vesikels groter is dan wat voorspeld zou worden op basis van één enkele tag.
Wat dit kan betekenen voor toekomstige behandelingen
Kort gezegd toont de studie aan dat EV’s bewapend met de PTHTRWA-tag selectief integrines kunnen herkennen die in longkanker overactief zijn, en dat ze dit doen door deze receptoren in een open, strak gebonden vorm te duwen. Door deze interacties in detail in kaart te brengen, leveren de onderzoekers ontwerprichtlijnen voor de volgende generatie vesikelgebaseerde dragers die geneesmiddelen, beeldvormingsagentia of andere ladingen direct aan kwaadaardige cellen kunnen afleveren terwijl gezond weefsel grotendeels genegeerd wordt. Hoewel meer werk in dieren en mensen nodig zal zijn, brengt deze integrinegerichte strategie de visie van gepersonaliseerde, EV-gebaseerde kankertherapie een stap dichterbij realiteit.
Bronvermelding: Nowicka, A.M., Żołek, T., Kowalczyk, A. et al. Structural and mechanistic insights into α2β1 and α5β1 integrin targeting by bioengineered extracellular vesicles originating from lung cancer cells. Sci Rep 16, 10833 (2026). https://doi.org/10.1038/s41598-026-46071-2
Trefwoorden: longkanker, extracellulaire vesikels, integrines, gerichte geneesmiddellevering, moleculaire simulaties