Clear Sky Science · nl
Vroege opsporing van metastatische risico’s bij primaire cutane melanoom met behulp van zwak-gestuurd leren
Waarom dit belangrijk is voor patiënten en artsen
Huidmelanoom kan dodelijk zijn, niet zozeer vanwege de plek op de huid zelf, maar omdat sommige tumoren zich stilletjes naar andere organen verspreiden. Tegenwoordig vertrouwen artsen vooral op hoe dik de tumor is en of het oppervlak is doorbroken om te schatten welke patiënten het grootste risico lopen. Deze studie onderzoekt of moderne kunstmatige intelligentie (AI) veel meer kan aflezen uit routinematige microscoopbeelden van de oorspronkelijke huidtumor en gevaarlijke kankers eerder kan signaleren, vooral bij patiënten die nog relatief kleine tumoren lijken te hebben.
Op zoek naar stille waarschuwingssignalen in weefselbeelden
De onderzoekers verzamelden digitale versies van standaard microscoopglaasjes van 426 primaire huidmelanomen, samen met basisgegevens zoals tumordikte, ulceratie, celdelingssnelheid en tumorgrootte. Ongeveer drie op de vijf van deze tumoren veroorzaakten later uitzaaiingen naar lymfeklieren of verre organen, terwijl de rest dat in elk geval niet deed gedurende minimaal drie jaar follow‑up. In plaats van pathologen specifieke gebieden met de hand te laten markeren, liet het team de computer elk deel van elk glaasje onderzoeken en sneed elke gigantische afbeelding in vele kleine steekproefvakken. De vraag was eenvoudig: kan een computer, getraind alleen op de uiteindelijke uitkomst of een patiënt uitzaaiingen ontwikkelde, leren visuele patronen te herkennen die hoog‑risico tumoren scheiden van laag‑risico tumoren?
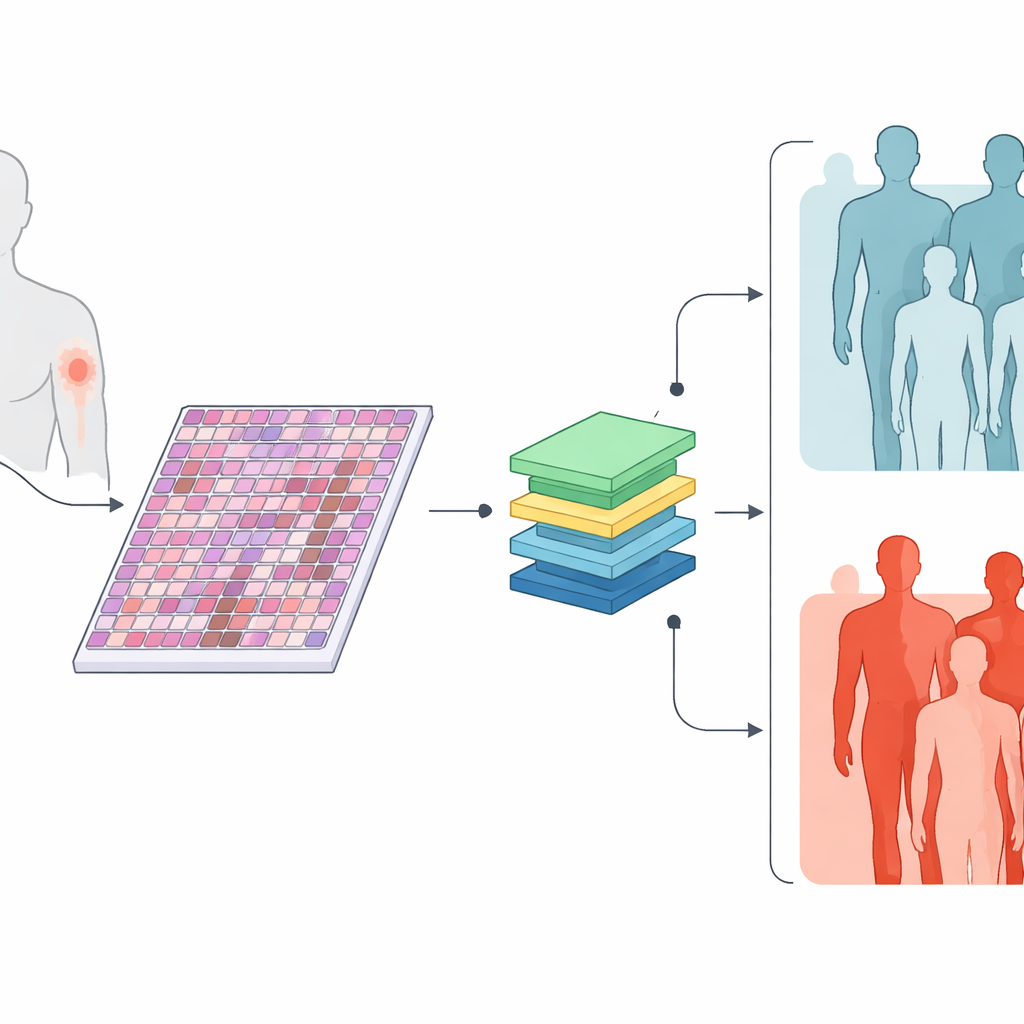
Machines leren weefsel lezen als een kaart
Het team gebruikte recente AI-methoden die eerst op enorme verzamelingen medische beelden en teksten waren voorgetraind en vervolgens waren aangepast aan melanoom. Eén model, TransMIL genoemd, keek alleen naar de weefselbeelden. Een ander, MultiTrans, combineerde de beeldinformatie met een compacte tekstbeschrijving van de klinische kenmerken van de tumor. Een derde, eenvoudiger model, BertMLP, gebruikte alleen die klinische kenmerken en negeerde de beelden. Bij tests op een aparte groep glaasjes die het model nog niet had gezien, scheidden beide op beelden gebaseerde modellen metastatische van niet‑metastatische tumoren correct in ongeveer 85% van de gevallen en toonden ze een hogere algehele nauwkeurigheid dan het model dat alleen klinische gegevens gebruikte. Dit suggereert dat de microscoopbeelden rijke aanwijzingen bevatten over toekomstig gedrag die door huidige routinematige metingen niet volledig worden vastgelegd.
Sterkere hulp waar beslissingen het moeilijkst zijn
Het voordeel van de op beelden gebaseerde AI was het duidelijkst bij tumoren van middelmatige dikte, een groep waarin artsen het meest worstelen met de beslissing wie agressieve behandeling nodig heeft. Bij deze T2‑melanomen presteerden de beeldmodellen duidelijk beter dan het alleen‑klinische model, dat geneigd was te veel tumoren als laag‑risico te classificeren. De op beelden gebaseerde systemen presteerden ook goed bij dikkere tumoren, maar die gevallen zijn op basis van standaardmaten al als gevaarlijk bekend. Bij meerdere patiënten die in eerste instantie als niet‑metastatisch werden geclassificeerd maar later uitzaaiingen ontwikkelden, gaven de AI‑modellen jaren eerder terecht aan dat de primaire tumoren een hoog risico vormden, wat aangeeft hoe dergelijke hulpmiddelen op termijn vroegere, meer gerichte therapie zouden kunnen ondersteunen.
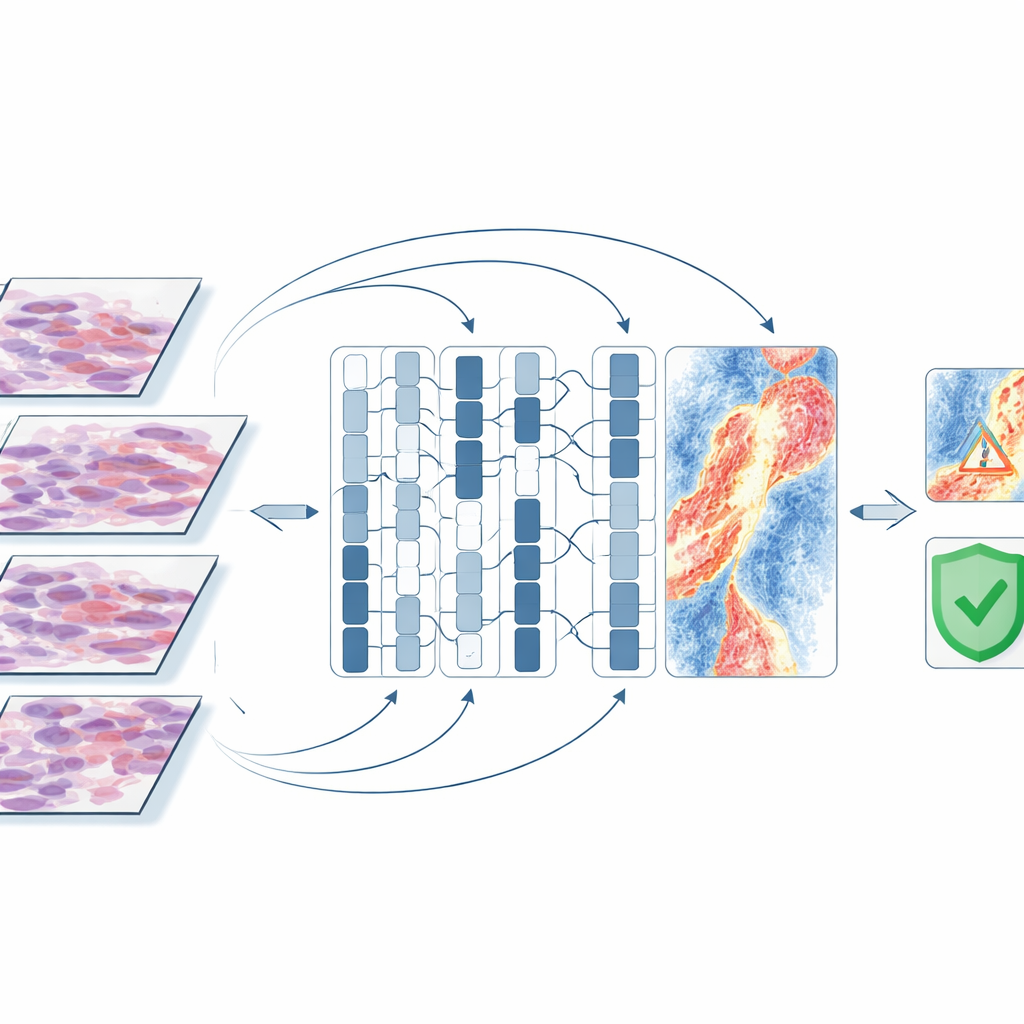
Waar de AI "naar kijkt" binnen de tumor
Om te begrijpen welke aanwijzingen de computer gebruikte, genereerden de onderzoekers attentiekaarten die de gebieden op een glaasje markeren die het meest invloedrijk waren voor een bepaalde voorspelling. In tumoren die uiteindelijk uitzaaiden, richtten de modellen zich vaak niet op dichte klonten tumorcellen, maar op de omgeving: bloedvaten, gebieden waar het huidoppervlak was afgebroken, en banden van ontstekingscellen die dieper in de huid lagen. In tumoren die niet uitzaaiden, waren de gemarkeerde gebieden vaak intacte oppervlaktelagen met weinig tekenen van schade. Verkeerd geclassificeerde gevallen bevatten vaak nietszeggend bindweefsel, vet of artefacten van de glaasjevoorbereiding, wat suggereert dat de computer moeite had wanneer duidelijke weefselsignalen zwak waren. Deze patronen sluiten aan bij het huidige begrip van hoe melanoomcellen in lymfevaten en de bloedbaan ontsnappen, wat biologische geloofwaardigheid geeft aan de keuzes van de AI.
Beperkingen, volgende stappen en wat dit zou kunnen betekenen
Dit werk werd uitgevoerd in één ziekenhuis op enkele honderden tumoren, en de modellen zijn nog niet getest in verschillende centra of gebruikt om overlevingstijd te voorspellen. De aanpak vervangt ook de patholoog niet; in plaats daarvan voegt ze een nieuwe laag risicoinformatie toe die automatisch uit routinematige glaasjes wordt gehaald. Desondanks tonen de bevindingen aan dat zwak‑gestuurde AI zinvolle waarschuwingssignalen van uitzaaiing rechtstreeks uit primair melanoomweefsel kan onthullen, zonder arbeidsintensieve handmatige markeringen. Als dit gevalideerd wordt in grotere, multicenterstudies en gecombineerd met andere gegevens zoals huidfoto’s en genactiviteitstests, zouden dergelijke hulpmiddelen artsen kunnen helpen beter patiënten te identificeren met ogenschijnlijk vroeg‑stadium melanoom die stilletjes een hoog risico op metastase dragen, zodat zij intensiever gecontroleerd kunnen worden of eerder preventieve behandeling kunnen krijgen.
Bronvermelding: Dahlén, F., Shujski, I., Yacob, F. et al. Early detection of metastatic risk in primary cutaneous melanoma using weakly supervised learning. Sci Rep 16, 11234 (2026). https://doi.org/10.1038/s41598-026-45588-w
Trefwoorden: melanoom, metastatisch risico, digitale pathologie, kunstmatige intelligentie, zwak-gestuurd leren