Clear Sky Science · nl
Proof of concept voor extractie van cell-free DNA uit plasma met behulp van een tweefasig aquatisch systeem voor toepassingen in vloeibare biopsie
Waarom een bloedtest van belang is voor kanker en andere aandoeningen
Veel moderne medische tests zoeken naar kleine DNA-fragmenten die vrij in ons bloed zweven. Deze deeltjes, bekend als cell-free DNA, kunnen onthullen of een tumor genetisch materiaal verliest, of een getransplanteerd orgaan afgestoten wordt, of hoe een zwangerschap vordert. Omdat deze DNA-fragmenten echter schaars, kort en vermengd met een soep van eiwitten en andere moleculen zijn, is het verrassend moeilijk om ze schoon en snel te isoleren. Deze studie introduceert een nieuwe, eenvoudiger manier om deze fragmenten uit bloedplasma te halen met een zachte watergebaseerde scheidingsmethode, wat geavanceerde “vloeibare biopsie”-testen mogelijk toegankelijker en betaalbaarder kan maken.
De uitdaging van het vangen van kleine DNA-stukjes
Artsen en onderzoekers gebruiken vloeibare biopsies om genetische aanwijzingen te lezen uit een eenvoudige bloedafname in plaats van weefsel te snijden. Het probleem is dat cell-free DNA in plasma meestal slechts enkele tientallen nanogram per milliliter voorkomt en in korte fragmenten is versneden. Een klein deel van dit materiaal kan afkomstig zijn van een tumor of van een getransplanteerd orgaan, dus elk fragment telt. Standaard extractiekits vangen DNA door het te laten hechten aan silica-oppervlakken in aanwezigheid van sterke zouten, gevolgd door meerdere was- en centrifugatiestappen. Deze kits werken goed maar vergen tijd, speciaal apparatuur en kunnen duur zijn. Ze hebben ook moeite om de kortste fragmenten terug te winnen en kunnen ongewenste lange stukken normaal genoom-DNA meenemen, die zeldzame ziektesignalen kunnen maskeren.
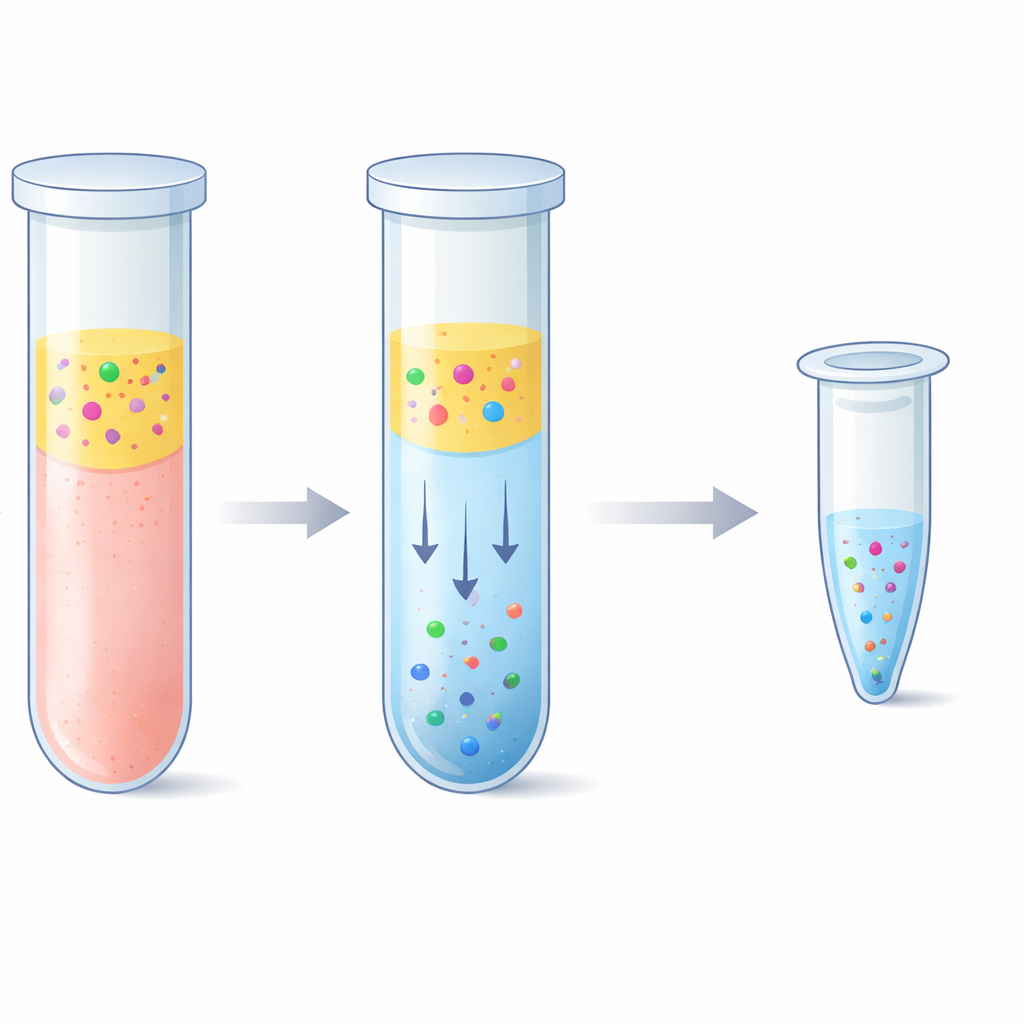
Een tweelaagse watertruc om DNA te vangen
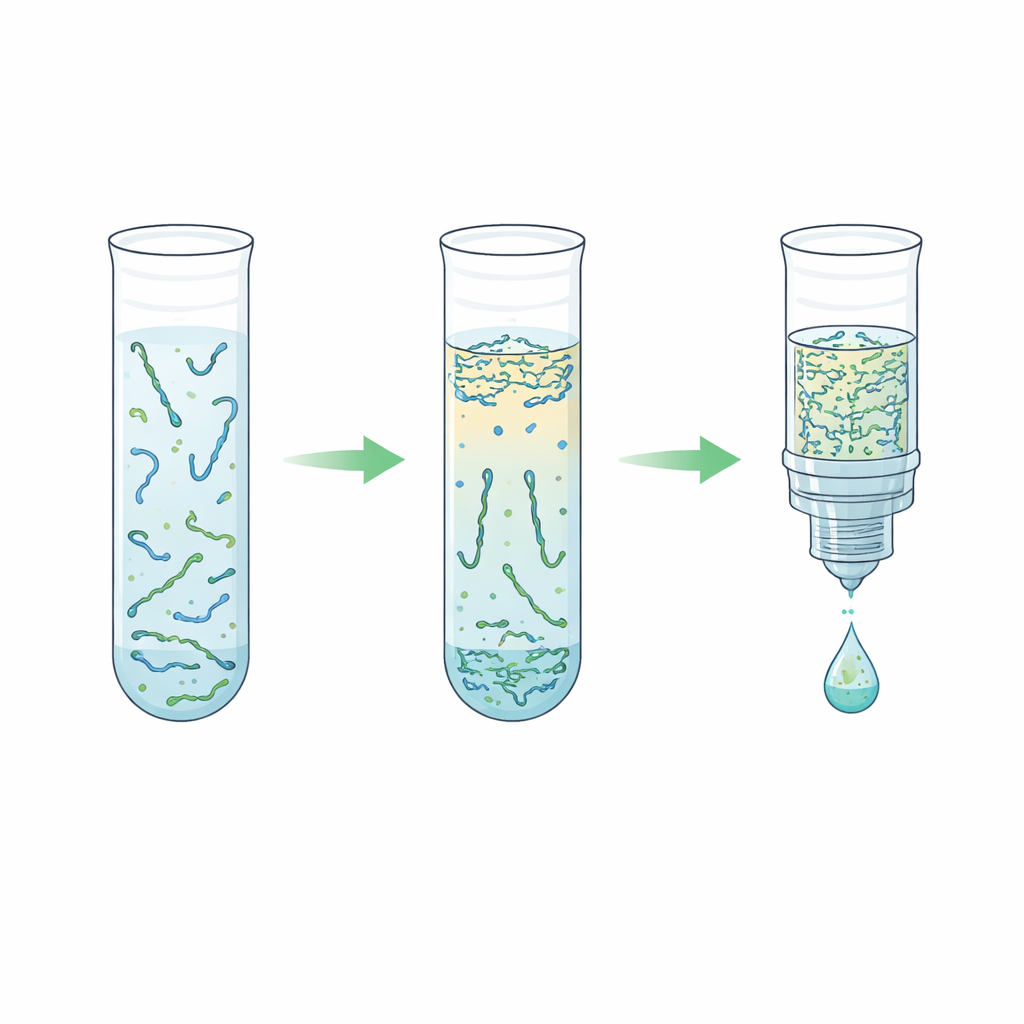
Het team onderzocht een alternatief gebaseerd op een “aqueous two-phase system” — in gewone taal: twee waterrijke vloeistoffen die niet volledig mengen, vergelijkbaar met olie en azijn maar beide grotendeels uit water bestaande. Door plasma te combineren met een polymeer genaamd polyethyleenglycol en eenvoudige fosfaatzouten, splitste het mengsel zich vanzelf in een boven- en onderlaag. Opmerkelijk genoeg gaven de korte DNA-fragmenten sterk de voorkeur aan de zoutrijke onderlaag, terwijl de meeste bloedeiwitten en lange DNA-strengen in de bovenlaag of bij het grensvlak bleven. De onderzoekers stemden het recept zorgvuldig af zodat de onderlaag klein genoeg bleef om het DNA te concentreren maar zacht genoeg om het niet te beschadigen. Ze koppelden deze stap vervolgens aan een “reverse elution”-zuivering, waarbij de zoute onderlaag door een poreus matrix wordt geduwd om zout te verwijderen en het eindvolume te verkleinen, resulterend in een schonere en geconcentreerdere DNA-oplossing.
Het proces verfijnen voor gebruik in de praktijk
Door vele rondes van testen pasten de auteurs de balans van polymeer en zout, centrifugesnelheden, volumes en optionele lysis-stappen aan die eiwit–DNA-complexen afbreken. Ze vonden dat het verhogen van het polymeergehalte langs bepaalde samenstellingslijnen de DNA-concentratie verdubbelde zonder de opbrengst te schaden, en dat sterkere conditionering in de reverse elution-stap de concentratie ruwweg verviervoudigde vergeleken met hun eerdere werk. Verrasend genoeg ontdekten ze dat het overslaan van agressieve lysis vóór de tweelaagse scheiding vaak het beste werkte; lysis verstoorde de fasen en verminderde de opbrengst. Een gestroomlijnde, grotendeels lysisvrije workflow verwijderde ongeveer 99,7% van de plasma-eiwitten terwijl tot ongeveer tweederde van het korte DNA-input werd teruggewonnen in een viermaal kleiner volume, alles binnen ongeveer tien minuten totale verwerkingstijd en slechts een paar minuten handwerk.
Hoe de nieuwe methode zich verhoudt
De onderzoekers vergeleken hun aanpak met een veelgebruikte commerciële silica-kit. De standaardkit gaf iets hogere totale DNA-opbrengsten en sterkere concentratie omdat deze elueren in zeer kleine volumes. De tweefasige methode toonde echter consistente terugwinningen van boven de 60% over een reeks DNA-inputs, zelfs bij zeer kleine hoeveelheden, en vereiste veel minder handmatige stappen en minder apparatuur. Belangrijk is dat het nieuwe proces fungeerde als een ingebouwd filter voor fragmentlengte: het verrijkte korte, cell-free-achtige DNA-fragmenten terwijl het grotendeels lange strengen uitsloot die kunnen voortkomen uit gebroken bloedcellen. Tests met kwantitatieve PCR toonden aan dat de gereinigde extracten de daaropvolgende amplificatie niet remden. Toen het team een commercieel referentiemonster met bekende kankergerelateerde mutaties gebruikte, kon het met hun methode teruggewonnen DNA worden omgezet in sequencelibraries, op een hogedoorvoersequencer worden gelezen, en gebruikt worden om alle verwachte varianten in de juiste frequenties te detecteren.
Wat dit kan betekenen voor toekomstige bloedtesten
Kort gezegd laat dit werk zien dat een relatief eenvoudige, watergebaseerde scheiding meer complexe vaste-oppervlakte-chemie kan vervangen voor het voorbereiden van cell-free DNA uit plasma. Hoewel de nieuwe methode momenteel iets minder DNA oplevert dan de beste commerciële kits, biedt zij snelle verwerking, sterke verwijdering van ongewenste eiwitten en lang DNA, en klaarheid voor gebruik met PCR en next-generation sequencing. Als verdere validatie op echte patiëntmonsters plaatsvindt en de methode geschikt wordt gemaakt voor automatisering, kan deze aanpak kosten verlagen en laboratoriumworkflows vereenvoudigen, waardoor precieze, genetica-gebaseerde bloedtests voor kanker, transplantatie en andere aandoeningen wijdverbreider in het dagelijks gebruik kunnen komen.
Bronvermelding: Meutelet, R., Buerfent, B.C., Hess, T. et al. Proof of concept for aqueous two-phase system-based extraction of cell-free DNA from plasma for liquid biopsy applications. Sci Rep 16, 11232 (2026). https://doi.org/10.1038/s41598-026-45585-z
Trefwoorden: vloeibare biopsie, cell-free DNA, kankerbloedtest, DNA-extractie, next-generation sequencing