Clear Sky Science · nl
Kristallografische gegevens voor Pyrococcus furiosus dolichylfosfaat mannosesynthase suggereren dat het enzym zijn glycolipideproduct zou kunnen omklappen
Hoe hitte-minnende microben hun celomhulsel in vorm houden
Veel microben die floreren in kokend hete omgevingen overleven dankzij een beschermend suikeromhulsel op hun celoppervlak. Het bouwen van dit omhulsel vereist speciale vet–suikermoleculen die aan één kant van het celmembraan moeten worden gemaakt en vervolgens naar de andere kant verplaatst. Deze studie ontleedt een zulk molecuul producerend enzym uit een hitte-minnende microbe en suggereert dat, opmerkelijk genoeg, hetzelfde eiwit mogelijk ook helpt om zijn product over het membraan te klappen—twee taken tegelijk vervullend.
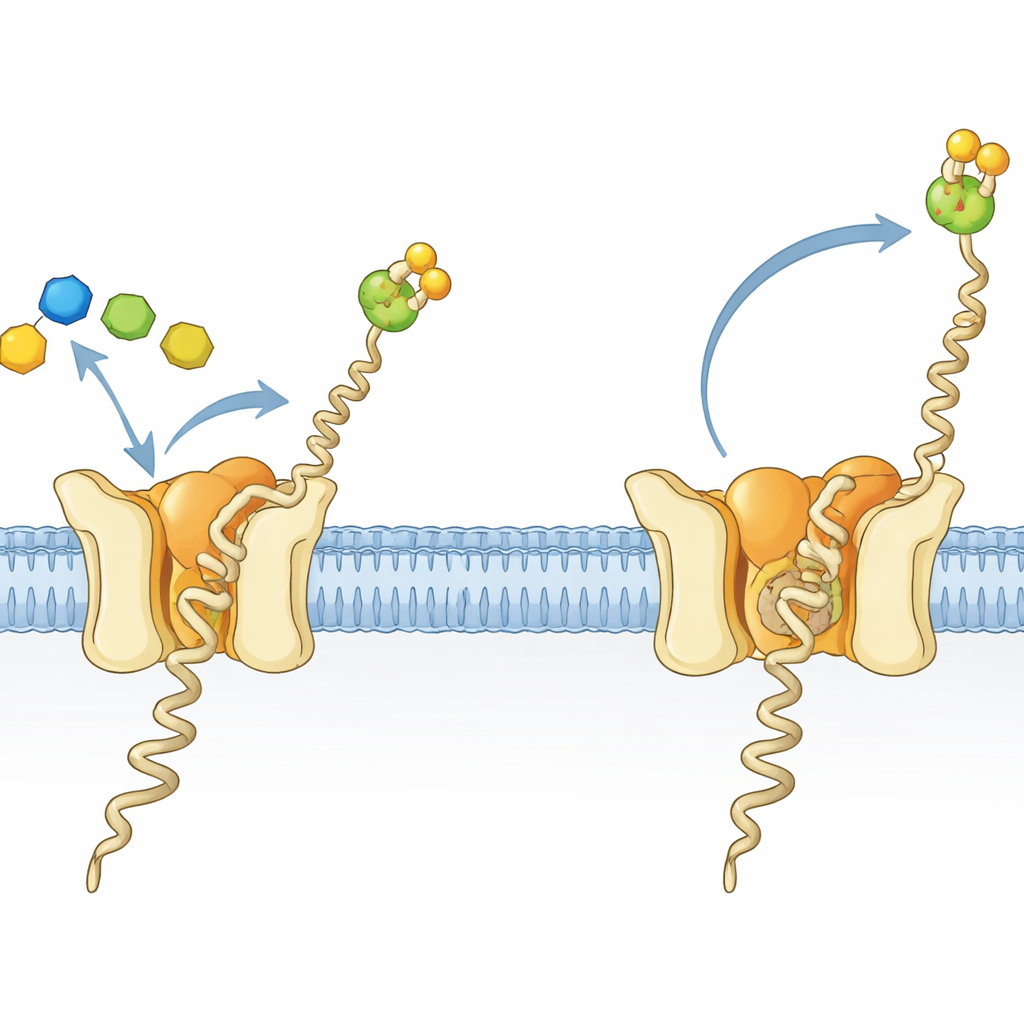
Een piepkleine fabriek voor een cruciaal suiker–vetmolecuul
Cellen in alle levensdomeinen versieren veel eiwitten met suikerketens, een proces essentieel voor juiste vouwing, stabiliteit en cel–celcommunicatie. Bij archaea en eukaryoten is een belangrijk bouwsteen voor deze versieringen een suiker–vetmolecuul genaamd dolichylfosfaat mannose (Dol-P-Man). Het bestaat uit een lange vette staart die in het membraan verankerd zit en een suiker–fosfaatkop die uitsteekt in de waterige omgeving. Dol-P-Man wordt gemaakt door het enzym dolichylfosfaat mannosesynthase (DPMS), dat een mannose overzet van een oplosbare donor op een membraangebonden lipide. Bij de hyperthermofiele archaeon Pyrococcus furiosus is DPMS een keten-eiwit, aangeduid als type-III DPMS, met een oplosbare katalytische regio gekoppeld aan een vier-helix membraan-doorstekend deel waarvan de rol onduidelijk was.
Het enzym in actie vastleggen
De onderzoekers kristalliseerden P. furiosus DPMS samen met zijn substraten en volgden de reactie met röntgendiffractie. Hun nieuwe structuur, gecombineerd met drie eerdere, legt een reeks momentopnames vast rond het moment waarop de suiker wordt overgedragen. In één toestand zijn het donormolecuul (GDP-mannose) en een Dol-P–achtig acceptor gebonden in een precieze geometrie die het reactieve koolstofatoom van mannose direct vóór de fosfaatgroep op Dol-P plaatst—een ideale “pre-transfer” configuratie. Lussen op het enzym werken als voor- en achterdeuren: ze sluiten om donor en metaalion op hun plek te houden en herschikken vervolgens om een pad te openen voor Dol-P om binnen te komen en voor het gebruikte GDP om te vertrekken zodra de suiker is overgedragen. Deze details verduidelijken hoe het enzym efficiënte en nauwkeurige suikeroverdracht aan het membraanoppervlak waarborgt.
Een ondersteboven product verborgen in het membraan
Nog verrassender was een tweede, onderscheidende toestand gezien in dezelfde kristallen. Hier bevindt het voltooide Dol-P-Man molecuul zich niet in het actieve centrum maar dieper ingebed in het membraan-doorstekende gedeelte van het eiwit, in een “ondersteboven” oriëntatie. De suiker–fosfaatkop zit in een polair zakje tussen twee paar helices (TMD1 en TMD2), terwijl de vette staart langs een groef loopt die door de helices wordt gevormd. Een sleutelaminozuur, een fenylalanine, lijkt te fungeren als poort die de toegang tot dit zakje kan blokkeren of openen. De kwaliteit van de elektrondichtheid en de manier waarop het eiwit in het kristal verpakt zit spreken ervoor dat dit omgeklapte Dol-P-Man geen artefact van kristalcontacten is, maar een echte, goed bevolkte toestand die het enzym kan aannemen.
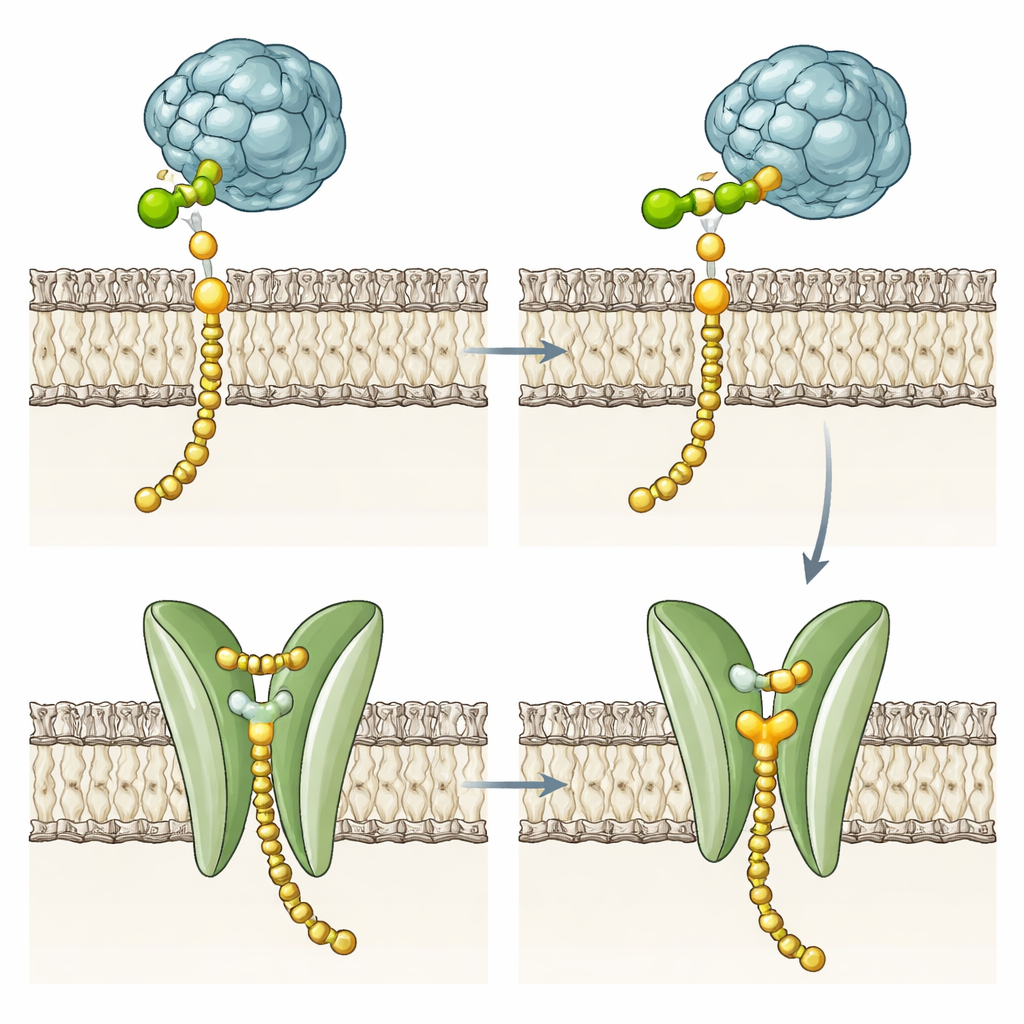
Mutante enzymen wijzen op een tweede taak
Om te testen of het membraan-doorstekende domein nodig is voor de suikeroverdrachtchemie, creëerde het team meerdere varianten. Ze verwijderden het grootste deel of alle helices, vervingen ze door een ander membraansegment uit gist-DPMS, of wijzigden sleutelresiduen in het zakje en de fenylalanine-poort. Opmerkelijk genoeg maakten deze mutantenzymen nog steeds Dol-P-Man aan met vergelijkbare snelheden als het intacte enzym, hoewel sommige iets minder stabiel waren in het membraan. Dit toont aan dat de kernchemie in de oplosbare katalytische regio huist en dat het vier-helixbundel niet nodig is om mannose aan Dol-P te hechten. In plaats daarvan suggereren het geconserveerde polaire zakje, de groef en het poortresidu een gespecialiseerde rol bij het afhandelen van het voltooide product, vooral bij hyperthermofiele archaea waarvan de stijve membranen spontane lipide-omklapping energetisch kostbaar maken.
Waarom een tweefunctie-enzym ertoe doet
Door het structurele en mutatiebewijs samen te brengen, stellen de auteurs voor dat type-III DPMS een “moonlighting” eiwit is. Eerst synthetiseert het Dol-P-Man aan de binnenzijde van het archaalse plasmamembraan; vervolgens kan het transmembranaire domein helpen het suiker–vetmolecuul om te klappen zodat de kopgroep aan de buitenkant van de cel verschijnt, klaar om te worden gebruikt door andere enzymen die het suikermantel van de cel opbouwen. Evolutie lijkt dit chimere ontwerp vooral te hebben bevoordeeld in extreem hitte-minnende archaea, waar het dicht bij elkaar brengen van de syntheseplaats en een gewijd omklapgroef afval en thermische schade kan minimaliseren. Hoewel dit werk omklapactiviteit nog niet direct bewijst, biedt het een concreet structureel model voor hoe een enzym zowel een essentieel lipide-intermediair kan creëren als herpositioneren over een vijandige membraanbarrière.
Bronvermelding: Gandini, R., Keskitalo, M.M., Reichenbach, T. et al. Crystallographic data for Pyrococcus furiosus dolichylphosphate mannose synthase suggest that the enzyme could flip its glycolipid product. Sci Rep 16, 9076 (2026). https://doi.org/10.1038/s41598-026-44343-5
Trefwoorden: dolichylfosfaat mannose, lipide-flippase, archaea, proteïneglycosylering, membraanenzymen