Clear Sky Science · nl
Modeleren van Clostridioides difficile-toxinepathogenese en antiserumbescherming in een immuuncompetent intestine-on-chip platform
Waarom dit darminfectiemodel belangrijk is
Antibiotica redden levens, maar kunnen ook de darm kwetsbaar maken voor gevaarlijke infecties. Een van de ergste veroorzakers is Clostridioides difficile, een bacterie die ernstige diarree en levensbedreigende ontsteking van de dikke darm kan veroorzaken, vooral bij opgenomen patiënten. Deze studie introduceert een miniatuur “darm op een chip” dat belangrijke kenmerken van de menselijke darm nabootst, inclusief bloedvaten en immuuncellen, om in real time te observeren hoe de toxines van C. difficile de darm beschadigen en hoe antilichaambehandelingen die schade mogelijk kunnen stoppen.
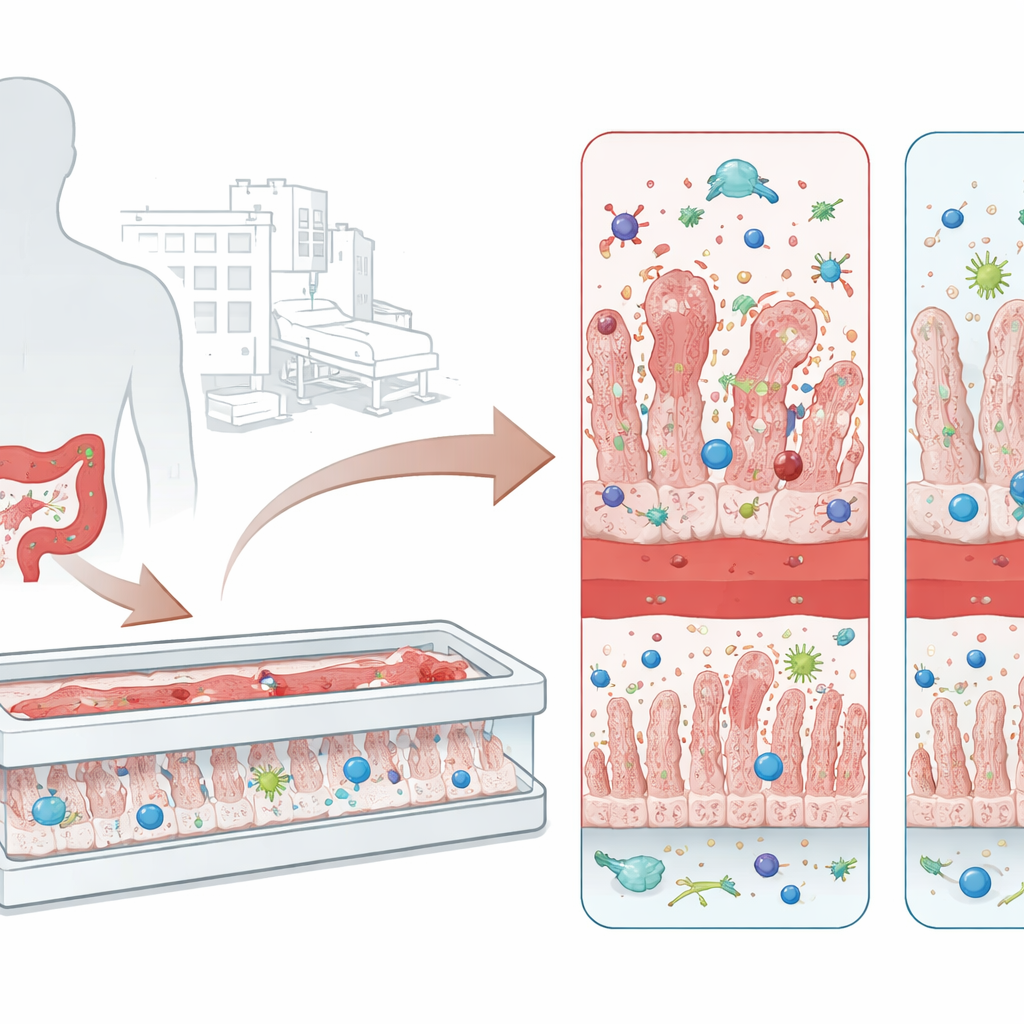
Van hardnekkige ziekenhuisbacterie tot darmschade
C. difficile gedijt bij mensen wiens normale darmmicrobioom verstoord is, vaak na een kuur met breedspectrumantibiotica. De microbe overleeft onder zware omstandigheden als taaie sporen en, eenmaal gevestigd in de dikke darm, scheidt twee belangrijke toxines af die bekendstaan als TcdA en TcdB. Deze toxines vallen darmcellen aan, versoepelen de verbindingen tussen cellen en veroorzaken golven van ontsteking. Het resultaat kan variëren van hardnekkige diarree tot pseudomembraneuze colitis, een aandoening waarbij lagen dood weefsel en immuuncellen de darmwand bedekken. Huidige behandelingen vertrouwen vooral op meer antibiotica en soms darminhoudtransplantaties, maar veel patiënten krijgen herhaalde infecties, wat het belang onderstreept van betere manieren om de ziekte te bestuderen en toxineblokkerende therapieën te testen.
Een klein levend darmweefsel op een chip bouwen
Traditionele laboratoriummodellen laten een platte laag darmcellen groeien in een schaaltje. Hoewel nuttig, ontbreken deze tweedimensionale kweeksystemen bloedvaten, immuuncellen en de zachte stroming van vloeistof die een echte darm vormgeeft. De onderzoekers gebruikten in plaats daarvan een microge-engineerde “intestine-on-chip”-apparaat met twee parallelle kanalen gescheiden door een poreus membraan. De ene zijde is bekleed met darmcellen die uitgroeien tot vingervormige richels die lijken op villi en een strakke barrière vormen. De tegenoverliggende zijde bevat menselijke bloedvatcellen. In dit miniatuurweefsel voegde het team monocyten-afgeleide macrofagen toe die zich in de darmwand vestigen en circulerende neutrofielen die via het vatkanaal kunnen reizen en in het weefsel infiltreren, waardoor een immuuncompetente intestine-on-chip (i‑IoC) ontstaat die de levende darm realistischer nabootst.
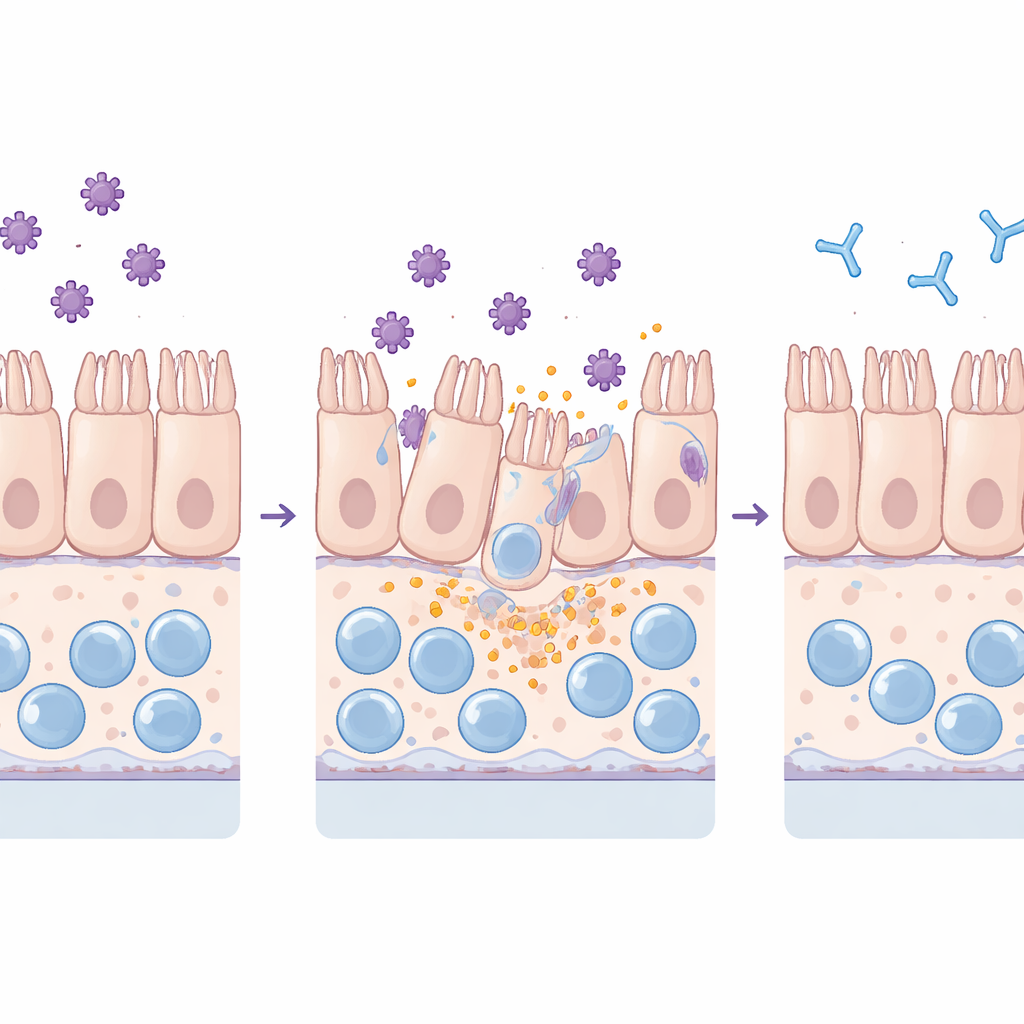
Observeren hoe toxines de barrière beschadigen
Het team bracht zowel standaard platte kweeklagen als het complexere chipmodel in contact met gezuiverde TcdA en TcdB. Ze volgden hoe goed de darmbarrière fluorescerende kleurstof buiten hield, onderzochten junction-eiwitten die aangrenzende cellen bij elkaar houden en maten ontstekingsmoleculen en markeerders van cellulaire schade in de omliggende vloeistof. Beide toxines schaadden het weefsel, maar op verschillende manieren: TcdA verstoorde vooral de tight junctions en zorgde ervoor dat cellen rond werden, terwijl TcdB leidde tot wijdverbreid verlies van cellen uit de laag. Cruciaal was dat de chip deze effecten detecteerde bij veel lagere toxineniveaus dan de platte kweeklagen, wat wijst op een grotere gevoeligheid en een levensechter gedrag onder continue stroming.
Immuuncellen blussen de vlammen niet — maar kunnen beschermd worden
Het toevoegen van macrofagen en neutrofielen aan de chip versterkte de reactie op toxines. Macrofagen verhoogden de afgifte van belangrijke ontstekingssignalen zoals IL‑6 en IL‑8 maar raakten zelf uitgeput, overeenkomstig een inflammatoire vorm van celdood. Neutrofielen hechtten zich aan de vaatwand en migreerden het darmweefsel in, overeenkomend met de toestroom van immuuncellen die bij patiënten wordt gezien. Langere blootstelling aan toxines beschadigde niet alleen het darmslijmvlies maar uiteindelijk ook de vaatlaag. Toen de onderzoekers de toxines echter vooraf mengden met toxine-neutraliserende antistoffensera, werden structurele schade, barrièrelekkage, cytokinepieken, verlies van macrofagen en neutrofiele infiltratie allemaal sterk verminderd. In langere experimenten konden weefsels die door TcdB waren beschadigd deels herstellen zodra de toxines werden verwijderd, terwijl TcdA meer aanhoudende schade achterliet, wat wijst op verschillende herstelcapaciteiten na elk toxine.
Wat dit betekent voor patiënten en therapieën
Voor de lekenlezers is de belangrijkste boodschap dat dit kleine, levende darmmodel realistisch kan nabootsen hoe de toxines van C. difficile de darm beschadigen en het immuunsysteem activeren, en tegelijkertijd laat zien hoe goed antitoxine-antilichamen het weefsel kunnen beschermen. Vergeleken met eenvoudige cellagen is de intestine-on-chip gevoeliger, bevat het bloedvaten en immuuncellen en kan het dagenlang functioneren om zowel vroege schade als herstelpogingen vast te leggen. Dat maakt het een veelbelovend testplatform voor volgende-generatie behandelingen en vaccins die toxines neutraliseren zonder de darmmicrobiota verder te verstoren, en mogelijk een hulpmiddel om therapieën op maat te maken met patiënt-afgeleide cellen in de toekomst.
Bronvermelding: Wegner, V.D., Warschinke, M., Brahim, I.B. et al. Modeling Clostridioides difficile toxin pathogenesis and antiserum protection in an immunocompetent intestine-on-chip platform. Sci Rep 16, 9233 (2026). https://doi.org/10.1038/s41598-026-44170-8
Trefwoorden: Clostridioides difficile, intestine-on-chip, darmaandoening, neutraliserende antilichamen, organ-on-chip modellen