Clear Sky Science · nl
Label-vrije multiphotonmicroscopie en machine learning voor herkenning van hepatocellulair carcinoom
Waarom dit belangrijk is voor mensen met leverkanker
Leverkanker, in het bijzonder hepatocellulair carcinoom, komt vaak voor en is dodelijk; chirurgie is vaak de enige kans op genezing. Tijdens een operatie moeten chirurgen de gehele tumor verwijderen terwijl ze zo veel mogelijk gezond leverweefsel sparen — een lastige afweging wanneer het zieke leverweefsel er al afwijkend uitziet. Deze studie verkent een nieuwe manier om kanker tijdens de operatie in realtime te "zien", zonder kleurstoffen of langdurig laboratoriumwerk, door geavanceerde lasermicroscopie te combineren met kunstmatige intelligentie. Het doel is chirurgen te helpen de werkelijke rand van de tumor sneller en nauwkeuriger te vinden, wat mogelijk de uitkomst voor patiënten verbetert.
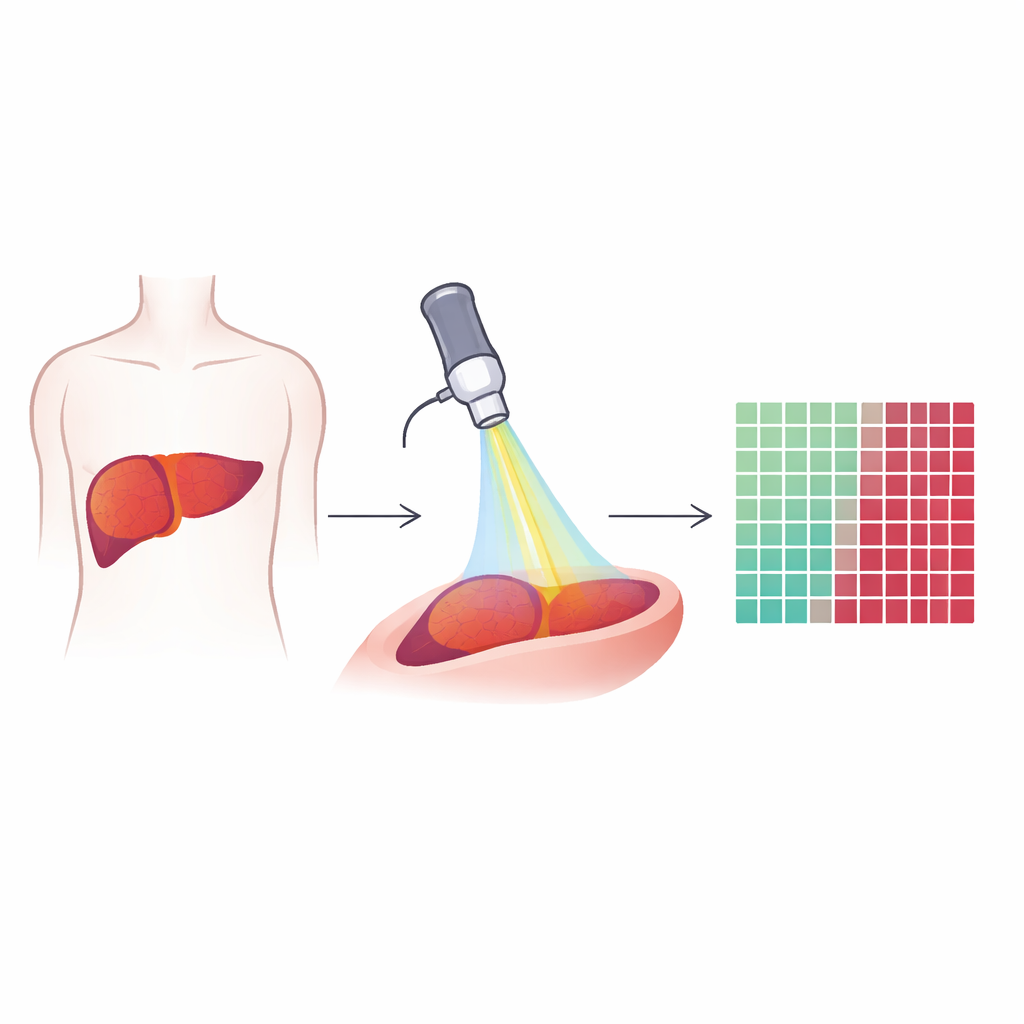
In het weefsel kijken met speciaal licht
De onderzoekers gebruikten een techniek genaamd multiphotonmicroscopie, die vertrouwt op zeer korte laserpulsen om natuurlijke moleculen in weefsel te laten oplichten of signalen te laten genereren. In plaats van kleurstoffen of contrastmiddelen toe te voegen, leest de methode wat er al aanwezig is: vetten, collageenvezels en van nature fluorescerende stoffen in cellen. Er werden drie typen signalen vastgelegd in elk klein gezichtsveld van levermonsters: één die lipiden benadrukt, één die autofluorescentie van moleculen zoals NADH en vitamine A toont, en één die stijve collageenvezels zichtbaar maakt. Samen creëren deze signalen kleurrijke, hoogresolutiebeelden die zowel individuele cellen als de algemene architectuur van leverweefsel en tumoren laten zien.
De vele gezichten van leverkanker vastleggen
Het team onderzocht weefsel van 76 patiënten die een operatie voor leverkanker ondergingen, waarbij zowel de tumor als de omringende lever werden bekeken. Ze toonden aan dat deze label-vrije beeldvorming klassieke groeipatronen van hepatocellulair carcinoom kan weergeven, zoals dunne of dikke platen tumorcellen, solide bladen en klierachtige structuren. Het toont ook veranderingen in de omliggende lever, waaronder vetophoping en littekenvorming, die veel voorkomen bij patiënten met chronische leverziekte. Belangrijk is dat deze patronen zichtbaar waren zelfs wanneer de beelden met relatief lage resolutie werden verkregen, vergelijkbaar met wat toekomstige endoscopische apparaten in het lichaam zouden kunnen leveren. Dit suggereert dat de aanpak praktisch toepasbaar kan zijn in de operatiekamer, niet alleen in een laboratorium.
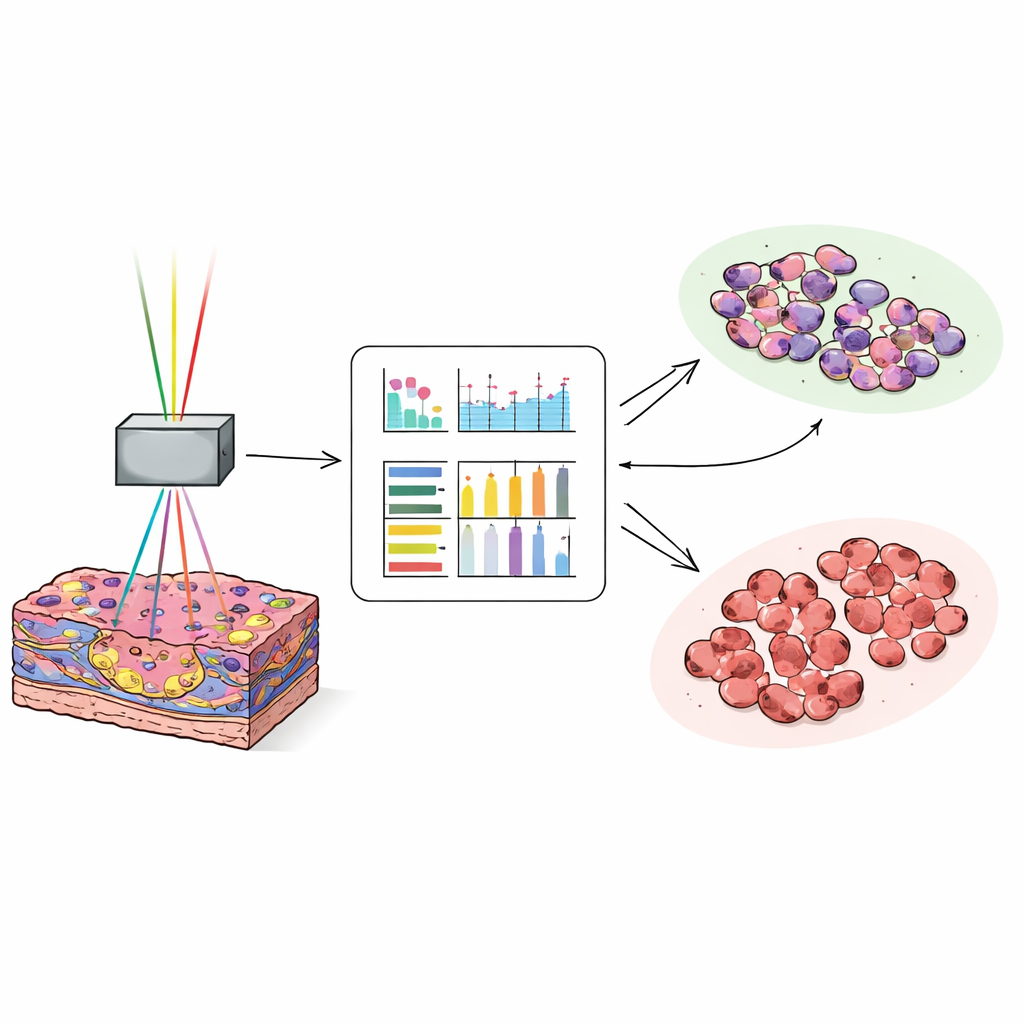
Een computer leren de tumorrand te herkennen
Om rijke maar complexe afbeeldingen om te zetten in snelle beslissingen veranderden de wetenschappers elk beeld in getallen die de textuur beschrijven, zoals hoe glad, grof of gevarieerd de pixellpatronen zijn. Voor elk beeldkanaal berekenden ze 17 van dergelijke metingen en trainden vervolgens een neuraal netwerk op ongeveer 25.000 afbeeldingen van 35 patiënten om tumorweefsel te onderscheiden van niet-kankerachtig leverweefsel. Ze testten het model daarna op ongeveer 27.000 nieuwe afbeeldingen van nog eens 38 patiënten. Wanneer de computer een combinatie van het autofluorescentie- en het collageen-gevoelige signaal gebruikte, labelde hij afbeeldingen correct als tumor of normaal in ongeveer 97 van de 100 gevallen. Zelfs de meest subtiele, goed gedifferentieerde tumoren, die moeilijk te herkennen zijn voor pathologen op snelle bevroren secties, werden met hoge nauwkeurigheid geclassificeerd.
Wat de lichtpatronen over kanker onthullen
Door verschillende signaalkombinaties te vergelijken, vond de studie dat autofluorescentie de meest bruikbare informatie droeg om kanker van niet-kanker te onderscheiden. Deze gloed ontstaat uit vele natuurlijke moleculen in cellen en uit structuren zoals elastine en collageen, en draagt dus informatie over celdichtheid, de grootte en vorm van kernen (zichtbaar als donkere gebieden), vetdruppels en de samenstelling van het omliggende weefsel. Het toevoegen van het collageenspecifieke signaal verscherpte verder het contrast tussen tumor en achtergrondlever, wat overeenkomt met bekende verschillen in de ordening van vezels en bloedvaten. Verrassend genoeg droeg het op lipiden gerichte signaal minder bij aan automatische classificatie — een praktische bedenking omdat dit eenvoudigere apparaatsontwerpen mogelijk maakt die op één laserstraal vertrouwen in plaats van complexere systemen met twee stralen.
Van laboratoriumbank naar operatiekamer
Om echt chirurgengebruik te simuleren, paste het team hun beste model ook toe op weefselmonsters die de werkelijke grens tussen tumor en lever omvatten, en creëerde kanskaarten die aangaven waar kanker eindigde en normaal weefsel begon. Deze kaarten kwamen over het algemeen goed overeen met conventionele histologie, hoewel sterk vette of collageenrijke gebieden de classifier soms in de war brachten. De auteurs merken op dat er nog hindernissen zijn voordat deze technologie live chirurgie kan begeleiden, waaronder de beperkte diepte van optische beeldvorming, de behoefte aan robuuste, steriele endoscopen, beweging en bloed in het operatieveld, en de uitdaging om kunstmatige intelligentie te valideren op grote, real-world datasets. Toch laat het werk zien dat label-vrije multiphotonbeeldvorming, gecombineerd met machine learning, kan fungeren als een snelle, digitale microscoop die op een dag chirurgen kan helpen preciezer en veiliger te snijden, waardoor de kans toeneemt dat alle kanker wordt verwijderd terwijl zo veel mogelijk gezond leverweefsel behouden blijft.
Bronvermelding: Galli, R., Korn, S., Aust, D. et al. Label-free multiphoton microscopy and machine learning for recognition of hepatocellular carcinoma. Sci Rep 16, 8734 (2026). https://doi.org/10.1038/s41598-026-43831-y
Trefwoorden: beeldvorming van leverkanker, multiphotonmicroscopie, autofluorescentie, chirurgische marges, machine learning