Clear Sky Science · nl
De relatie tussen affiniteit en potentie verduidelijken in de prestaties van therapeutische IgE
Allergie-antilichamen inzetten tegen kanker
Allergiepatiënten kennen de kracht van IgE-antilichamen — de moleculen die jeukende ogen en plotseling niezen helpen veroorzaken. Deze studie stelt een verrassende vraag: kan diezelfde krachtige biologie worden hergeleid om kanker te bestrijden, en zo ja, hoe precies moeten deze antilichamen worden afgesteld om het beste te werken? De onderzoekers richtten zich op borstkankers die een eiwit genaamd HER2 maken, waaronder gevallen waarin HER2 in zeer lage hoeveelheden aanwezig is en huidige medicijnen vaak falen.
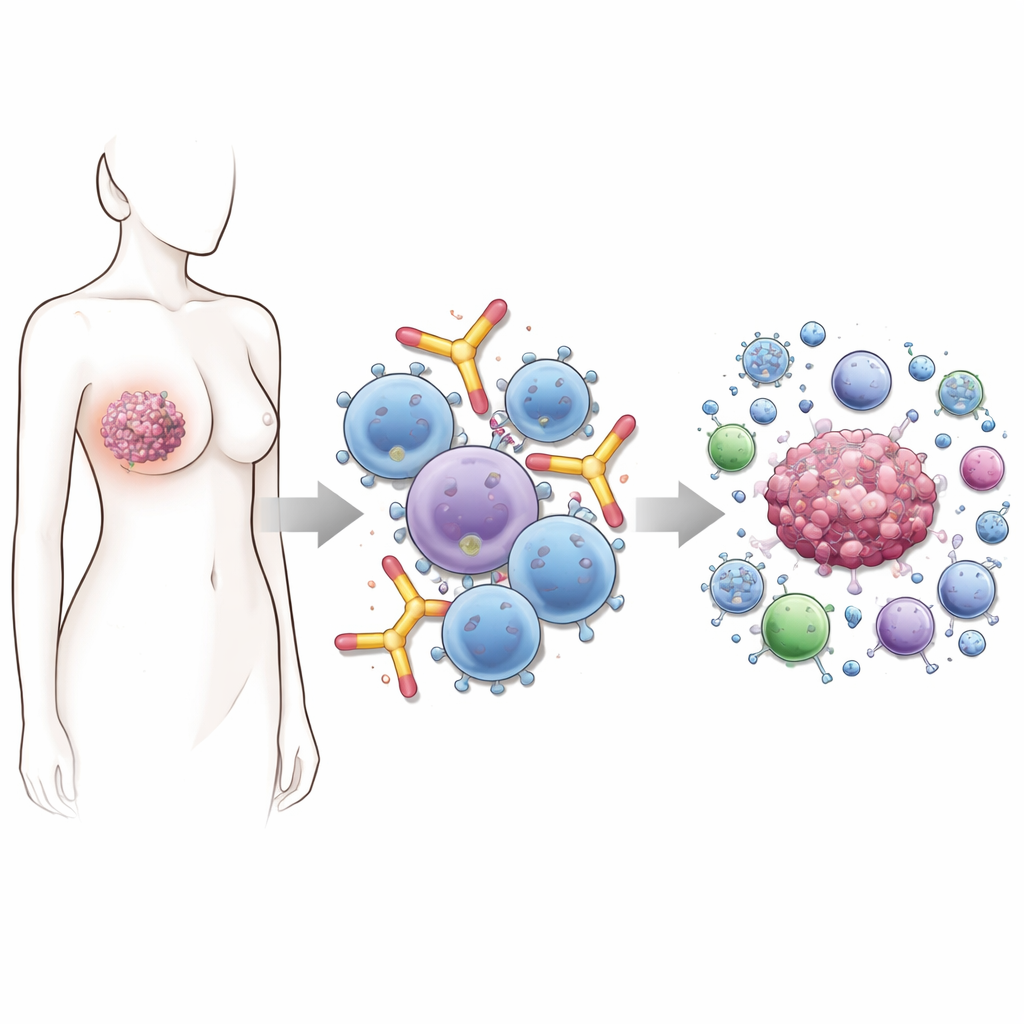
Waarom deze antilichaamklasse zo bijzonder is
De meeste antilichaamgeneesmiddelen op de markt behoren tot de IgG-klasse. Zij zijn de werkpaarden van de moderne kankertherapie, maar hebben beperkingen — vooral wanneer tumoren aanvaltactiek vermijden door de hoeveelheid doelwit-eiwit op hun oppervlak te verlagen. IgE-antilichamen zijn anders. Ze hechten van nature heel sterk aan immuuncellen zoals mestcellen, basofielen, monocyten en macrofagen, en zetten deze klaar voor snelle reacties. Bij allergie betekent dat explosieve reacties op pollen of voedsel. Bij kanker kan diezelfde schakeling snelle, gerichte aanvallen op tumorcellen betekenen zodra IgE zijn doel op het tumormembraan ontmoet.
Een scherper kankerzoekend IgE ontwerpen
Het team had eerder een IgE-antilichaam gemaakt, EPS 226 genoemd, dat HER2 op borstkankercellen herkent en de tumorgroei in experimentele modellen kan vertragen. In dit nieuwe werk wilden ze een subtiele maar cruciale ontwerpvraag beantwoorden: verbetert het sterker laten vastgrijpen van het antilichaam aan HER2 daadwerkelijk zijn vermogen om het immuunsysteem te mobiliseren, of doet de natuurlijke “veelhandige” binding van IgE (avideit) al het merendeel van het werk? Om dit te onderzoeken gebruikten ze gerichte mutagenese en selectiemethoden in bacteriën om miljoenen kleine variaties van het HER2-bindende domein te genereren en selecteerden ze vervolgens 12 nieuwe IgE-varianten die sterker aan HER2 binden dan het oorspronkelijke antilichaam.
Bekijkende werking op cellen en in dieren
Deze verbeterde antilichamen werden daarna op de proef gesteld in een reeks celgebaseerde experimenten. Wanneer ze op mestcellen werden geladen en blootgesteld aan HER2-positieve kankercellen, veroorzaakten de meeste sterker bindende IgE’s sterkere degranulatie — een activatiereactie die krachtige immuunstoffen vrijgeeft. Eén variant, hernoemd EPS 232, viel op door zijn vermogen cellen te activeren terwijl hij nog steeds effectief aan HER2 op menselijke en ratten-tumorcellen bond. Verdere tests toonden aan dat EPS 232 immuuncellen beter toerustte om kanker te doden: het versterkte cel-doding door basofielen en bevorderde efficiëntere fagocytose van HER2-positieve tumorcellen door gemodificeerde immuuncellen en door primaire humane macrofagen. Interessant genoeg hielp het verhogen van de bindingssterkte slechts tot op zekere hoogte; varianten met extreem hoge affiniteit presteerden niet beter dan EPS 232, wat suggereert dat er een “sweet spot” bestaat waarin de greep sterk genoeg is om effectief te zijn maar niet zo sterk dat het het aantal antilichamen en immuuncellen dat elk tumorcel kan engageren, belemmert.
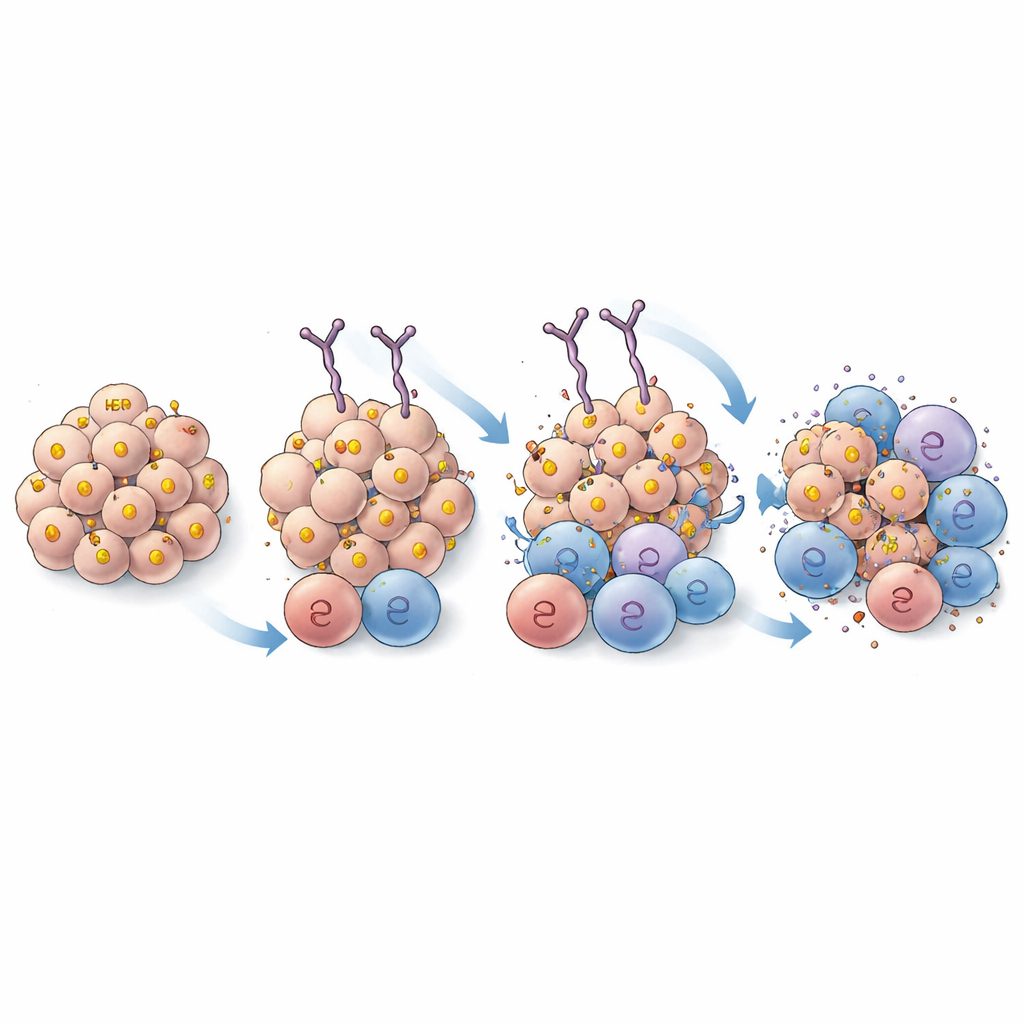
Inzoomen op hoe het antilichaam bindt
Om te verzekeren dat de winst voortkwam uit sterkere greep en niet uit het herkennen van een nieuw stukje HER2, gebruikten de wetenschappers hoogresolutie cryo-elektronenmicroscopie om te visualiseren hoe EPS 232 en het oorspronkelijke EPS 226 op het HER2-eiwit zitten. De structuren toonden aan dat beide antilichamen op hetzelfde gebied van HER2 aanmeren en zeer vergelijkbare contactpunten gebruiken, met slechts subtiele verschillen die naar verwachting de algemene bindingsplaats niet veranderen. Dit ondersteunt het idee dat de verbeterde prestatie van EPS 232 voortkomt uit verbeterde affiniteit in plaats van een verandering in target.
Van laboratorium naar tumorgedrag
De echte test vond plaats in diermodellen. In muizen met menselijke borstkankers en voorzien van menselijke immuuncellen remde EPS 232 de tumorgroei effectiever en bij lagere doseringen dan EPS 226. In ratten met een agressief borstkankermodel dat extreem lage niveaus van HER2 produceert — vergelijkbaar met sommige triple-negatieve borstkankers — vertraagde een aangepaste rattenversie van EPS 232 niet alleen de tumorgroei meer dan zijn voorganger, maar verlengde ook de overleving. Tumoren van behandelde dieren vertoonden verhoogde infiltratie van T-cellen en macrofagen, wat aangeeft dat het verbeterde antilichaam het tumor micro-omgeving beter wist te hervormen naar een toestand die gunstiger is voor immuunaanval.
Wat dit betekent voor toekomstige kankertherapieën
Voor de algemene lezer is de kernboodschap dat het fijn afstemmen van hoe strak een IgE-antilichaam zijn kankertarget vastgrijpt een echt verschil kan maken voor hoe goed het werkt, ook al vormt IgE al veel gelijktijdige contactpunten met cellen. De studie identificeert EPS 232 als een leidende kandidaat voor een IgE-medicijn tegen HER2-positieve en HER2-lage borstkankers, inclusief vormen die momenteel weinig behandelopties hebben. Algemeen laat het zien dat “allergie-stijl” antilichamen kunnen worden ontworpen met de juiste balans van bindingssterkte om een bijna-overgevoelige systeem dat gewoonlijk niezen veroorzaakt, om te vormen tot een systeem dat het immuunsysteem helpt tumoren op te sporen en te elimineren.
Bronvermelding: Marano, F., McKenzie, C., Birtley, J.R. et al. Elucidating the relationship between affinity and potency in the performance of therapeutic IgE. Sci Rep 16, 10555 (2026). https://doi.org/10.1038/s41598-026-43772-6
Trefwoorden: therapeutische IgE, HER2 borstkanker, antilichaamaffiniteit, kankerimmunotherapie, triple-negatieve borstkanker