Clear Sky Science · nl
Op weg naar volledig geautomatiseerde synthetische ECV‑kwantificatie: een open‑toegankelijke machine learning‑benadering voor snelle, bloedafnamevrije CMR
Waarom dit belangrijk is voor hartgezondheid
Artsen vertrouwen steeds vaker op hart‑MRI’s om vroege littekenvorming in de hartspier op te sporen, een subtiele verandering die samenhangt met veel ernstige hartaandoeningen. Tegenwoordig vereist het verkrijgen van deze informatie doorgaans zowel tijdrovende beeldanalyse als een bloedonderzoek. Deze studie laat zien dat een computer speciale hart‑MRI’s automatisch kan uitlezen en zonder bloedafname dezelfde informatie kan schatten, wat de weg opent naar snellere, comfortabelere en mogelijk bredere toegang tot geavanceerde hartdiagnostiek.
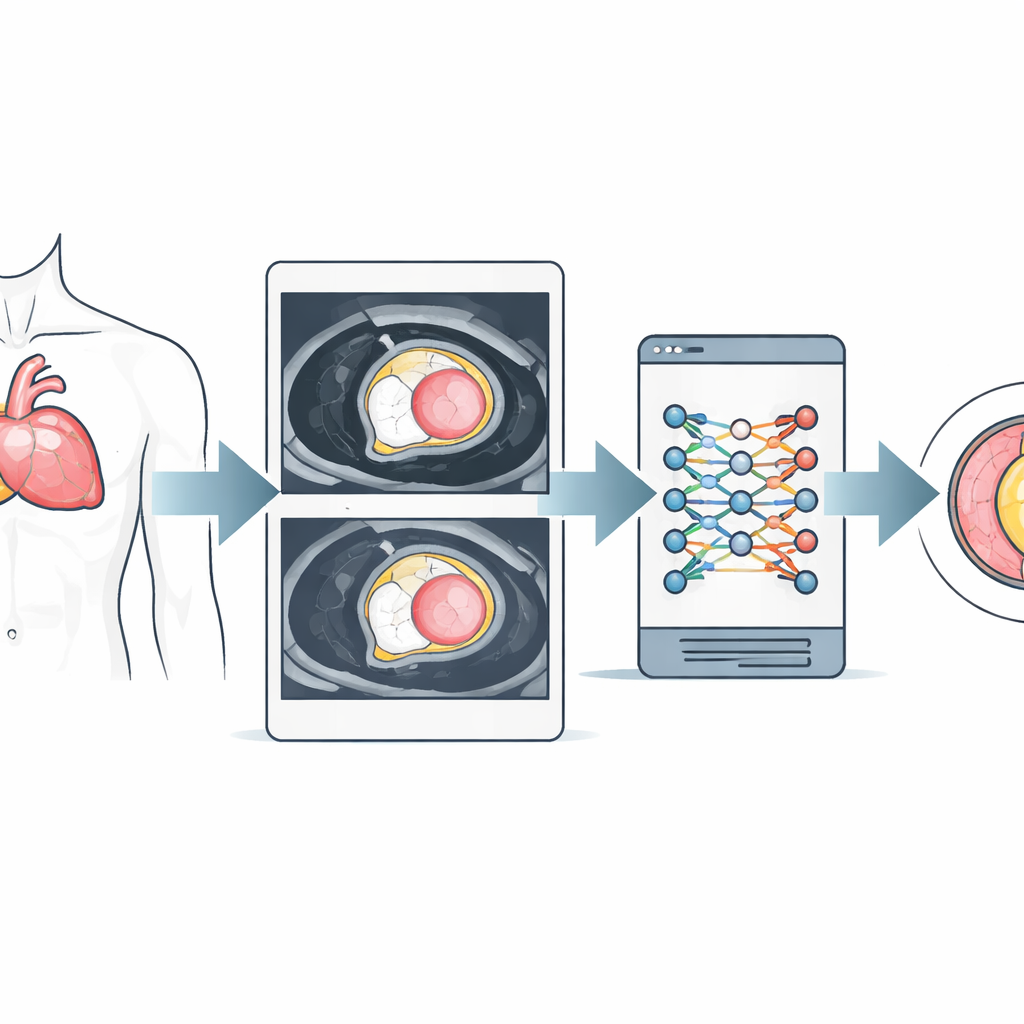
Verborgen littekens in het hart zichtbaar maken
Veel chronische hartaandoeningen veroorzaken fibrose—kleine plekjes littekenachtig weefsel die de hartspier verstevigen en de lange‑termijnuitkomst verslechteren. Moderne cardiale MRI kan iets meten dat extracellulair volume (ECV) wordt genoemd, wat weergeeft hoeveel van de hartspier wordt ingenomen door vloeistof en bindweefsel in plaats van gezonde cellen. ECV is een krachtig beeldvormingsmarker voor diffuse fibrose geworden, maar het praktisch meten ervan is omslachtig. Het vereist meestal handmatig uittekenen van regio’s op meerdere MRI‑beelden, zorgvuldige correctie voor beweging en een recent bloedonderzoek om hematocriet te bepalen, het aandeel rode bloedcellen in het bloed.
Het probleem van bloedtesten en handwerk
In de praktijk vormen deze traditionele werkprocessen een knelpunt. Niet alle centra kunnen rond het tijdstip van de MRI een bloedmonster nemen, en hematocriet kan zelf fluctueren door factoren zo simpel als lichaamshouding. De beeldanalyse is bovendien afhankelijk van getrainde experts, gespecialiseerde software en meerdere handmatige stappen waarbij men hartstructuren laag voor laag omlijnt. Deze stappen vergen tijd en kunnen per lezer of centrum verschillen, wat het moeilijker maakt om resultaten tussen ziekenhuizen of grote onderzoeken te vergelijken.
Een computer leren hartkaarten te lezen
Voortbouwend op eerder werk dat liet zien dat hematocriet direct uit het MRI‑signaal in de bloedbaan van het hart geschat kan worden, wilden de auteurs de rest van het proces automatiseren. Ze gebruikten MRI‑gegevens van meer dan 1000 patiënten die bij twee verschillende magnetische veldsterktes waren gescand. In de trainingsfase tekenden experts zorgvuldig de grenzen van de hartspier en bloedkamers op speciale T1‑“kaarten” gemaakt voor en na contrastinjectie. Deze voorbeelden werden gebruikt om een deep‑learningmodel (een U‑net‑achtig neuronaal netwerk) te trainen om dezelfde structuren automatisch te vinden. Het algoritme voerde ook beeldverwerkingstappen uit om bloed van nabijgelegen weefsel te scheiden en de randen iets in te krimpen om vervaging door beweging te vermijden.
Van ruwe scans naar synthetische ECV in één stap
Eenmaal getraind werd het model getest op een aparte groep patiënten. Voor elke persoon mat het automatisch typische T1‑waarden in de hartspier en het bloed, voerde die waarden in gepubliceerde formules in om hematocriet alleen uit MRI te schatten, en berekende vervolgens een “synthetische” ECV—volledig zonder bloedafname of handmatig contureren. De onderzoekers vergeleken deze volledig geautomatiseerde synthetische ECV met de conventionele ECV die was berekend met deskundige contouren en laboratoriumgemeten hematocriet. In het algemeen kwamen de twee methoden goed overeen: de gemiddelde waarden waren bijna identiek en de correlatie tussen beide was sterk. De overeenstemming was met name goed in het klinisch belangrijke bereik tot ongeveer 35% ECV, waar de meeste patiënten zich bevinden.
Wat goed werkte en waar het moeite heeft
De geautomatiseerde contouren werden over het algemeen door onafhankelijke hartbeeldspecialisten als acceptabel tot uitstekend beoordeeld, en het model ging betrouwbaar om met beelden van beide MRI‑veldsterktes. De verschillen tussen de geautomatiseerde en conventionele metingen werden echter groter bij zeer hoge ECV‑waarden, een bereik dat vaak ernstige ziekte weerspiegelt. De auteurs suggereren dat dit deels komt doordat zulke extreme gevallen zeldzaam waren in de dataset, en deels doordat beeldkwaliteit en lastige anatomie het algoritme kunnen verwarren. Ze merken ook op dat de traditionele referentie een kleine regio in het septum gebruikt, terwijl de geautomatiseerde methode het hele plakje gemiddeld, wat van nature enkele verschillen introduceert.
Wat dit vooruit betekent
Vooralsnog is deze benadering het beste te beschouwen als een onderzoekstool en niet als een kant‑en‑klaar klinisch alternatief. Toch toont het aan dat een computer standaard pre‑ en post‑contrast hart‑MRI‑kaarten kan nemen en, zonder bloedtest en met minimale menselijke invoer, ECV‑waarden kan produceren die in de meeste patiënten dicht bij de huidige arbeidsintensieve metingen liggen. Omdat de code en het getrainde model openlijk beschikbaar zijn, kunnen andere centra de methode testen, verfijnen en aanpassen aan hun eigen scanners. Als verdere validatie volgt—vooral bij patiënten met zeer hoge ECV—zou volledig geautomatiseerde, bloed‑vrije ECV‑bepaling de beoordeling van geavanceerde fibrose sneller, consistenter en breder toegankelijk kunnen maken.
Bronvermelding: Beyer, R.E., Hüllebrand, M., Doeblin, P. et al. Towards fully automated synthetic ECV quantification: an open-access machine learning-based approach for fast blood draw-free CMR. Sci Rep 16, 8552 (2026). https://doi.org/10.1038/s41598-026-43624-3
Trefwoorden: cardiale MRI, myocardiale fibrose, extracellulair volume, deep learning, automatisering medische beeldvorming